
科目: 来源: 题型:
【题目】在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中。
(1)________元素被氧化,________是氧化剂。
(2)________是氧化产物,________发生氧化反应。
(3)在参加反应的盐酸中,起还原剂(被氧化)作用的HCl与起酸性作用的HCl的质量比为_______。
(4)用双线桥法标明电子转移的方向和数目。____________________
查看答案和解析>>
科目: 来源: 题型:
【题目】在某恒温恒容的密闭容器内发生反应:2A(g)+B(g)![]() C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是
C(g)△H<0。开始充入2mol A和2mol B,并达到平衡状态,下列说法正确的是
A. 再充入2mol A,平衡正移,A的转化率增大
B. 如果升高温度,C的体积分数增大
C. 如果增大压强,化学平衡一定向正反应方向移动,B的体积分数减小
D. 再充入1mol C,C的物质的量浓度将增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,向2 L恒容密闭容器中加入2 mol X、1 mol Y。发生如下反应:2X(g)+Y(?)![]() 3Z(g) ΔH=-a kJ·mol-1(a>0)。经60 s达平衡,此时Y的物质的量为0.2 mol。下列说法错误的是( )
3Z(g) ΔH=-a kJ·mol-1(a>0)。经60 s达平衡,此时Y的物质的量为0.2 mol。下列说法错误的是( )
A.0~60 s内,用Z表示的化学反应速率为1.2 mol·L-1·min-1
B.若再充入1 mol Z,重新达到平衡时,X的体积分数不变,则Y为气态
C.达平衡后,实际放出的热量为b kJ,则b=a
D.若Y为气态,则使容器体积变为1 L,Z的物质的量不变
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如右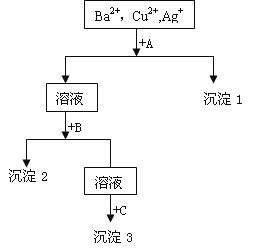
(1)沉淀的化学式:沉淀1___________,沉淀2__________,沉淀3____________;
(2)写出混合液+A的离子方程式________________________________________;
溶液+B的离子方程式_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】烯烃是重要的有机化合物.其中乙烯是最简单的一种烯烃,其产量代表着一个国家石油化工产业的水平。
完成下列问题:
(1)实验室用如图所示装置制取乙烯,反应方程式是____,无水乙醇与浓硫酸的体积比为1:3,请解释加入浓硫酸不宜过少的原因是__。

(2)反应需要迅速升温至所需温度的理由是___。所以烧瓶中应放入的固体物质是___,其作用是____。
(3)烯烃通过催化加氢可以得到烷烃。请写出一种可以通过催化加氢反应得到2,2-二甲基丁烷的结构简式:___。
(4)有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到。请写出A的结构简式___,在A的同分异构体中,却存在只能由1种烯烃催化加氢得到的烷烃,请写出一种符合要求的A的同分异构体的结构简式:___。
烯烃还可以与卤素单质、卤化氢、水发生加成反应,产物有主次之分,例如:


(5)化学式为C4H8的某烃A与HBr加成得到的主要产物,其一氯代物只有一种,请写出A发生聚合反应的方程式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是____________。
(2)该反应中,发生还原反应的过程是______________→____________。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目_____________。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下的体积为 。
(5)已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为:SO2>I->H2O2>Fe2+>Cl-,则下列反应不能发生的是( )
A.2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
B.I2+SO2+2H2O=H2SO4+2HI |
C.H2O2+H2SO4=SO2↑+O2↑+2H2O |
D.2Fe3++2I-=2Fe2++I2 |
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上从钴渣[含Co(OH)3、Fe(OH)3等]中回收钴的两种方法如下:
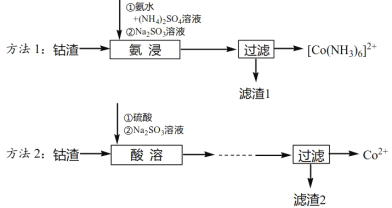
已知:
①Ksp[Co(OH)3]=1.6×10-44,Ksp[Co(OH)2]=6.3×10-15,Ksp[Fe(OH)3]=4.0×10-38。
②碱性条件下,Fe(OH)3不与亚硫酸钠反应;Fe3++NH3→不发生类似Co2+、Co3+的配位化学反应。
请回答下列问题:
(1)方法1“氨浸”时用的氨水的质量百分数为a,密度为ρg·cm-3,该氨水的物质的量浓度为_____mol·L-1,“氨浸”过程中发生反应的离子方程式为_______。
(2)方法1“氨浸”时,未加Na2SO3溶液和加入Na2SO3溶液时的钴浸出率如图1所示。请解释两种情况下钴浸出率不同的原因:______。
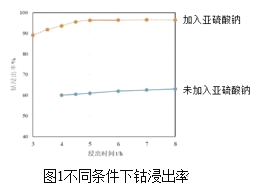
(3)方法1中,浸出温度对钴浸出率的影响如图2所示,工业上选择50℃而不是更高温度的可能的原因是_____。
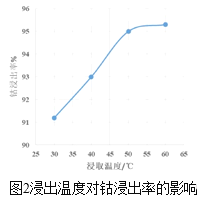
(4)方法2中,为提高酸溶速率,可采取的措施是______(写出一条即可)。
(5)对比方法1和方法2,从物质分离的角度分析方法1的优点是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学反应的离子方程式正确的是
A. 钠和冷水反应:Na+2H2O=Na++2OH﹣+H2↑
B. 用小苏打治疗胃酸过多:![]() +H+=CO2↑+H2O
+H+=CO2↑+H2O
C. 氯化铝溶液中加入过量氨水:Al3++3OH﹣=Al(OH)3↓
D. 三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】CuH不稳定,易跟盐酸反应:2CuH+2HCl![]() CuCl2+2H2↑+Cu。下列说法正确的是
CuCl2+2H2↑+Cu。下列说法正确的是
A. CuH中H的化合价为+1 B. CuH在反应中只被还原
C. 在反应中HCl失去电子 D. Cu是反应的还原产物
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机物合成中的重要试剂,可由NO与Cl2在常温常压下反应得到。ClNO部分性质如下:黄色气体,熔点:-59.6℃,沸点:-6.4℃,遇水易水解。某研究性学习小组根据亚硝酰氯(ClNO)性质拟在通风橱中制取亚硝酰氯,设计了如下实验装置。、

试回答下列问题:
(1)写出实验室利用装置A制备Cl2的离子反应方程式___。
(2)装置B的作用是①__,②___。
(3)若用A装置制取NO气体,B中应该盛放__。
(4)为使NO和Cl2恰好完全反应生成ClNO,理论上向E中通入NO和Cl2两种气体的流速比为__。
(5)装置H吸收尾气,有同学认为尾气中的某种气体不能完全被吸收。为了充分吸收尾气,可将尾气与__同时通入NaOH溶液中。
(6)已知:ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸:__。(仅提供的试剂:1molL-1HCl、1molL-1HNO2溶液、NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)。
②通过以下实验测定ClNO样品的纯度。取F中所得液体3.0g溶于水,配制成250mL溶液;取出25.00mL样品溶液置于锥形瓶中,用0.20molL-1AgNO3标准溶液滴定至终点,根据表中所给信息,应选用___做指示剂。
物质 | Ag2CrO4 | AgCl | AgI | Ag2S |
颜色 | 砖红色 | 白色 | 黄色 | 黑色 |
Ksp | 1×10-12 | 1.56×10-10 | 8.3×10-17 | 6.3×10-50 |
消耗标准AgNO3溶液的体积为20.00ml,亚硝酰氯(ClNO)的质量分数为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com