
科目: 来源: 题型:
【题目】(1)已知:常温下浓度为0.1mol/L的下列溶液的pH如表
溶质 | NaCl | CH3COOK | Na2CO3 | NaClO | NaHCO3 |
pH | 7 | 8.1 | 11.6 | 9.7 | 8.3 |
①等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:Cl-_________ClO-,浓度相等的NaClO和CH3COOK溶液中:[c(Na+)-c(ClO-)]__________[c(K+)-c(CH3COO-)](填“>”“<”或“=”)
②HCO3-的水解常数为__________(填写具体数值),在相同温度下,同浓度的CH3COOH、H2CO3、HClO三种酸溶液的导电能力大小为__________
(2)常温下,向pH=a的醋酸中加入等体积NaOH时后呈中性,则此NaOH的pH_____14-a(>、<、=)
(3)常温下,已知0.1mol﹒L-1一元酸HA溶液中![]() =1×10-6。
=1×10-6。
①常温下,0.1mol﹒L-1HA溶液的pH=_____;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是:_____。
(4)常温下,amol/L氨水与等体积0.1mol/LH2SO4溶液混合后溶液显中性,则NH3·H2O的电离平衡常数Kb=_____
查看答案和解析>>
科目: 来源: 题型:
【题目】糖类、油脂、蛋白质是维持人体生命活动所必需的营养物质,下列叙述不正确的是( )
A.将碘酒滴到土豆片上,土豆片变蓝,说明碘元素均遇淀粉变蓝
B.工业上常用油脂在碱性条件下的水解反应来制肥皂
C.加热条件下,葡萄糖溶液能与新制![]() 悬浊液反应产生砖红色沉淀
悬浊液反应产生砖红色沉淀
D.蛋白质在浓硝酸作用下能发生颜色反应,可用来鉴别部分蛋白质
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是一些常见元素的单质或化合物之间的转化关系。溶液中的水及部分反应物或生成物未标出。A、E是空气的两种主要成分;反应①是在1500℃隔绝空气的条件下发生的,其中生成物D是单质。C是由两种元素组成的新型材料,且和SiC具有相同的最外层子数和原子数,J是一种能引起温室效应的气体,K是两性化合物,反应③、④、⑤用于工业中生产H。
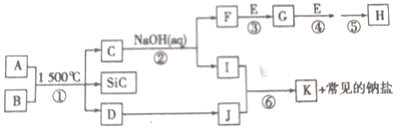
请回答下列问题。
(1)A的电子式:_____________;I的化学式:_____________;H的化学式:_____________。
(2)写出反应③的化学方程式:____________。
(3)写出反应⑥的离子方程式(J少量):_________。写出反应②的离子方程式:_________。
(4)B和SiC的纳米级复合粉末是新一代大规模集成电路理想的散热材料,反应①是科学家研究开发制备该纳米级复合材料的最新途径。已知:B由Si及另外两种元素组成,且Si与另外两种元素的物质的量之比均为1:4。请写出反应①的化学方程式:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关乙烯和乙烷的说法中错误的是![]()
![]()
A. 乙烯是平面分子,乙烷分子中所有原子不可能在同一平面内
B. 溴的四氯化碳溶液和酸性![]() 溶液都可以鉴别乙烯和乙烷
溶液都可以鉴别乙烯和乙烷
C. 溴的四氯化碳溶液和酸性![]() 溶液都可以除去乙烷中混有的乙烯
溶液都可以除去乙烷中混有的乙烯
D. 乙烯的化学性质比乙烷的化学性质活泼
查看答案和解析>>
科目: 来源: 题型:
【题目】固体硝酸盐受热易分解且产物较复杂。已知KNO3、Cu(NO3)2、AgNO3三种硝酸盐的热分解反应的化学方程式如下:
Ⅰ:2KNO3 ![]() 2KNO2+O2↑
2KNO2+O2↑
Ⅱ:2Cu(NO3)2 ![]() 2CuO+4NO2↑+O2↑
2CuO+4NO2↑+O2↑
Ⅲ:2AgNO3![]() 2Ag+2NO2↑+O2↑
2Ag+2NO2↑+O2↑
某固体可能由KNO3、Cu(NO3)2、AgNO3三种硝酸盐中的一种或几种组成。取适量该固体充分加热,得到一定量气体,该气体经水充分吸收后,剩余气体的体积在同温、同压下为吸收前的![]() (忽略氧气在水中的溶解)
(忽略氧气在水中的溶解)
(1)若该固体只由一种盐组成,则该盐为___________________,
(2)若该固体是混合物,则该混合物的可能组成为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】过一硫酸氢钾复合盐(KHSO4·2KHSO5·K2SO4)常用作漂白剂和消毒剂,其制备流程如下:
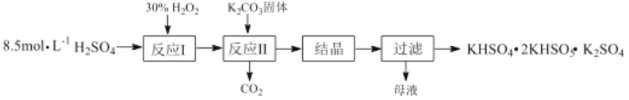
(1)反应Ⅰ的化学方程式为:H2O2+H2SO4![]() H2SO5+ H2O,△H<0;则反应Ⅱ中K2CO3与H2SO5反应生成KHSO5的化学方程式为_____________。
H2SO5+ H2O,△H<0;则反应Ⅱ中K2CO3与H2SO5反应生成KHSO5的化学方程式为_____________。
(2)生产原料的理论比值[n(H2O2):n(H2SO4)]为0.4:1,但实际生产最佳投料比为 0.6:1,其原因是_________________。
(3)过一硫酸氢钾复合盐可以处理废水中的H2S。己知:25℃,H2S的电离常数Ka1=1.1×10-7, Ka2=1.3×10-13由于电离常数值极小,H2S水溶液中H2S的平衡浓度近似等于H2S的初始浓度。0.090 mol·L-1H2S溶液的pH=4,该溶液中c(S2-)=________________。
(4)准确称取3.350g复合盐样品配制成250mL溶液,取25.00 mL置于锥形瓶中,加入适量的稀硫酸和足量的KI溶液,摇匀后置于暗处,充分反应后,加入少量淀粉溶液,用0.1000 mol·L-1Na2S2O3标准溶液滴定至终点,消粍标准溶液20.00 mL。计算复合盐中有效成分KHSO5的质量分数。(写出计算过程)(已知:HSO5- ![]() I2
I2 ![]() S4O62-)________________________。
S4O62-)________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下含碳各微粒H2CO3、HCO3-和CO32-存在于CO2和NaOH溶液反应后的溶液中,它们的物质的量分数与溶液pH的关系如图所示,下列说法错误的是( )

A. 为获得尽可能纯的NaHCO3,宜控制溶液的pH为7~9之间
B. pH=10.25时,c(Na+)=c(CO32-)+c(HCO3-)
C. 根据图中数据,可以计算得到H2CO3第一步电离的平衡常数K1(H2CO3)=10-6.37
D. 若是0.1mol NaOH反应后所得的1L溶液,pH=10时,溶液中存在以下关系: c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,pH均为2、体积均为V0的HA、HB、HC溶液,分别加水稀释至体积为V,溶液pH随lg![]() 的变化关系如图所示,下列叙述错误的是( )
的变化关系如图所示,下列叙述错误的是( )
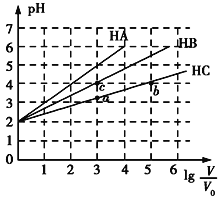
A.常温下:Ka(HB)>Ka(HC)
B.HC的电离度:a点<b点
C.当lg![]() =4时,三种溶液同时升高温度,
=4时,三种溶液同时升高温度,![]() 减小
减小
D.当lg![]() =5时,HA溶液的pH为7
=5时,HA溶液的pH为7
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在粗制MgCl2晶体中常含有杂质Fe2+,在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质最好采用的是_________(填下面的选项),加入该氧化剂时,温度不能太高,原因是_________。
A.KMnO4 B.H2O2 C.HNO3 D.氯水
然后再加入适当物质调节溶液pH,可以达到除去Fe3+而不损失MgCl2的目的,调节溶液pH可选用下列中的有_________。
A.Mg2(OH)2CO3 B.MgO C.NH3·H2O D.Mg(OH)2
某溶液中含Mg2+和Fe3+,c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全,即溶液中c(Fe3+)=1.0×10-5mol/L,此时是否有Mg3(PO4)2沉淀生成?_________(FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24)
(2)常温下Ksp[Fe(OH)3]=8.0×1038,Ksp[Cu(OH)2]=3.0×1020,通常认为残留在溶液中的离子浓度小于1×105molL1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0molL1,为除去溶液中的Fe3+而不影响Cu2+,溶液的pH的范围为_________。(已知lg5=0.7)。
(3)矿物中各种原生铜的硫化物经氧化、淋滤后可变成CuSO4溶液,并向内部渗透,遇到深层的闪锌矿(ZnS)和方铅矿(PbS),可慢慢转化为铜蓝(CuS)。写出硫酸铜与ZnS反应的离子方程式为:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知常温下Cu能与Fe3+发生反应:Cu+2Fe3+=Cu2++2Fe2+现将铜粉与二氧化二铁的混合物22.4g加入到1mol/L的H2SO4溶液中进行反应。
(1)若固体恰好溶解,消耗硫酸的体积为V,则V的取值范围是_______。
(2)若硫酸溶液过量,反应后溶液的体积为1L,测得此溶液中Fe2+的浓度为0.1mol/L,则混合物中含铜_______g或_______g(只需写出结果)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com