
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΔώ. (1) “―÷ΣS4ΒΡΫαΙΙ Ϋ»γΆΦΘ§Ζ¥”ΠS4(g) + 4Cl2(s )== 4SCl2(g) ΓςH= - 4 kJΓΛmol-1Θ§SΓΣSΦϋΒΡΦϋΡήΈΣ266 kJΓΛmol-1Θ§SΓΣClΦϋΒΡΦϋΡήΈΣ255 kJΓΛmol-1Θ§‘ρ1mol Cl2(g)Ζ÷Ή”÷–ΒΡΜ·―ßΦϋΕœΝ― ±–η“ΣΈϋ ’ΒΡΡήΝΩΈΣ_____kJΓΘ
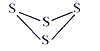
Δρ. ΙΛ“Β…œΚœ≥…¬»Μ·―«μΩΖ¥”ΠΘΚSO2(g)+ SCl2(g)+Cl2(s)![]() 2SOCl2(g)Θ§ΗΟΖ¥”Π÷–Ρ≥“ΜΖ¥”ΠΈοΒΡΧεΜΐΖ÷ ΐ(“‘A%±μ Ψ)ΥφΈ¬Ε»ΒΡ±δΜ·ΙΊœΒ»γΆΦΥυ ΨΓΘ
2SOCl2(g)Θ§ΗΟΖ¥”Π÷–Ρ≥“ΜΖ¥”ΠΈοΒΡΧεΜΐΖ÷ ΐ(“‘A%±μ Ψ)ΥφΈ¬Ε»ΒΡ±δΜ·ΙΊœΒ»γΆΦΥυ ΨΓΘ
(2) ‘Ύ373K ±Θ§œρ2LΟή±’»ίΤς÷–Ά®»κΈο÷ ΒΡΝΩΨυΈΣ0.04 molΒΡSO2ΓΔSCl2”κCl2Θ§ ΖΔ…ζ…œ ωΖ¥”ΠΓΘ≤βΒΟΤδ―Ι«Ω(p)Υφ ±Φδ(t)ΒΡ±δΜ·ΈΣœ¬±μ÷– ΐΨίΔώ(ΤΫΚβ ±ΒΡΈ¬Ε»”κΤπ ΦΈ¬Ε»œύΆ§)
t/min | 0 | 1 | 2 | 3 | 4 | 5 |
Δώ | 6.0p0 | 6.7 p0 | 6.1 p0 | 5.4 p0 | 5.0 p0 | 5.0 p0 |
Δρ | 6.0 p0 | 7.0 p0 | 5.3 p0 | 5.0 p0 | 5.0 p0 | 5.0 p0 |
ΔΌΗΟΖ¥”ΠΒΡΓςH_____0(ΧνΓΑΘΨΓ±ΓΑΘΦΓ±ΜρΓΑ=Γ±)ΓΘ
ΔΎΖ¥”ΠΩΣ Φ÷Ν¥οΒΫΤΫΚβ ±Θ§v(SCl2)=__________ΓΘ
Δέ»τ÷ΜΗΡ±δΡ≥“ΜΧθΦΰΘ§≤βΒΟΤδ―Ι«ΩΥφ ±ΦδΒΡ±δΜ·ΈΣ±μ÷– ΐΨίΔρΘ§‘ρΗΡ±δΒΡΧθΦΰ «_______________ΓΘ
(3) œ¬ΆΦ «Ρ≥Ά§―ß≤βΕ®ΒΡ…œ ωΖ¥”ΠΒΡpK(pK= - lgK)”κΈ¬Ε»ΒΡ±δΜ·ΙΊœΒΆΦΓΘ

ΔΌ AΒψΒΡ ΐ÷ΒΈΣ_________(“―÷Σlg4=0.6)ΓΘ
ΔΎΒ±…ΐΗΏΒΫΡ≥“ΜΈ¬Ε» ±Θ§Ζ¥”Π÷Ί–¬¥οΒΫΤΫΚβΘ§AΒψΩ…Ρή±δΜ·ΈΣ______ΒψΓΘ
III. (4) ΒγΫβNO2÷Τ±ΗNH4NO3Θ§ΤδΙΛΉς‘≠άμ»γΆΦΥυ ΨΓΘ
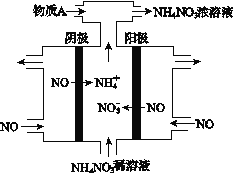
ΔΌ“θΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ_________________________ΓΘ
ΔΎΈΣ ΙΒγΫβ≤ζΈο»Ϊ≤ΩΉΣΜ·ΈΣNH4NO3Θ§–η≤Ι≥δΡ≥÷÷Έο÷ AΘ§‘ρAΒΡΜ·―ß ΫΈΣ___________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ25Γφ ±Θ§œρ“ΜΕ®≈®Ε»ΒΡNa2X»ή“Κ÷–ΒΈ»κ―ΈΥαΘ§»ή“ΚΒΡpH”κάκΉ”≈®Ε»±δΜ·ΙΊœΒ»γΆΦΥυ ΨΓΘ

“―÷ΣΘΚH2X «Εΰ‘Σ»θΥαΘ§Y±μ Ψ![]() Μρ
Μρ![]() Θ§pYΘΫ©¹lgYΘ°œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
Θ§pYΘΫ©¹lgYΘ°œ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
A. «ζœΏn±μ ΨpH”κp![]() ΒΡ±δΜ·ΙΊœΒ
ΒΡ±δΜ·ΙΊœΒ
B. Ka2Θ®H2XΘ©ΘΫ1.0ΓΝ10©¹10.3
C. NaHX»ή“Κ÷–cΘ®H+Θ©ΘΨcΘ®OH©¹Θ©
D. Β±»ή“Κ≥ ÷––‘ ±Θ§cΘ®Na+Θ©ΘΫcΘ®HX©¹Θ©+2cΘ®X2©¹Θ©+cΘ®Cl©¹Θ©
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–άκΉ”ΖΫ≥Χ Ϋ ι–¥’ΐ»ΖΒΡ «( )
A. Β―ι “”Ο¬»Μ·οßΚΆ λ ·Μ“÷ΤΑ±ΘΚNH4+ΘΪOHΘ≠![]() NH3ΓϋΘΪH2O
NH3ΓϋΘΪH2O
B. NaOH»ή“Κ”κNH4Cl»ή“ΚΜλΚœΦ”»»ΘΚNH4+ ΘΪOHΘ≠![]() NH3ΓΛH2O
NH3ΓΛH2O
C. Α±Υ°÷–Φ”―ΈΥαΘΚNH3ΓΛH2OΘΪHΘΪ=NH4+ΘΪH2O
D. Α±Υ°÷–Φ”»κ¬»Μ·Χζ»ή“ΚΘΚFe2ΘΪΘΪ2NH3ΓΛH2O=2NH4+ΘΪFe(OH)2Γΐ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ2A1+MoO3![]() Mo+Al2O3”Ο”Ύ÷Τ±ΗΫπ τνβ(Mo)ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
Mo+Al2O3”Ο”Ύ÷Τ±ΗΫπ τνβ(Mo)ΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A.AlΒΟΒγΉ”B.Al2O3 «―θΜ·ΦΝ
C.MoO3 ΖΔ…ζΜΙ‘≠Ζ¥”ΠD.ΟΩ…ζ≥…1molMo”–3molΒγΉ”ΉΣ“Τ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈ“ΙζΩΤ―ßΦ“―–ΖΔΝΥ“Μ÷÷ “Έ¬œ¬ΓΑΩ…ΚτΈϋΓ±ΒΡNaΓΣCO2Εΰ¥ΈΒγ≥ΊΓΘΫΪNaClO4»ή”Ύ”–Μζ»ήΦΝΉςΈΣΒγΫβ“ΚΘ§ΡΤΚΆΗΚ‘ΊΧΦΡ…ΟΉΙήΒΡΡχΆχΖ÷±πΉςΈΣΒγΦΪ≤ΡΝœΘ§Βγ≥ΊΒΡΉήΖ¥”ΠΈΣΘΚ3CO2+4Na![]() 2Na2CO3+CΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «
2Na2CO3+CΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «

A. Ζ≈Βγ ±Θ§ClO4Θ≠œρΗΚΦΪ“ΤΕ·
B. ≥δΒγ ± ΆΖ≈CO2Θ§Ζ≈Βγ ±Έϋ ’CO2
C. Ζ≈Βγ ±Θ§’ΐΦΪΖ¥”ΠΈΣΘΚ3CO2+4e ΘΫ2CO32Θ≠+C
D. ≥δΒγ ±Θ§’ΐΦΪΖ¥”ΠΈΣΘΚNa++eΘΫNa
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩBΓΔEΓΔH «…ζΜν÷–≥ΘΦϊΒΡ”–ΜζΈοΘ§H≥Θ”Ο”Ύ ≥ΤΖΑϋΉΑΘ§AΒΡ≤ζΝΩ « ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΒΡ±ξ÷ΨΓΘΗυΨί»γΆΦΉΣΜ·ΙΊœΒΜΊ¥πΈ ΧβΘΚ
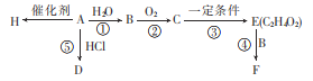
(1)–¥≥ωAΚΆF÷–ΙΌΡήΆ≈ΒΡΟϊ≥ΤΘΚA___Θ§F___ΓΘ
(2)Ζ¥”ΠΔΌΓΔΔήΒΡΖ¥”Πάύ–ΆΖ÷±πΈΣ___ΓΔ___ΓΘ
(3)–¥≥ωDΚΆEΒΡΫαΙΙΦρ ΫΘΚD___ΓΔE___ΓΘ
(4)«κ–¥≥ωœ¬Ν–Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
IΘ°–¥≥ωΖ¥”ΠΔΎ‘Ύ¥ΏΜ·ΦΝ¥φ‘ΎΒΡΧθΦΰœ¬≤ΔΦ”»»ΒΡΜ·―ßΖΫ≥Χ ΫΘΚ___ΓΘ
IIΘ°AΓζHΒΡΜ·―ßΖΫ≥Χ ΫΘΚ___ΓΘ
(5)H «“Μ÷÷≥ΘΦϊΒΡΗΏΖ÷Ή”≤ΡΝœΘ§”…’β÷÷≤ΡΝœ‘λ≥…ΒΡΜΖΨ≥Έ Χβ «___ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡΤΝρΒγ≥Ί“‘»έ»ΎΫπ τΡΤΓΔ»έ»ΎΝρΚΆΕύΝρΜ·ΡΤ(Na2Sx)Ζ÷±πΉςΈΣΝΫΗωΒγΦΪΒΡΖ¥”ΠΈοΘ§ΙΧΧεAl2O3Χ’¥…(Ω…¥ΪΒΦNaΘΪ)ΈΣΒγΫβ÷ Θ§Τδ‘≠άμ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
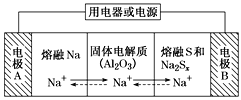
A.Ζ≈Βγ ±Θ§ΒγΦΪAΈΣ’ΐΦΪ
B.≥δΒγ ±Θ§Na+ ¥”ΒγΦΪAœρΒγΦΪB«®“Τ
C.≥δΒγ ±Θ§ΒγΦΪBΖ¥”Π ΫΈΣS22-- 2e- === xS
D.ΗΟΒγ≥ΊΙΛΉςΒΡ “ΥΈ¬Ε»”ΠΩΊ÷Τ‘Ύ25 ΓφΉσ”“
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΫΪ Σ»σΒΡΚλ…Ϊ ·»ο ‘÷ΫΖ≈‘ΎΫχ––œ¬Ν– Β―ιΒΡ ‘ΙήΩΎΘ§ ‘÷Ϋ≤Μ±δάΕ…ΪΒΡ”–(ΓΓΓΓ)
A.Φ”»»≈®Α±Υ°
B.Φ”»»NH4HCO3ΙΧΧε
C.Φ”»»NH4ClΚΆCa(OH)2ΒΡΜλΚœΈο
D.Φ”»»±ΞΚΆNH4Cl»ή“Κ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “÷Τ»ΓœθΜυ±ΫΒΡ÷ς“Σ≤Ϋ÷η»γœ¬ΘΚ
ΔΌΫΪ≈δ÷ΤΚΟΒΡ≈®ΝρΥα”κ≈®œθΥαΒΡΜλΚœΥαΘ§ά以ΚσΦ”»κ ‘Ιή÷–ΓΘ
ΔΎœρΜλΚœΥα÷–÷πΒΈΦ”»κ“ΜΕ®ΝΩΒΡ±ΫΘ§≥δΖ÷’ώΒ¥Θ§ΜλΚœΨυ‘»ΓΘ
ΔέΥ°‘ΓΦ”»»ΖΔ…ζΖ¥”ΠΓΘ
ΔήΖ¥”ΠΫα χΚσΘ§¥ΐΜλΚœ“Κά以ΚσΉΣ“Τ÷ΝΖ÷“Κ¬©ΕΖ÷–Θ§≥ΐ»ΞΜλΚœΥαΘ§¥÷≤ζΤΖ“ά¥Έ”Ο’τΝσΥ°ΚΆ10%ΒΡNa2CO3»ή“Κœ¥Β”Θ§‘Ό”Ο’τΝσΥ°œ¥Β”Θ§ΒΟ¥÷œθΜυ±ΫΓΘ
ΔίΫΪ¥÷œθΜυ±Ϋ”ΟΈόΥ°CaCl2Η…‘οΚσ’τΝσΒΟΒΫ¥ΩœθΜυ±ΫΓΘ

ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)≈δ÷Τ“ΜΕ®±»άΐ≈®ΝρΥαΚΆ≈®œθΥαΒΡΜλΚœΥαΒΡ≤ΌΉς «___ΓΘ
(2)≤Ϋ÷ηΔέ÷–Θ§Υ°‘ΓΦ”»»ΒΡ”≈Βψ «___ΓΘ
(3)ΆΦ÷–≥Λ≤ΘΝßΒΦΙήΒΡΉς”Ο «___ΓΘ
(4)–¥≥ω÷Τ»ΓœθΜυ±ΫΒΡΜ·―ßΖΫ≥Χ ΫΘΚ___ΓΘ
(5)≤Ϋ÷ηΔή÷–¥÷≤ζΤΖ”Ο10%ΒΡNa2CO3»ή“Κœ¥Β”ΒΡΡΩΒΡ «___ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Έ¬Ε»œ¬Θ§œρΧεΜΐΈΣ2LΒΡΚψ»ίΟή±’»ίΤς÷–Ά®»κ2molN2ΚΆ6molH2Θ§‘Ύ“ΜΕ®ΧθΦΰœ¬ΖΔ…ζΖ¥”ΠΘΚN2(g)+3H2(g)![]() 2NH3(g)ΓΘ Β―ι≤βΒΟΖ¥”ΠΨ≠5minΚσ¥οΒΫΤΫΚβΘ§¥Υ ±ΜλΚœΈοΒΡΉήΈο÷ ΒΡΝΩΈΣ5.6molΘ§«σΘΚ
2NH3(g)ΓΘ Β―ι≤βΒΟΖ¥”ΠΨ≠5minΚσ¥οΒΫΤΫΚβΘ§¥Υ ±ΜλΚœΈοΒΡΉήΈο÷ ΒΡΝΩΈΣ5.6molΘ§«σΘΚ
(1)ΤΫΚβ ±NH3ΒΡ≈®Ε»ΈΣ___molΓΛL-1ΓΘ
(2)0~5minΡΎΘ§v(H2)=___molΓΛL-1ΓΛmin-1ΓΘ
(3)Ζ¥”Π¥οΒΫΤΫΚβ ±Θ§N2ΒΡΉΣΜ·¬ ΈΣ___ΓΘ
(4)œ¬Ν–ΆΦœσ÷–ΡήΖ¥”≥ΗΟΖ¥”ΠΒΡΡήΝΩ±δΜ·ΒΡ «___(Χν±ξΚ≈)ΓΘ
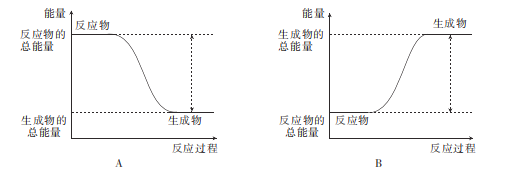
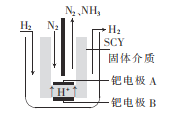
(5)»τ“‘N2ΚΆH2Κœ≥…Α±ΒΡΖ¥”Π…ηΦΤ»γΆΦΥυ ΨΒΡ‘≠Βγ≥ΊΘ§‘ρΆ®»κN2ΒΡ“ΜΦΪΈΣ__(ΧνΓΑ’ΐΓ±ΜρΓΑΗΚ")ΦΪΘΜΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ___ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com