
科目: 来源: 题型:
【题目】在t℃下,某反应达到平衡,平衡常数K=![]() 。恒容时,温度升高时NO浓度减小。下列 说法正确的是
。恒容时,温度升高时NO浓度减小。下列 说法正确的是
A.该反应的焓变为正值
B.若恒温下增大压强(缩小体积),则反应体系的颜色加深
C.在t℃时,加入催化剂,该反应的化学平衡常数增大
D.该反应化学方程式为NO+SO3![]() NO2+SO2
NO2+SO2
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)铝热反应在工业生产中的重要用途之一是_________________;用化学方程式表示出其中的原理________________________________________(举一例)。铝制品因为表面易形成致密的氧化铝薄膜而经久耐用,但是该氧化膜易被酸碱破坏,若将氧化铝与氢氧化钠溶液作用,反应的化学方程式为____________________________________。
(2)氯气用于漂白、消毒时,能起漂白、消毒作用的物质是____________(写化学式)。缺铁性贫血患者应补充Fe元素,通常以硫酸亚铁的形式给药,而硫酸铁则没有这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是_______________。
(3)镁带着火时,不能用液态CO2灭火剂来灭火的原因是_________。(用化学方程式表示)。
(4)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C=2AlN+3CO。
①在化学方程式上标出该反应中电子转移的方向和数目。_________
②在该反应中,氧化剂是________________ ,氧化产物是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol·L-1Na2SO4溶液,下列叙述正确的是
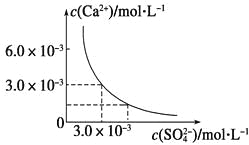
A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活密切相关。下列说法错误的是 ( )
A.使用医用酒精杀菌消毒的过程中只发生了物理变化
B.医用口罩无纺布的原材料成分之一是聚丙烯,其结构简式为![]()
C.疫苗一般应冷藏存放,以避免蛋白质变性
D.医用防护服的核心材料是微孔聚四氟乙烯薄膜,其单体四氟乙烯属于卤代烃
查看答案和解析>>
科目: 来源: 题型:
【题目】浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( )
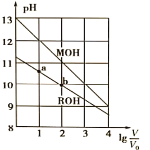
A. MOH的碱性强于ROH的碱性
B. ROH的电离程度:b点大于a点
C. 若两溶液无限稀释,则它们的c(OH-)相等
D. 当![]() =2时,若两溶液同时升高温度,则
=2时,若两溶液同时升高温度,则![]() 增大
增大
查看答案和解析>>
科目: 来源: 题型:
【题目】在室温下,下列五种溶液:①0.1mol/L NH4Cl②0.1mol/L CH3COONH4 ③0.1mol/LNH4HSO4④0.1mol/L NH3H2O和0.1mol/L NH4Cl混合液 ⑤0.1mol/L NH3H2O。
请根据要求填写下列空白:
(1)溶液①呈_____性(填“酸”、“碱”或“中”),其原因是________(用离子方程式表示)。
(2)比较②③溶液中,c(NH4+)的大小关系是②______③(填“>”“<”或“=”)。
(3)在溶液④中,_____ 离子的浓度为0.1mol/L;NH3H2O和_____离子的物质的量浓度之和为0.2mol/L。
(4)室温下,测得溶液②的pH=7,则CH3COO-的水解程度_____(填“>”“<”或“=”)NH4+-的水解程度。CH3COO-与NH4+浓度的大小关系是:c(CH3COO-)_____c(NH4+)(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】银是一种在工业、生活上有广泛用途的金属。
已知:①金属在水中存在如下溶解平衡过程:M![]() Mx+ + xe-,
Mx+ + xe-,
氢气在水溶液中也存在如下平衡过程:H2![]() 2H++ 2e-
2H++ 2e-
②Ag2S 的Ksp=6.7×10-50; AgCl的Ksp=1.6×10-10
据此回答下列有关问题:
(1)银质餐具可杀菌消毒,原因是_________________(用适当的方程式和文字表述说明);金属银与氢硫酸可反应生成黑色固体和无色气体,写出该反应的化学方程式_______________
(2)金属银与硝酸银溶液组成电池示意图如右,a电极的反应为________________,NO3-从电池________侧溶液向电池_______侧溶液移动 (填“左”或“右”)。
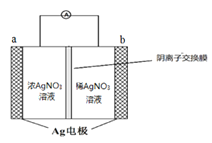
(3)硝酸银见光或受热易分解为Ag、NO2、O2,反应中生成NO2、O2的 物质的量之比为___________,将混合气体通过水吸收后,剩余气体为________________
(4)已知:Ag+(aq) + 2NH3H2O(aq)![]() [Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式________________________;计算该反应的平衡常数K=___________。在氯化银溶于氨水后的溶液中滴加稀硝酸,会再产生白色氯化银沉淀,滴加硝酸至刚好沉淀完全,取上层清液测其pH,发现呈酸性,主要原因是_______________(用离子方程式表示)。
[Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式________________________;计算该反应的平衡常数K=___________。在氯化银溶于氨水后的溶液中滴加稀硝酸,会再产生白色氯化银沉淀,滴加硝酸至刚好沉淀完全,取上层清液测其pH,发现呈酸性,主要原因是_______________(用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】A物质是由茶叶中一种有机物衍变而来。已知:
①A物质氢原子核磁共振谱有6种。
②H结构简式为: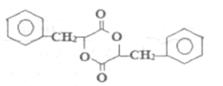
它们的关系如下:
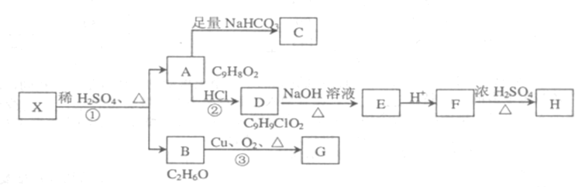
请回答下列问题:
(1)有机物X的结构简式为_______
(2)指出反应①、②、③的反应类型:①______② ______③______。
(3)写出下列反应的化学方程式(有机物写结构简式)
①D—E:_____________
②F在浓硫酸加热条件下发生缩聚反应的化学方程式:____________
(4)写出所有符合下列条件的A的同分异构体的结构简式:__________
①苯环上只有一个取代基
②能发生水解反应
③能与银氨溶液发生反应
查看答案和解析>>
科目: 来源: 题型:
【题目】用中和滴定法测定某烧碱样品的纯度。有以下步骤:
(1)配制待测液:用5.00 g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000 mL溶液。除了烧杯外,还需要的玻璃仪器有_____________ 、____________、和_____________。
(2)滴定:
①盛装0.1000 mol·L-1盐酸标准液应该使用_______________式滴定管。
②滴定时眼睛应________.
③有关数据记录如下:
测定序号 | 待测溶液的体积/mL | 所耗盐酸标准液的体积/mL | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.50 | 20.50 |
2 | 20.00 | 1.20 | 21.20 |
(3)计算纯度:烧碱样品的纯度是_______。
(4)误差分析(填“偏高”,“偏低”,或“无影响”)
a. 酸式滴定管用蒸馏水洗后未用标准液润洗,就直接装入标准液,造成测定结果____________。
b、锥形瓶水洗后,又用待测液润洗,,测定结果____________。
c、用碱式滴定管取待测液时,滴定管尖嘴处有气泡未排出就取液入锥形瓶,造成测定结果____________。
d、滴定前,锥形瓶用水洗涤后,锥形瓶中残留水未干燥,造成最终结果___。
e、酸式滴定管,滴定前仰视读数,滴定后平视读数,造成测定结果__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用![]() 溶液分别滴定
溶液分别滴定![]() 溶液和
溶液和![]() 溶液,得到2条滴定曲线,如下图所示:
溶液,得到2条滴定曲线,如下图所示:
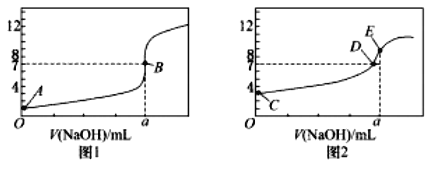
![]() 由A、C点判断,滴定HCl溶液的曲线是_____
由A、C点判断,滴定HCl溶液的曲线是_____![]() 填“图1”或“图2”
填“图1”或“图2”![]() ;
;
![]()
![]() ____
____![]() ;
;
![]()
![]() 的点是_________;
的点是_________;
![]() 点对应离子浓度由大到小的顺序为___________________________。
点对应离子浓度由大到小的顺序为___________________________。
![]() 当NaOH溶液滴定
当NaOH溶液滴定![]() 溶液过程中,NaOH溶液消耗了
溶液过程中,NaOH溶液消耗了![]() mL时,则此时混合液中
mL时,则此时混合液中![]() ____c
____c![]() “
“![]() ”或“
”或“![]() ”或“
”或“![]() ”
”![]() 。
。
![]() 室温时,浓度均为
室温时,浓度均为![]() 的
的![]() 和NaOH的混合液
和NaOH的混合液![]() ,则溶液中
,则溶液中![]() ___________
___________![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com