
科目: 来源: 题型:
【题目】水合草酸晶体的组成可表示为![]() ,为测定x的值,做了如下实验:
,为测定x的值,做了如下实验:
![]() 称取Wg纯草酸晶体,将其配制成100mL水溶液为待测液;
称取Wg纯草酸晶体,将其配制成100mL水溶液为待测液;
![]() 取25mL待测液放入锥形瓶中,再加入适量的稀
取25mL待测液放入锥形瓶中,再加入适量的稀![]() ;
;
![]() 用浓度为a
用浓度为a![]() 的
的![]() 标准溶液进行滴定
标准溶液进行滴定![]() 滴定过程中有
滴定过程中有![]() 、
、![]() 生成
生成![]() 。
。
请回答:(1)写出滴定时发生的反应的离子方程式为:______。
(2)滴定时,将![]() 标准液装在 ______ 式滴定管中。
标准液装在 ______ 式滴定管中。
(3)假设滴定终点时,用去VmL![]() 溶液,则待测草酸溶液的物质的量浓度为 ______
溶液,则待测草酸溶液的物质的量浓度为 ______ ![]() 。
。
(4)在上述实验中,下列操作![]() 其他操作正确
其他操作正确![]() 会造成测定结果x值偏高的有 ______
会造成测定结果x值偏高的有 ______ ![]() 填字母
填字母![]() 。
。
A.滴定终点读数时俯视读数![]() 酸式滴定管使用前,水洗后未用标准液润洗
酸式滴定管使用前,水洗后未用标准液润洗
C.锥形瓶水洗后再用待测液润洗![]() 滴定时所用的
滴定时所用的![]() 溶液因久置而导致浓度变小。
溶液因久置而导致浓度变小。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学上常用AG表示溶液中的lg![]() 。25℃时,用0.100molL-1的NaOH溶液滴定20.00mL 0.100molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
。25℃时,用0.100molL-1的NaOH溶液滴定20.00mL 0.100molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
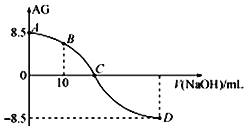
A. D点溶液的pH=11.25
B. C点之前溶液显碱性,C点之后溶液显酸性
C. C点时,加入NaOH溶液的体积为20mL
D. 25℃时,HNO2的电离常数Ka=1.0×10-5.5
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=4的醋酸中:c(H+)= 0.4mol·L-1
B.饱和碳酸氢钠溶液中(已知碳酸氢钠溶液呈碱性):c(Na+)= c(HCO3-)
C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)
D.pH=12的纯碱溶液中:c(OH-)=1.0×10-12mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含NH4+废水和工业废气(主要含NO、CO、CO2、SO2、N2)的流程如图:
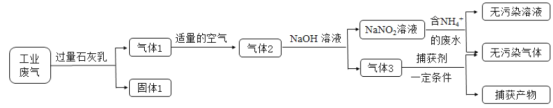
已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体1的主要成分有Ca(OH)2、__________(填化学式)。
(2)若实验室需要配制3 mol·L-1NaOH溶液1L进行模拟测试,需称取NaOH固体质量为__________g。
(3)用NaNO2溶液处理含NH4+废水反应的离子方程式为__________。
(4)验证废水中NH4+已基本除净的方法是___________(写出操作、现象与结论)。
(5)气体1转化为气体2时空气不能过量的原因是__________。
(6)捕获剂捕获的气体主要是__________(填化学式)。
(7)流程中生成的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应,选择生活中常见的物质和有关试剂进行实验,以鉴别NaNO2和NaCl。需选用的物质是__________(填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】对称变换是一种建模方法。依据甲烷的一氯代物只有一种,采用如下代换;

下列说法错误的是
A.a、b、c互为同系物B.X的通式一定为CnH2n+2
C.b的同分异构体只有2种(不含立体异构)D.c的三氯代物只有7种(不含立体异构)
查看答案和解析>>
科目: 来源: 题型:
【题目】某物质可溶于水、乙醇,熔点为209.5℃,其结构简式如图所示。下列说法正确的是( )
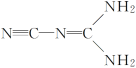
A.该物质为原子晶体
B.该物质分子中σ键和π键的个数比为5∶3
C.该物质分子中每个原子最外层均达到8电子稳定结构
D.该物质分子中含有极性共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】将NO2、O2和熔融KNO3制成燃料电池,电解处理含Cr2O72-的废水。电解过程中发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。下列说法正确的是( )
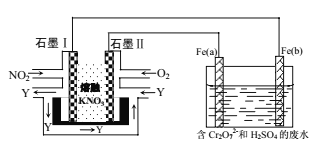
A.石墨Ⅱ是电池的负极
B.若溶液中减少了0.01molCr2O72-,则电路中至少转移了0.12mol电子
C.Fe(a)棒上发生的电极反应为:Fe-3e-=Fe3+
D.在相同条件下,消耗的O2和NO2的体积比为4∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、M、N为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与N分别同主族,在周期表中X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,Z、W的最外层电子数之和与M的核外电子总数相等。试回答下列问题:
![]() 、Z、W、N四种元素的原子半径由大到小的排列顺序是 ______
、Z、W、N四种元素的原子半径由大到小的排列顺序是 ______ ![]() 用元素符号表示
用元素符号表示![]() 。
。
![]() 由X、Z、W、N四种元素中的三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为 ______ 。
由X、Z、W、N四种元素中的三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为 ______ 。
![]() 由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式 ______ 。
由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式 ______ 。
![]() 由X、Z、W、N和Fe五种元素可组成类似明矾的化合物
由X、Z、W、N和Fe五种元素可组成类似明矾的化合物![]() 相对分子质量为
相对分子质量为![]() ,1molH中含有6mol结晶水。对化合物H进行如下实验:
,1molH中含有6mol结晶水。对化合物H进行如下实验:
![]() 取H的溶液,加入过量的NaOH浓溶液并加热,产生白色沉淀和无色有刺激性气味的气体。白色沉淀迅速变为灰绿色,最终变为红褐色;
取H的溶液,加入过量的NaOH浓溶液并加热,产生白色沉淀和无色有刺激性气味的气体。白色沉淀迅速变为灰绿色,最终变为红褐色;
![]() 另取H的溶液,加入过量的
另取H的溶液,加入过量的![]() 溶液产生白色沉淀,加盐酸沉淀不溶解。
溶液产生白色沉淀,加盐酸沉淀不溶解。
![]() 的化学式为 ______ 。
的化学式为 ______ 。
![]() 已知100mL
已知100mL![]() 的H溶液能与20mL
的H溶液能与20mL![]()
![]() 溶液
溶液![]() 硫酸酸化
硫酸酸化![]() 恰好反应,写出该反应的离子方程式______。
恰好反应,写出该反应的离子方程式______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验方案能达到实验目的的是(部分夹持装置已略去)
A. 验证木炭和浓硫酸反应生成CO2
验证木炭和浓硫酸反应生成CO2
B. 实验室制备Fe(OH)2并能较长时间观察到白色固体
实验室制备Fe(OH)2并能较长时间观察到白色固体
C.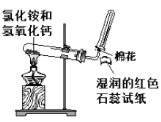 实验室制备和收集氨气并验满
实验室制备和收集氨气并验满
D.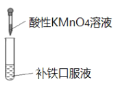 证明补铁口服液中存在+2价的铁
证明补铁口服液中存在+2价的铁
查看答案和解析>>
科目: 来源: 题型:
【题目】中和滴定的误差要求小于0.1%,若用20.00 mL0.2000mol·L-1盐酸滴定20mL0.2000mol·L-1NaOH溶液,则中和滴定曲线中发生突变时的pH范围是(lg2=0.3)( )
A. 4.3~9.7B. 3.7~10.3C. 4.0~10.0D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com