
科目: 来源: 题型:
【题目】化合物F可通过如下路线合成得到:
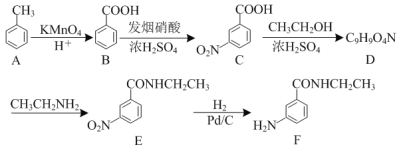
(1)F中的含氧官能团的名称为___。D→E的反应类型为___。
(2)写出D的结构简式:___。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
①含苯环,既能发生银镜反应、也能发生水解反应;
②是一种α-氨基酸,分子中含6种不同化学环境的氢。
(4)已知:苯胺(![]() )有弱碱性、易被氧化。写出以
)有弱碱性、易被氧化。写出以![]() 和CH3CH2OH为原料制备
和CH3CH2OH为原料制备 的合成路线流程图___(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图___(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目: 来源: 题型:
【题目】不同价态氯(或卤素)的归中或歧化反应,试写出下列反应的离子方程式。
(1)次氯酸钠与盐酸反应:________________________。
(2)酸化NaIO3和NaI的混合溶液:_____________________。
(3)氯气通入热的氢氧化钾溶液(生成物中检测出含有氯酸钾):_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1 ℃和T2 ℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )
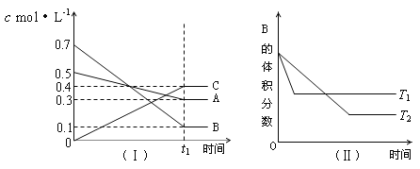
A.该平衡体系的化学反应方程式为:A(g)+B(g)![]() C(g)
C(g)
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
C.T1<T2
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于水溶液中的离子平衡问题叙述正确的是( )
A.将10mL0.1mol·L-1盐酸加入到10mL0.1mol·L-1碳酸钠溶液中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-)
B.0.02mol·L-1HCN溶液与0.02mol·L-1NaCN溶液等体积混合:c(HCN)+c(CN-)=0.04mol·L-1
C.等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH4+) 由大到小的顺序是:①=②>③>④
D.向0.01mol·L-1醋酸溶液中加水,稀释后溶液中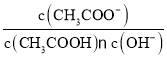 比值增大(忽略稀释过程中溶液温度变化)
比值增大(忽略稀释过程中溶液温度变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】请补充完成下列方程式![]() 配平或按要求写方程式
配平或按要求写方程式![]()
(1)______NH3+_________O2=___________NO+____________H2O
(2)_____________NO2+____________NaOH=____________NaNO2+____________NaNO3+________H2O
(3)____________Fe(OH)3+____________OH-+____________Cl2=____________FeO42-+____________Cl-+____________H2O
(4)___________Cu(IO3)2+____________KI+____________H2SO4=____________CuI↓+____________I2+____________K2SO4+___________H2O
(5)_______MnO4-+_______C2O42-+_______=_______Mn2++_______CO2↑+______________
(6)NaAlH4是一种重要的还原剂,它与水发生氧化还原反应的化学方程式是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为更有效处理工业废气中排放的氮氧化物(NOx)、SO2等,减少大气污染。科学家不断对相关反应进行研究尝试。
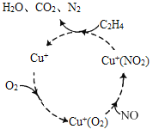
(1)脱硝反应机理如图,Cu+的作用是___,C2H4参与的反应方程式__。
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g);ΔH=-1627kJmol-1
4N2(g)+6H2O(g);ΔH=-1627kJmol-1
①该方法应控制反应温度在315~400℃之间,反应温度不宜过高的原因是__。
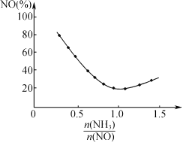
②氨氮比n(NH3)/n(NO)![]() 会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当
会直接影响该方法的脱硝率。如图为350℃时,只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当![]() >1.0时,烟气中NO含量反而增大,主要原因是___。
>1.0时,烟气中NO含量反而增大,主要原因是___。
(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点。ClO2及NaClO2均是性能优良的脱硫脱硝试剂。
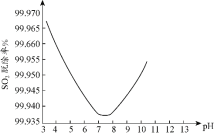
某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是___;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】苯环结构中不存在碳碳单键与碳碳双键交替的结构,下列可以作为证据的是( )
①苯不能使溴的四氯化碳溶液褪色
②苯在一定条件下既能发生取代反应,又能发生加成反应
③经测定,邻二甲苯只有一种结构
④经测定,苯环上碳碳键的键长相等,都是![]()
A.仅①B.仅①②C.仅①②④D.仅①③④
查看答案和解析>>
科目: 来源: 题型:
【题目】Co2O3常用于作氧化剂,在生产中有重要应用。
(1)一定条件下,0.996gCo2O3与15.00mL0.1mol·L-1的Na2S2O3溶液恰好完全反应,生成Co2+和一种含硫物质,该含硫物质中硫元素的化合价是___。
(2)Co2O3、PbO2、KMnO4均可与浓盐酸反应生成Cl2,同时分别生成Co2+、Pb2+和Mn2+。若生成等物质的量的Cl2,所需Co2O3、PbO2和KMnO4的物质的量之比为___。
(3)为测定某Co2O3样品中Co2O3的纯度(杂质不参与反应),现进行如下实验:
步骤1:称取样品2.000g于锥形瓶中,加入足量硫酸和50mL0.5000mol·L-1FeSO4溶液充分反应。
步骤2:向步骤1所得溶液中逐滴滴加0.0500mol·L-1KMnO4标准溶液至终点,消耗KMnO4标准溶液的体积为20.00mL。
已知步骤1、2中所涉及物质的转化分别为:Co3+![]() Co2+、MnO
Co2+、MnO![]()
![]() Mn2+
Mn2+
通过计算确定Co2O3样品中Co2O3的质量分数___(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙醇是重要的有机化工原料,可由乙烯直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H)。再水解生成乙醇。乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的与间接水合法相比,气相直接水合法的优点是:___。
(2)如图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O)︰n(C2H4)=1︰1)
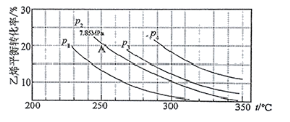
①图中压强P1、P2、P3、P4的大小顺序为:___,理由是:___。
②气相直接水合法党采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9MPa,n(H2O)︰n(C2H4)=0.6︰1。乙烯的转化率为5℅。若要进一步提高乙烯的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有:___、___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com