
科目: 来源: 题型:
【题目】如图所示的各图中,表示2A(g)+B(g)2C(g)(△H<0)这个可逆反应的正确图象为(注:(C)表示C的质量分数,P表示气体压强,C表示浓度)
A.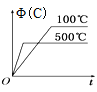 B.
B.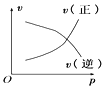 C.
C.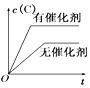 D.
D.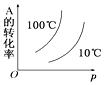
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应![]() △H=+802kJ/mol,如图为在恒温、光照、不同初始浓度和不同催化剂
△H=+802kJ/mol,如图为在恒温、光照、不同初始浓度和不同催化剂![]() Ⅰ、Ⅱ
Ⅰ、Ⅱ![]() 作用下,体积为2L的密闭容器中
作用下,体积为2L的密闭容器中![]() 随光照时间的变化曲线。根据所给信息可得出的结论
随光照时间的变化曲线。根据所给信息可得出的结论

A.对于Ⅰ,![]() ,υ(H2O)=0.015mol mol·L-1·h-1
,υ(H2O)=0.015mol mol·L-1·h-1
B.![]() ,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
,催化剂Ⅱ的催化效果比催化剂Ⅰ效果好
C.![]() ,使用催化剂Ⅰ吸出的热量多于催化剂Ⅱ
,使用催化剂Ⅰ吸出的热量多于催化剂Ⅱ
D.a点时,二氧化碳的转化率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】中华传统文化蕴含着很多化学科学知识,下列说法不正确的是
A.“丹砂(HgS)烧之成水银,积变又还成丹砂”描述的是可逆反应
B.“水声冰下咽,沙路雪中平”未涉及化学变化
C.“烈火焚烧若等闲”涉及的反应在高温下自发进行
D.“洪炉照破夜沉沉”中涉及的反应是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务
[实验目的]制取乙酸乙酯
[实验原理]甲、乙、丙三位同学均采取乙醇、乙酸与浓H2SO4混合共热的方法制取乙酸乙酯,反应的方程式为______________________________________该反应类型______________其中浓H2SO4的作用是_________________和_________________
[装置设计]甲、乙、丙三位同学分别设计下列三套实验装置
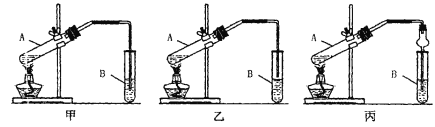
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是__________(选填“甲”或“乙”),丙同学将甲装置中的玻璃管改成球形干燥管,除起冷凝作用外,另一重要作用是_____________
[实验步骤]①按我选择的装置仪器,在试管中先加入3mL乙醇,并在摇动下缓缓加入2mL浓H2SO4 充分摇匀,冷却后再加入2mL冰醋酸;②将试管固定在铁架台上;③在试管B中加入适量的饱和Na2CO3溶液;④用酒精灯对试管A加热;⑤当观察到试管B中有明显现象时停止实验。
[问题讨论]
(1)步骤①装好实验装置,加入样品前还应检查_________________
(2)试管B中饱和Na2CO3溶液的作用是_________________________
(3)从试管B中分离出乙酸乙酯的实验操作是__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。
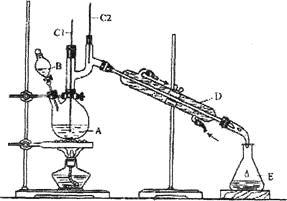
发生的反应如下:
CH3CH2CH2CH2OH![]() CH3CH2CH2CHO
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm﹣3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。在A中加入4.0g正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g。回答下列问题:
(1)上述装置图中,B仪器的名称是__________,D仪器的名称是__________;
(2)加入沸石的作用是__________;
(3)分液漏斗使用前必须进行的操作是__________ (填正确答案标号);
a.润湿 b.干燥 c.检漏 d.标定
(4)将正丁醛粗产品置于分液漏斗中分水时,水在__________层(填“上”或“下”);
(5)反应温度应保持在90~95℃。其原因是______________________________;
(6)本实验中,正丁醛的产率为__________%。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如表所示:
元素编号 | 元素性质或原子结构 |
T | M层上电子数是K层上电子数的3倍 |
X | 最外层电子数是次外电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素X位于元素周期表的第________周期______族;
(2)元素Y的原子结构示意图为________。
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________(填序号)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为_______,基态Cu3+的核外电子排布式为____________。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A.V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为___________;碳原子的杂化方式有_______。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为________________。
②H2O的VSEPR模型为___________,比较键角的大小:H2O_______CH4(填“>”“<”或“=”),原因为___________________________________。
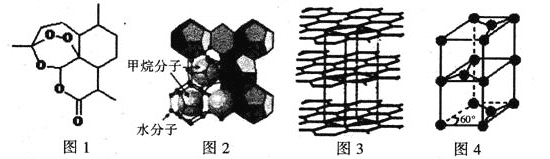
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有__________个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为_________________g·cm-3(列出计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】等质量的碳酸钙与过量的盐酸在不同的实验条件下进行反应,测得在不同时间(t)内产生气体体积(V)的数据如下图所示,根据图示分析实验条件,下列说法中一定不正确的是( )
组别 | 对应曲线 | c(HCl) / mol·L-1 | 反应温度 / ℃ | 铁的状态 | |
1 | a | 30 | 粉末状 | ||
2 | b | 30 | 粉末状 | ||
3 | c | 2.5 | 块状 | ||
4 | d | 2.5 | 30 | 块状 |
A. 第4组实验的反应速率最慢
B. 第1组实验中盐酸的浓度可能最大
C. 第2组实验中盐酸浓度可能等于2.5mol/L
D. 第3组实验的反应温度低于30 ℃
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温恒容装置中发生如下反应:A(g)+2B(g)![]() 2C(g) ΔH = -a kJ·mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如下图所示。下列说法正确是
2C(g) ΔH = -a kJ·mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如下图所示。下列说法正确是

A. 反应放出的热量一定小于a kJ
B. 5s后,反应停止,各物质浓度保持不变
C. 5s末,ν(A)︰ν(B)=1︰2
D. 阴影部分面积可以表示A的物质的量浓度减少量
查看答案和解析>>
科目: 来源: 题型:
【题目】四氯化锡![]() 是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
是一种重要的化工产品。某兴趣小组拟制备四氯化锡。
I.(查阅资料)
物质 | 熔点 | 沸点 | 化学性质 |
Sn | 231 | 227 | 加热时与 |
| 246 | 652 |
|
|
| 114 | 极易水解 |
Ⅱ![]() (制备产品)
(制备产品)
实验装置如图所示![]() 省略夹持和加热装置
省略夹持和加热装置![]()
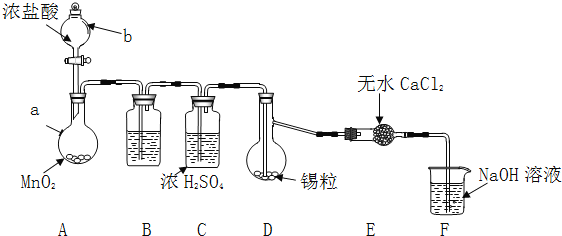
实验步骤:
(1)检查装置气密性后,按图示加入试剂.仪器b的名称是 ______ ,其中无水![]() 的作用是 ______ ,B中的试剂是 ______
的作用是 ______ ,B中的试剂是 ______ ![]() 选填下列字母编号
选填下列字母编号![]() 。
。
A.![]() 溶液
溶液 ![]() 溶液
溶液
![]() 饱和NaCl溶液
饱和NaCl溶液 ![]() 溶液
溶液
(2)先向A中烧瓶内加入盐酸并加热a,当整个装置 ______ 后![]() 填实验现象
填实验现象![]() ,再加热熔化锡粒,反应完后,停止加热。
,再加热熔化锡粒,反应完后,停止加热。
(3)待反应结束后,经 ______ ![]() 填写操作名称
填写操作名称![]() 、洗涤、干燥,可回收利用装置A中未反应完的
、洗涤、干燥,可回收利用装置A中未反应完的![]() 。
。
Ⅲ![]() 探究与反思
探究与反思![]()
(1)装置F中吸收![]() 发生反应的离子方程式是 ______ 。
发生反应的离子方程式是 ______ 。
(2)实验在D中得到的产品很少,经分析装置设计有缺陷,应在D和E之间补充 ______ ![]() 填装置名称
填装置名称![]() 。
。
(3)为验证产品中是否含有![]() ,该小组设计了以下实验方案:
,该小组设计了以下实验方案:![]() 所需试剂从稀
所需试剂从稀![]() 、稀HCl、
、稀HCl、![]() 溶液、
溶液、![]() 溶液、KSCN溶液、蒸馏水中选择
溶液、KSCN溶液、蒸馏水中选择![]()
取适量![]() 产品溶入20mL蒸馏水中,加入 ______ ,若 ______
产品溶入20mL蒸馏水中,加入 ______ ,若 ______ ![]() 填实验现象
填实验现象![]() ,则含有
,则含有![]() ,否则无
,否则无![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com