
科目: 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4),也称为保险粉,Na2S2O4易溶于水,难溶于乙醇,具有极强的还原性,易被空气氧化,在碱性介质中稳定。其阴离子的结构如图所示: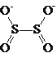 。某科研小组制备并探究其性质。
。某科研小组制备并探究其性质。
Ⅰ.制备Na2S2O4(加热等辅助仪器略去)
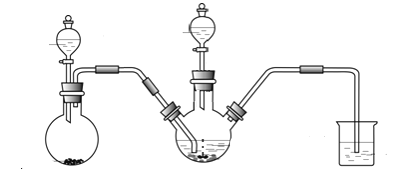
(1)Na2S2O4中硫元素的化合价为_______。
(2)连接好装置后,检查其气密性良好的操作是____________________。
(3)添加药品、再次连接好装置:
①第一步,将A中生成的气体通往B中进行反应,在B装置生成连二亚硫酸锌的化合反应方程式为__________;
②第二步,加入NaOH溶液,于28~35℃下反应生成Na2S2O4,该步反应的离子方程式为_____________。
第三步,将第二步的混合物过滤,并向滤液中加入固体NaCl,冷却至20℃,便有Na2S2O4晶体析出。
③第四步,将第三步所得混合物经________(填操作名称)、________(填写 “水”或“乙醇”)洗涤,得到纯净的Na2S2O4晶体。
(4)装置C的作用是 _______________。
Ⅱ.探究Na2S2O4的稳定性
(5)隔绝空气加热Na2S2O4固体完全分解得到固体产物Na2SO3、Na2S2O3和SO2,但科研小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是______________。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液、KMnO4溶液)
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列反应进行判断,下列各微粒氧化能力由强到弱的顺序正确的是( )
①ClO3-+5Cl-+6H+=3Cl2+3H2O ②2FeCl3+2KI=2FeCl2+2KCl+I2 ③2FeCl2+Cl2=2FeCl3
A.ClO3- >Cl2 >I2 >Fe3+B.Cl2> ClO3- >I2 >Fe3+
C.ClO3- >Cl2 >Fe3+ >I2D.ClO3- >Fe3+ >Cl2 >I2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学用语的表述正确的( )
A. 醋酸的电离方程式:CH3COOH= CH3COO-+H+
B. H216O、H218O互为同位素
C. 质子数为53,中子数为78的碘原子:13153I
D. 氯离子的结构示意图:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素 X、Y、Z 组成的化合物 Y2X 和 ZX2。Y2X 溶于水形成的溶液能与 ZX2 反应生成一种化合物 Y2ZX3。已知三种元素原子的质子总数为 25,且 Z 和 Y 的原子序数之和比 X 的 原子序数2倍还多 1,Z 原子有2个电子层,最外层电子数是核外电子数的 2/3 倍,试回答:
(1)Y 元素在元素周期表中的位置_____。
(2)Y2X 对应水化物的电子式_____。
(3)X 的氢化物比同主族的氢化物的熔沸点明显偏高的原因_____。
(4)X、Y 两种元素还可以形成除 Y2X 之外的另一种化合物,试用电子式表示该物质的形成 过程_________,该化合物与 1mol ZX2完全反应,则反应中电子转移的数目 为_____。(用 NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目: 来源: 题型:
【题目】氟及其化合物用途非常广泛。回答下列问题:
(1)基态F原子的价层电子的轨道表达式为____。
(2)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为_____,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_____和_____(各举一例)。
(3)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。![]() 中中心原子的杂化类型是_____;氟化铵中存在的化学键是_____(填字母)。
中中心原子的杂化类型是_____;氟化铵中存在的化学键是_____(填字母)。
A.离子键 B.σ键 C.π键 D.氢键
(4)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为____kJ·mol-1,S-F键的键能为____kJ·mol-1。
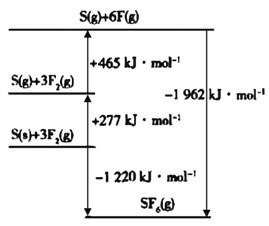
查看答案和解析>>
科目: 来源: 题型:
【题目】钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是
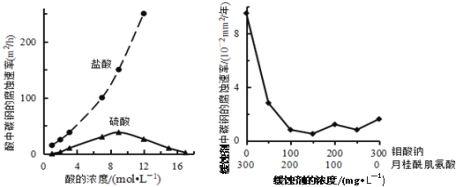
A. 盐酸的浓度越大,腐蚀速率越快
B. 钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小
C. 碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比
D. 对比盐酸和硫酸两条曲线,可知Cl—也会影响碳素钢的腐蚀速率
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关图像,其中说法正确的是

A. 由图Ⅰ知,反应在 T1、T3 处达到平衡
B. 由图Ⅰ知,该反应的△H<0
C. 由图Ⅱ知,t3时采取降低反应温度的措施
D. 由图Ⅱ知,反应在 t6时,NH3 体积分数最大
查看答案和解析>>
科目: 来源: 题型:
【题目】向含有0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为8.96 L(0 ℃,1.01×105Pa)时立即停止,则这一过程中,溶液中离子的物质的量与通入CO2气体的体积关系图像正确的是(气体的溶解和离子的水解忽略不计)( )。
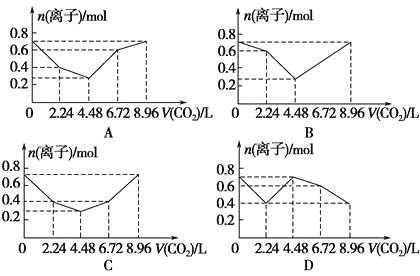
查看答案和解析>>
科目: 来源: 题型:
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构与H2O2类似,熔点为193K,沸点为411K,遇水很容易水解,产生的气体能使品红褪色,S2Cl2可由干燥氯气通入熔融的硫中制得。下列有关说法正确的是
A. S2Cl2的电子式为![]()
B. 固态时S2Cl2属于原子晶体
C. S2Cl2与NaOH的化学方程式可能为:S2Cl2+6NaOH=2NaCl+Na2SO3+Na2S+3H2O
D. S2Cl2是含有极性键和非极性键的离子化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】多硫化钠Na2Sx(x≥2)在NaOH溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16.Na2Sx在结构上与Na2O2相似.则下列有关说法正确的是( )
A.该反应中Na2Sx是氧化剂,NaClO是还原剂
B.Na2Sx含有离子键和极性共价键
C.1molNa2Sx参加反应,有32mol电子转移
D.Na2Sx中的x数值为2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com