
科目: 来源: 题型:
【题目】有一包白色粉末,其中可能含有KCl、Ba(NO3)2、CuSO4、Na2CO3,现通过以下实验流程进行检验(假设物质间的反应恰好完全)。回答下列问题:

(1)白色粉末中一定没有的物质是_____________(填化学式,下同)。
(2)无色溶液1中一定含有的溶质___________,是可能含有的溶质是___________。
(3)生成无色气体的化学方程式为__________________________________;该反应属于____________(填反应基本类型).
(4)生成白色沉淀b的离子方程式为__________________________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化硫—空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。下列说法错误的是( )

A.Pt1 附近的电极反应式为 SO2+2H2O2e═2H2SO4
B.Pt2 附近的电极反应式为 O2+4H++4e═2H2O
C.该电池放电时电子从 Pt1 电极经过外电路流到 Pt2 电极
D.相同条件下,放电过程中消耗的 SO2 和 O2 的体积比为 2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00 mL 0.049 mol·L-1羟胺的酸性溶液与足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.55 mL 0.020 mol·L-1酸性KMnO4溶液完全反应。已知(未配平):FeSO4+KMnO4+H2SO4 → Fe2(SO4)+K2SO4+MnSO4+H2O,则羟胺的氧化产物是
A. N2 B. N2O C. NO D. NO2
查看答案和解析>>
科目: 来源: 题型:
【题目】0.1 mol·L-1氨水10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是( )
①电离程度增大 ②c(NH3·H2O)增大 ③NH![]() 数目增多 ④c(OH-)增大 ⑤导电性增强
数目增多 ④c(OH-)增大 ⑤导电性增强
A.①②③ B.①③⑤ C.①③ D.②④
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室欲利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5mol﹒L-1的碳酸钠溶液1000mL。回答下列问题
(1)需要称量碳酸钠晶体的质量为___________g,所选用容量瓶的规格为___________ mL。
(2)洗涤操作中,将洗涤烧杯后的溶液也注入容量瓶,其目的是__________________________________。
(3)定容的正确操作是继续加蒸馏水至离刻度线下1~2cm时,改用_________加水至液面与刻度线相切。
(4)用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是__________(填字母)。
a.重新配制
b.吸出多余液体,使凹液面与刻度线相切
c.经计算加入一定量的碳酸钠晶体
d.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
(5)配制时下列操作会导致所配溶液浓度偏高的是_____________(填字母)。
a.转传移时有少量溶液溅出
b.定容时俯视读取刻度
c.容量瓶用蒸馏水洗净后未干燥
d.定容时液面超过了刻度线
(6)从上述配制的溶液中取出10mL,其中含Na2CO3的质量是_____________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组研究SO2与Na2O2的反应。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有______性,SO2与Na2O2反应生成Na2SO4。
(2)用下图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是______。
②B中的试剂为______,其主要作用是干燥SO2。
③能证明假设1成立的实验现象是______。
(3)为检验C中是否有Na2SO4生成,设计如下方案:
取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。
该方案是否合理?______(填“合理”或“不合理”)。请简要说明理由:______。
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4。从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的______(只写一条)有关。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,Na2CO3 溶液存在水解平衡:CO32-+H2O![]() HCO3-+OH-。下列说法正确的是()
HCO3-+OH-。下列说法正确的是()
A.加入 NaOH 固体,溶液 pH 减小
B.稀释溶液,水解平衡常数增大
C.升高温度,![]() 减小
减小
D.加入 CaCl2 固体,平衡向逆反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】柠檬烯是一种食用香料,其结构简式如图所示,下列有关柠檬烯的说法正确的是( )

A.它的一氯代物有 7 种
B.它与足量氢气反应后生成的分子中所有的碳原子可能在同一平面上
C.它与足量的溴水反应后,产物的化学式为:C10H14Br4
D.一定条件下,它可以发生加成、取代、氧化等反应
查看答案和解析>>
科目: 来源: 题型:
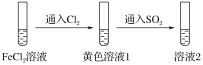
【题目】为验证还原性:SO2>Fe2+>Cl-,三组同学分别进行了下图实验,并对溶液1和溶液2中所含离子进行了检验,能证明上述还原性顺序的实验组有( )
溶液1 | 溶液2 | |
甲 | 含Fe3+、Fe2+ | 含SO |
乙 | 含Fe3+,无Fe2+ | 含SO |
丙 | 含Fe3+,无Fe2+ | 含Fe2+ |
A.只有甲B.甲、乙
C.甲、丙D.甲、乙、丙
查看答案和解析>>
科目: 来源: 题型:
【题目】研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
NaNO3(s)+ClNO(g) K1 ΔH1<0(Ⅰ)
2NO(g)+Cl2(g)![]() 2ClNO(g) K2 ΔH2<0 (Ⅱ)
2ClNO(g) K2 ΔH2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________(用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得平衡后n(Cl2)=2.5×10-2 mol,10 min内υ(ClNO)=________________,则NO的转化率α1=________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2 ________α1(填“>”、“<”或“=”),
(3)氨气是工业制硝酸的主要原料之一,催化氧化步骤中发生的主要反应如下:
I. 4NH3(g) + 5O2(g)![]() 4NO(g) + 6H2O(g) △H =-906 kJ·mol-1
4NO(g) + 6H2O(g) △H =-906 kJ·mol-1
II.4NH3(g) + 3O2(g) 2N2(g) + 6H2O(g) △H = -1266 kJ·mol-1
在1L的密闭容器中充入1 mol NH3和2 mol O2,测得有关物质的物质的量与反应温度的关系如图所示。

①催化氧化步骤中,最适宜的温度为_________________(填“T1”或“T2” 或“T3”)
②写出N2和O2生成NO的热化学方程式________。
③温度为T2时,反应II的平衡常数K =_________________(只列算式)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com