
科目: 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为 C6H6的结构有多种,其中的两种为:
Ⅰ.![]() Ⅱ.
Ⅱ.
(1)这两种结构的化学性质区别表现在:Ⅰ不能____(填字母,下同),而Ⅱ能____。
A.被酸性KMnO4溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)已知Ⅰ结构下,该物质能在一定条件下与液溴反应,其反应方程式为________________。
(3)今发现C6H6还可能有另一种如下图所示的立体结构,该结构的四氯代物有______种。
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向10mL0.1mol·L-1CuCl2溶液中滴入0.1ml·L-1的Na2S溶液,滴加过程中溶液中-1gc(Cu2+)随滴人的Na2S溶液体积的变化如图所示。下列叙述正确的是
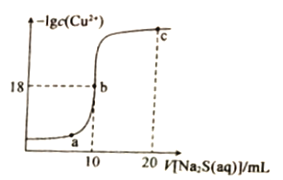
A. Na2S溶液中:c(S2-)+c(HS-)+c(H2S)==2c(Na+)
B. Ksp(CuS)的数量级为10-36
C. a、b、c三点溶液中,b点水的电离程度最大
D. c点溶液中:c(C1-)=2c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.1 mol·L-1的盐酸和25.00 mL 0.1 mol·L-1氨水混合。
(1)当加入10.00 mL稀盐酸时,溶液中的溶质是________(填化学式),溶液的pH______(填“>”、“<”或“=”)7。
(2)当某一时刻溶液中c(NH4+)=c(Cl-),此时溶液的pH____(填“>”、“<”或“=”)7。所加的盐酸体积V ____(填“>”、“<”或“=”)25.00 mL。其原因是_______。
(3)某一时刻溶液中会不会存在:c(Cl-)>c(NH4+),且c(OH-)>c(H+)的关系?_____(填“会”或“不会”)。其原因是________。
(4)已知常温时 ,K(NH3·H2O)=1.8×10-5 当V(HCl)=12.50 mL时,下列离子浓度的大小关系是: c(Cl-) ___ c(NH4+) ,c(OH-) ___ c(H+)。(填“>”、“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
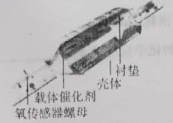
【题目】某种 “全氢电池”的工作原理如图所示。下列说法错误的是( )

A.右边吸附层中发生了氧化反应
B.负极的电极反应是H2-2e-+2OH-===2H2O
C.该电池总反应是H++OH-===H2O
D.电解质溶液中Na+向右移动、ClO4-向左移动
查看答案和解析>>
科目: 来源: 题型:
【题目】I、下图为汽车尾气处理系统中“三元催化”的工作原理,NO和CO在催化剂作用下生成无污染性物质的方程式2NO+2CO![]() N2+2CO2。
N2+2CO2。
某课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验。
实验编号 | 实验目的 | T/℃ | NO初始浓度/mol·L-1 | CO初始浓度/mol·L-1 | 同种催化剂的比表面积/m2·g-1 | c(CO)不变时所用的时间/min |
① | 参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
② | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
③ | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
(1)实验编号②的实验目的为_______。
(2)课题中探究外界条件对汽车尾气转化反应速率的影响的另一因素是________。
II、某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
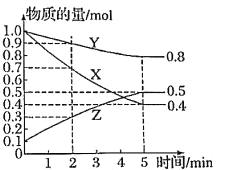
(1)该反应的化学方程式是______。
(2)该反应达到平衡状态的标志是
A. Y的体积分数在混合气体中保持不变
B. X、Y的反应速率比为3:1
C. 容器内气体压强保持不变
D. 容器内气体的总质量保持不变
E. 生成1 mol Y的同时消耗2 mol Z
(3)2~5min内用X表示的化学反应速率为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组的同学根据“侯氏制碱法”的原理:
①NH3+H2O+CO2+NaCl===NaHCO3↓+NH4Cl
②2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
利用如下实验装置制备Na2CO3。
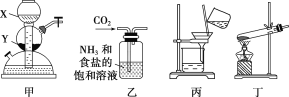
下列叙述正确的是( )
A.若X为稀硫酸,Y为碳酸钙,则可用装置甲制取CO2
B.装置乙中会有白色沉淀析出
C.将装置丙中所得滤液蒸干可得到NH4Cl固体
D.用装置丁加热NaHCO3固体可制得Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】T、W、X、Y、Z为前四周期元素,其原子序数依次增大,有关五种元素的性质或原子结构描述如下:
元素符号 | 元素性质或原子结构 |
T | 其一种无色氧化物遇空气变为红棕色 |
W | 其单质和化合物的焰色反应焰色均呈黄色 |
X | 基态原子的最外层电子排布式为 |
Y | 单质常温下为气体,可用于自来水消毒 |
Z | 一种核素的质量数为56,中子数为30 |
(1)Z元素位于周期表中第_ ______ 族,其基态原子的价层电子排布式为:______ ;
(2)T的一种化合物为![]() ,该分子中极性键和非极性键的数目之比为 ______,T的最低价氢化物与其最高价氧化物的水化物能发生化合反应,其产物属于______ 晶体。
,该分子中极性键和非极性键的数目之比为 ______,T的最低价氢化物与其最高价氧化物的水化物能发生化合反应,其产物属于______ 晶体。
(3)W、X和Y三种元素中,第一电离能最小的为 ______ (填元素符号);W、X和Y的简单离子的半径从小到大的顺序为 ______ (用离子符号表示)。
(4)Z与水蒸气反应的化学方程式为:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物Y具有抗菌、消炎作用,可由X制得。
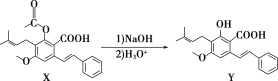
下列有关化合物X、Y的说法正确的是( )
A.1 mol X最多能与2 mol NaOH反应
B.Y与乙醇发生酯化反应可得到X
C.X、Y均能与酸性KMnO4溶液反应
D.室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目不相等
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是一种综合处理SO2废气的工艺流程,若每步都完全反应。下列说法正确的是 ( )

A.溶液B中发生的反应为2SO2+O2=2SO3
B.可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
C.由以上流程可推知氧化性:Fe3+>O2>SO42—
D.此工艺的优点之一是物质能循环利用
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B两个完全相同的装置,某学生分别在它们的侧管中装入![]()
![]() 和
和![]()
![]() ,A、B中分别有10mL相同浓度的盐酸(不考虑盐酸的挥发),将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
,A、B中分别有10mL相同浓度的盐酸(不考虑盐酸的挥发),将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )

A.B装置的气球膨胀的体积大
B.最终两试管中NaCl的物质的量一定相同
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于![]()
D.若最终两气球体积相同,则盐酸的浓度一定大于或等于![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com