
科目: 来源: 题型:
【题目】氮有不同价态的氧化物,如NO、N2O3、NO2等,它们在一定条件下可以相互转化。
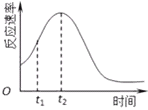
(1)某温度下,在一体积可变的密闭容器中充入1molN2O3,发生反应N2O3NO2(g)+NO(g),达到平衡后,于t1时刻改变某一条件后,速率与时间的变化图象如图1所示,有关说法
正确的是____
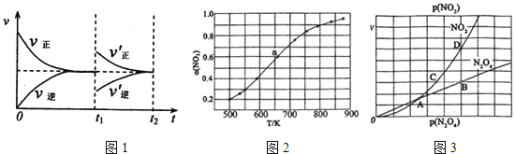
A.t1时刻改变的条件是增大N2O3的浓度,同时减小NO2或NO的浓度
B.t1时刻改变条件后,平衡向正反应方向移动,N2O3的转化率增大
C.在t2时刻达到新的平衡后,NO2的百分含量不变
D.若t1时刻将容器的体积缩小至原容积的一半,则速率~时间图象与上图相同
(2)在1000K下,在某恒容容器中发生下列反应:2NO2(g)2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率α(NO2)随温度变化如图所示。
图2中a点对应温度下。已知NO2的起始压强P0为120kPa,列式计算该温度下反应的平衡常数Kp=______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)对于反应N2O4(g)2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2).其中,k1、k2是与反应及温度有关的常数。相应的速率﹣压强关系如图所示:一定温度下,k1、k2与平衡常数Kp间的关系是k1=_____;在图3标出点中,指出能表示反应达到平衡状态的两个点_____,理由是____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,pH相同的盐酸和氯化铵溶液分别稀释,pH随溶液体积变化的曲线如下图所示。据图判断下列叙述中,正确的是
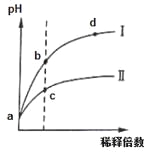
A.Ⅰ为氯化铵稀释时pH值变化曲线,Ⅱ为盐酸稀释时pH值变化曲线
B.b点溶液中水的电离程度比d点溶液中水的电离程度大,但两点的KW相同
C.a点时,等体积的两溶液分别与NaOH反应,消耗的NaOH量相同
D.c点溶液的导电能力一定比b点溶液导电能力强
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某温度时CH3COOH的电离平衡常数为K。该温度下向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,pH变化曲线如图所示(忽略温度),以下叙述正确的是
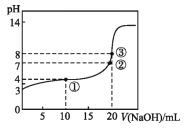
A.根据图中数据可计算出K值约为1×10-5
B.①②③点水的电离程度由大到小的顺序为:②>③>①
C.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
D.点③时c(CH3COOH)+c(CH3COO-)=0.1 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知用硫酸酸化的草酸(H2C2O4)溶液能与KMnO4溶液反应.某化学小组研究发现,少量MnSO4可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下:
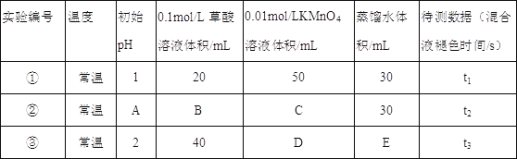
(1)常温下,探究不同的初始pH和草酸溶液浓度对反应速率的影响,设计如下实验,则A=____,C=____,E=_____.
(2)该反应的离子方程式______________________________________.
(3)若t1<t2,则根据实验①和②得到的结论是_____________________________.
(4)小组同学发现每组实验反应速率随时间的变化总是如图,其中t1~t2时间内速率变快的主要原因可能是:①__________________;②__________________________.
(5)化学小组用滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O42H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定三次,平均消耗KMnO4溶液VmL.滴定到达终点的现象是:______________________________;实验中所需的定量仪器有__________________(填仪器名称).该KMnO4溶液的物质的量浓度为____mol/L.
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂的工业废水中含有大量的![]() ,较多的
,较多的![]() 和少量
和少量![]() 为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。
为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜.请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。![]() 可供选择的试剂为铁粉、稀
可供选择的试剂为铁粉、稀![]() 、NaOH溶液等试剂
、NaOH溶液等试剂![]()
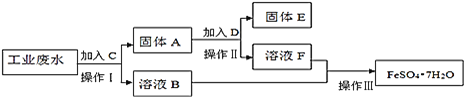
![]() 操作Ⅰ的名称为 ______ ,所需要的玻璃仪器有 ______ ;
操作Ⅰ的名称为 ______ ,所需要的玻璃仪器有 ______ ;
![]() 固体A的成分为 ______ ,溶液B中含有的离子有 ______
固体A的成分为 ______ ,溶液B中含有的离子有 ______
![]() 加入试剂C的目的是 ______ ,发生的化学方程式为 ______ ;
加入试剂C的目的是 ______ ,发生的化学方程式为 ______ ;
![]() 加入的试剂D为 ______ ,发生的离子方程式为 ______ ;
加入的试剂D为 ______ ,发生的离子方程式为 ______ ;
![]() 操作Ⅲ为 ______ 。
操作Ⅲ为 ______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】分支酸用于生化研究,可以由物质A合成.已知:连4个不相同的原子或原子团的碳原子是手性碳原子.
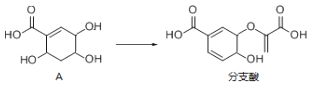
下列叙述不正确的是![]()
A.用![]() 溶液可鉴别化合物A和分支酸
溶液可鉴别化合物A和分支酸
B.化合物A中含有3个手性碳原子
C.1mol分支酸在一定条件下最多可与![]() 发生反应
发生反应
D.在浓硫酸和加热条件下,化合物A可发生消去反应生成多种有机产物
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5流程:
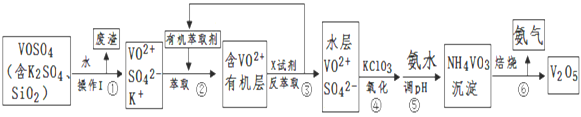
(1)步骤①所得废渣的成分是____________(写化学式),操作I的名称__________;
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n (水层)+ 2nHA(有机层)![]() 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是_____________________________;
③中X试剂为(写化学式)______________________________________;
(3)④的离子方程式为 ___________________________________________;
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为____________;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< _____________;(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有__________和_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】据报道,1996年8月,我国科学家首次制出一种新核素镅—235,已知镅(Am)的原子序数为95,下列关于![]() 的叙述正确的是
的叙述正确的是
A. 镅—235与铀—235具有相同的质子数
B. 镅—235的原子质量是12C原子质量的235倍
C. 镅—235原子核内中子数为140,核外电子数为95
D. 镅—235原子一定不具有放射性
查看答案和解析>>
科目: 来源: 题型:
【题目】侯德榜制碱法生产流程为:
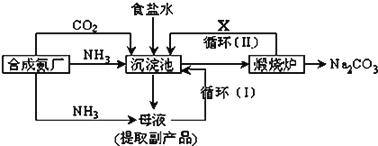
![]() 沉淀池中反应的化学方程式:________________________________;
沉淀池中反应的化学方程式:________________________________;
![]() 检验产品碳酸钠中是否含有氯化钠的操作方法为:___________________________
检验产品碳酸钠中是否含有氯化钠的操作方法为:___________________________
![]() 上述流程中物质X的分子式为 ______
上述流程中物质X的分子式为 ______
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用铝土矿![]() 主要成分为
主要成分为![]() 、
、![]() 、
、![]() 提取氧化铝做冶炼铝的原料,提取的操作流程如下:
提取氧化铝做冶炼铝的原料,提取的操作流程如下:
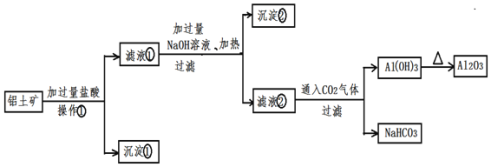
请回答下列问题:
![]() 操作
操作![]() 的名称:______
的名称:______
![]() 沉淀
沉淀![]() 的化学式:______沉淀
的化学式:______沉淀![]() 的化学式:______
的化学式:______
![]() 写出沉淀
写出沉淀![]() 与NaOH溶液反应的化学方程式:______
与NaOH溶液反应的化学方程式:______
![]() 写出滤液
写出滤液![]() 与NaOH溶液反应生成沉淀
与NaOH溶液反应生成沉淀![]() 的离子方程式:______
的离子方程式:______
![]() 尝试写出滤液
尝试写出滤液![]() 中通入
中通入![]() 后的反应方程式:______
后的反应方程式:______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com