
【题目】氮有不同价态的氧化物,如NO、N2O3、NO2等,它们在一定条件下可以相互转化。
(1)某温度下,在一体积可变的密闭容器中充入1molN2O3,发生反应N2O3NO2(g)+NO(g),达到平衡后,于t1时刻改变某一条件后,速率与时间的变化图象如图1所示,有关说法
正确的是____
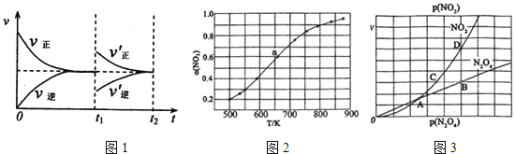
A.t1时刻改变的条件是增大N2O3的浓度,同时减小NO2或NO的浓度
B.t1时刻改变条件后,平衡向正反应方向移动,N2O3的转化率增大
C.在t2时刻达到新的平衡后,NO2的百分含量不变
D.若t1时刻将容器的体积缩小至原容积的一半,则速率~时间图象与上图相同
(2)在1000K下,在某恒容容器中发生下列反应:2NO2(g)2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率α(NO2)随温度变化如图所示。
图2中a点对应温度下。已知NO2的起始压强P0为120kPa,列式计算该温度下反应的平衡常数Kp=______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)对于反应N2O4(g)2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2).其中,k1、k2是与反应及温度有关的常数。相应的速率﹣压强关系如图所示:一定温度下,k1、k2与平衡常数Kp间的关系是k1=_____;在图3标出点中,指出能表示反应达到平衡状态的两个点_____,理由是____________________________。
【答案】C 81kPa ![]() K2Kp B、D N2O4与NO2的消耗速率满足条件v(NO2)=2v(N2O4)
K2Kp B、D N2O4与NO2的消耗速率满足条件v(NO2)=2v(N2O4)
【解析】
(1)利用等效平衡分析;
(2)三行式法计算;
(3)根据平衡常数表达式计算;根据达到化学平衡后,正逆反应速率比等于化学计量数之比判断。
(1)A.由速率与时间的变化图象可知,t1时刻改变某一条件后,反应N2O3(g)NO2(g)+NO(g)正反应速率增大,逆反应速率减小,最后平衡速率与原平衡相等,则改变的条件是增大N2O3的浓度,由于T、P相等,则容器体积增大,导致NO2、NO的浓度减小,但达到新平衡后与原平衡等效,故A错误;
B.t1时刻改变的条件是增大N2O3的浓度,由于T、P相等,则容器体积增大,导致NO2、NO的浓度减小,但达到新平衡后与原平衡等效,N2O3的转化率不变,故B错误;
C.t1时刻改变的条件是增大N2O3的浓度,由于T、P一定,则容器体积增大,导致NO2、NO的浓度减小,但达到新平衡后与原平衡等效,NO2的百分含量不变,故C正确;
D.若t1时刻将容器的体积缩小至原容器的一半,则压强增大,正逆反应速率都增大,所以速率~时间图象与上图不同,故D错误;
答案:C;
(2)图中a点对应温度下,NO2的转化率是0.6,设原来NO2的物质的量为xmol,转化的物质的量为0.6xmol;
2NO2(g) 2NO(g)+O2(g)
开始 x 0 0
转化0.6xmol 0.6xmol 0.3xmol
平衡0.4xmol 0.6xmol 0.3xmol
则混合气体的物质的量=0.4xmol+0.6xmol+0.3xmol=1.3xmol,相同条件下,气体的压强之比等于其物质的量之比,所以反应后压强=![]() ×1.3xmol=156KPa,NO2的分压=156KPa×
×1.3xmol=156KPa,NO2的分压=156KPa×![]() =48KPa,NO的分压=156KPa×
=48KPa,NO的分压=156KPa×![]() =72KPa,O2的分压=156KPa×
=72KPa,O2的分压=156KPa×![]() =36KPa;
=36KPa;
化学平衡常数Kp=![]() =
=![]() =81;
=81;
答案:81;
(3)反应N2O4(g)2NO2(g),则化学平衡常数Kp=![]() ,当二者的反应速率之比等于其计量数之比,反应达到平衡,则v(NO2):v(N2O4)=k2p2(NO2):k1p(N2O4)=2:1,又化学平衡常数Kp==
,当二者的反应速率之比等于其计量数之比,反应达到平衡,则v(NO2):v(N2O4)=k2p2(NO2):k1p(N2O4)=2:1,又化学平衡常数Kp==![]() ,所以K1=
,所以K1=![]() K2Kp,满足平衡条件v(NO2)=2v(N2O4)即为平衡点,B、D点的压强之比等于其反应速率之比为1:2,所以B、D为平衡点;
K2Kp,满足平衡条件v(NO2)=2v(N2O4)即为平衡点,B、D点的压强之比等于其反应速率之比为1:2,所以B、D为平衡点;
答案:![]() K2Kp ;B、D;N2O4与NO2的消耗速率满足条件v(NO2)=2v(N2O4)。
K2Kp ;B、D;N2O4与NO2的消耗速率满足条件v(NO2)=2v(N2O4)。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】一定条件下,向一密闭容器中充入一定量的NH3,反应2NH3(g)![]() N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
N2(g)+3H2(g)达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是

A. 压强:p1>p2
B. b、c两点对应的平衡常数:Kc>Kb
C. a点:2v(NH3)正=3v(H2)逆
D. a点:NH3的转化率为1/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示M的结构简式,下列有关M的说法正确的是

A.M可以发生加成、加聚、水解、酯化等反应
B.1 mol M最多可以与3 mol NaOH反应
C.M苯环上的一氯取代物有两种不同结构
D.1 molM最多可以与5 mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图所示,有关该物质的说法中正确的是![]()
![]()

A.该物质与苯酚属于同系物,遇![]() 溶液呈紫色
溶液呈紫色
B.滴入酸性![]() 溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C.1mol该物质分别与浓溴水和![]() 反应时最多消耗
反应时最多消耗![]() 和
和![]() 分别为4mol和7mol
分别为4mol和7mol
D.该分子中的所有碳原子不可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分支酸用于生化研究,可以由物质A合成.已知:连4个不相同的原子或原子团的碳原子是手性碳原子.
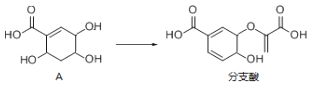
下列叙述不正确的是![]()
A.用![]() 溶液可鉴别化合物A和分支酸
溶液可鉴别化合物A和分支酸
B.化合物A中含有3个手性碳原子
C.1mol分支酸在一定条件下最多可与![]() 发生反应
发生反应
D.在浓硫酸和加热条件下,化合物A可发生消去反应生成多种有机产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图三条曲线表示不同温度下水的离子积常数,下列说法不正确的是
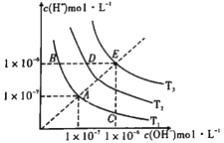
A. 图中温度:T3>T2>T1
B. 图中pH关系是:pH(B)=pH(D)=pH(E)
C. 图中五点Kw间的关系:E>D>A=B=C
D. C点可能是显酸性的盐溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是A、B两种重要的有机合成原料的结构。下列有关说法中正确的是
A. ![]() B.
B.![]()
A.A与B互为同系物
B.A与B都能与溴的四氯化碳溶液发生加成反应
C.在一定条件下,A与B均能发生取代反应
D.1mol B能与4mol![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯的实验装置如图所示(夹持装置已略去)。下列说法不正确的是
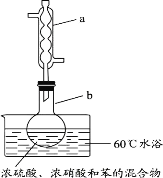
A.水浴加热的优点为使反应物受热均匀、容易控制温度
B.仪器a的作用是冷凝回流,提高原料的利用率
C.浓硫酸、浓硝酸和苯混合时,应先向浓硫酸中缓缓加入浓硝酸,待冷却至室温后,再将苯逐滴滴入
D.反应完全后,可用蒸馏的方法分离苯和硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示。A的摩尔质量为120 g·mol1且只含两种元素。B、E是常见气体,其中B为单质,E能使品红溶液褪色。D为红棕色固体,F为紫红色金属,C的浓溶液可干燥某些气体。

(1)A的化学式为______。
(2)H的电子式为______。
(3)写出反应③的离子方程式:______。
(4)写出反应④的化学方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com