
科目: 来源: 题型:
【题目】如图是元素周期表的框架,请在表中①~⑩元素中回答问题。
① |
|
| |||||||||||||||
|
|
|
|
| ② | ③ | ④ |
| |||||||||
⑤ | ⑥ | ⑦ |
|
|
| ⑧ |
| ||||||||||
⑨ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| ⑩ |
|
请回答下列问题:
(1)元素②的原子结构示意图是___。
(2)在表中④、⑤、⑥三种元素的简单离子半径由小到大的顺序为___(填离子符号)。
(3)其中⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为____。
(4)⑧与⑩两种元素非金属较强的是___(填元素符号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.(化学反应原理)
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

(1)在相同时间内, 两烧杯中产生气泡的速度:甲__乙(填“>”“<”或“=”)。
(2)请写出图中构成原电池的负极电极反应式:__。
II.(化学与生活)
材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
(1)在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点___。(选填“高”或“低”)
(2)石英玻璃纤维又称光导纤维,其主要成分和NaOH溶液反应的化学方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.(化学反应原理)
恒温恒容下,将2mol气体A和2mol气体B通入体积为2L的密闭容器中,发生如下反应:2A(g)+B(g)![]() xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mol/L。
(1)从开始反应到平衡状态,生成C的平均反应速率为___。
(2)该反应的化学平衡表达式为___。
(3)下列各项可作为该反应达到平衡状态的标志是___。
A.压强不再变化 B.气体密度不再变化
C.气体平均相对分子质量不再变化 D.A的消耗速率与B的消耗速率之比为2:1
II.(化学与生活)
有四种常见药物①阿司匹林②青霉素③胃舒平④麻黄碱。请回答:
(1)某同学胃酸过多,应选用的药物是___(填序号)。
(2)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是___(填序号)。
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是___(填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.(化学反应原理)
25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)CH3COOH的电离平衡常数表达式__。
(2)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为__。
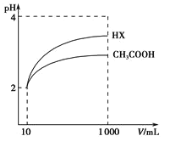
(3)体积均为l00mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___(填“大于”、“小于”或“等于”)醋酸的电离平衡常数。
Ⅱ.(化学与生活)
防治环境污染,改善生态环境已成为全球共识。
(1)燃煤气化有助于减少PM2.5,写出焦炭与水蒸气反应的化学方程式___。
(2)采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾:
A.废纸 B.废电池 C.易拉罐 D.玻璃瓶 E.塑料制品
在焚烧处理前,除废电池外,还有___(填字母)应剔除并回收,随意丢弃电池造成的主要危害是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇![]() 是重要的溶剂和替代燃料,工业上用CO和
是重要的溶剂和替代燃料,工业上用CO和![]() 在一定条件下制备
在一定条件下制备![]() 的反应为:
的反应为:![]() ,在体积为1L的恒容密闭容器中,充人
,在体积为1L的恒容密闭容器中,充人![]() 和
和![]() ,一定条件下发生上述反应,测得
,一定条件下发生上述反应,测得![]() 和
和![]() 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:

![]() 从反应开始至达到平衡,用氢气表示的平均反应速率
从反应开始至达到平衡,用氢气表示的平均反应速率![]() ______
______![]()
![]() 下列说法正确的是______
下列说法正确的是______![]() 填字母序号
填字母序号![]() 。
。
A.达到平衡时,CO的转化率为![]()
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充入氩气,反应速率减小
D.2min前![]() 正
正![]() 逆
逆![]() ,2min后
,2min后![]() 正
正![]() 逆
逆![]()
![]() 该条件下反应的平衡常数
该条件下反应的平衡常数![]() ______。
______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个容积为2L的密闭容器中,加入0.8mol的A2气体和0.6molB2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示。
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示。
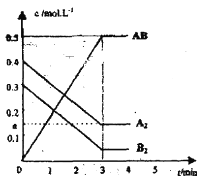
(1)在上述反应达到平衡后,第4min时,若将容器的体积快速扩大一倍(其他条件不变),请在图中画出4min~5min的AB浓度的变化线。____
(2)在相同条件下,若开始时向此容器中加入的A2(g)、B2(g)和AB(g)的物质的量分别为0.4mol、0.2mol、0.8mol。则反应开始时v正____v逆 (填“>”、“<”或“=”)。判断依据是____________________________________________________。反应达到平衡后,各物质的体积分数与原平衡相比____(填序号)
①A2、B2减小,AB增大 ②A2、B2增大,AB减小 ③均不变 ④无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系,则X、W可能的组合有

①C、O2 ②Na、O2 ③Fe、HNO3 ④S、O2 ⑤N2、O2⑥H2S、O2⑦NH3、O2
A. 四项 B. 五项 C. 六项 D. 七项
查看答案和解析>>
科目: 来源: 题型:
【题目】I.(化学反应原理)
(1)在101kPa时,足量H2在1molO2中完全燃烧生成2mol液态水,放出571.6kJ的热量,H2的燃烧热△H=__。
(2)1.00L1.00mol·L-1硫酸与2.00L1.00mol·L-1NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为__。
II.(化学与生活)
保证食品安全、保持营养均衡,是保障人体健康的基础。
(1)维生素C能促进人体生长发育。下列富含维生素C的是___。
A.牛肉 B.辣椒 C.鸡蛋
(2)缺乏某种微量元素将导致甲状腺肿大,且造成智力损害,该微量元素是__。
A.碘 B.铁 C.钙
查看答案和解析>>
科目: 来源: 题型:
【题目】将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转。下列针对该装置的说法正确的是( )

A.将电能转换为化学能
B.电子由铜片流出经导线到锌
C.一段时间后,锌片质量减轻
D.铜片一侧柠檬变蓝色,产生Cu2+
查看答案和解析>>
科目: 来源: 题型:
【题目】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素的基态价电子排布式为_____________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______________,提供孤电子对的成键原子是_____________。
②氨的沸点_________(填“高于”或“低于”)膦(PH3),原因是__________________;氨是_________分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______________键形成的晶体。
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为___________。
②若合金的密度为dg/cm3,晶胞边长a=______________nm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com