
科目: 来源: 题型:
【题目】由下列“实验操作和现象”与“结论”均正确的( )
选项 | 实验操作及现象 | 结论 |
A | 将含铁的氧化物的砖块用盐酸浸取,浸取液能使KMnO4溶液褪色 | 浸取液中含Fe2+ |
B | 常温下,测得饱和Na2CO3 溶液的pH大于饱和NaHCO3 溶液的pH | 常温下水解程度 |
C | 25℃时,向AgNO3溶液中滴加足量NaCl溶液至不再产生沉淀,然后滴加KI溶液,有黄色沉淀生成 | 25℃时,Ksp(AgCl)>Ksp(AgI) |
D | 将Cl2通入滴有酚酞的NaOH溶液后,溶液褪色 | Cl2具有漂白性 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA 为阿伏加德罗常数的值,下列说法正确的是( )
A.1mol SiO2 所含Si-O键的数目为 2 NA
B.常温下,1 L pH=9的CH3COONa 溶液中由水电离的H+ 数目为 10-9 NA
C.40 mL 10 mol/L浓盐酸与足量MnO2充分反应,生成的氯气分子数为 0.1NA
D.标准状况下,11.2 L 甲烷和乙烯混合物中含氢原子数目为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】NiCl2是化工合成中最重要的镍源。工业上利用含镍(Ni)废催化剂(主要含有Ni,还含有SiO2、Al2O3、Fe及其它不溶于酸、碱的杂质)生产氯化镍晶体(NiCl2·nH2O)流程如下:
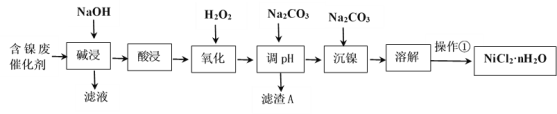
部分金属氢氧化物Ksp近似值如下表所示:
化学式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-38 | 10-34 | 10-15 |
回答下列问题:
(1)Ni的原子序数为28,位于元素周期表第四周期,最外层电子数为2,则其原子结构示意图为________________。
(2)“酸浸”、“溶解”所使用的酸为_____________。“碱浸”时发生反应的离子方程式为SiO2+2OH-=SiO32-+H2O、___________________。
(3)“氧化”加入H2O2溶液,其作用是____________________(用离子方程式表示)。然后调节pH使溶液中铁元素恰好完全沉淀(离子浓度≤10-5mol·L-1时,离子沉淀完全),此时常温下的pH约为____________。
(4)“操作①”的实验操作依次为缓缓加热,浓缩至_________________________为止、冷却结晶、过滤、洗涤、干燥,即得产品。
(5)为了测定NiCl2nH2O中结晶水数目进行如下实验:取23.8 g样品在一定条件下脱水得13.0 g NiCl2,则n=__________。
(6)镍氢电池已成为混合动力汽车的主要电池类型,其在碱性电解质溶液的工作原理如下:M+Ni(OH)2![]() MH+NiOOH(式中M为储氢合金)。写出电池充电过程中阳极的电极反应式__________________。
MH+NiOOH(式中M为储氢合金)。写出电池充电过程中阳极的电极反应式__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应N2+3H2 ![]() 2NH3刚开始时,N2的浓度为3mol·L-1 ,H2的浓度为5mol·L-1,3min后测得NH3的浓度为0.6mol·L-1则此时间内,下列反应速率表示正确的是( )
2NH3刚开始时,N2的浓度为3mol·L-1 ,H2的浓度为5mol·L-1,3min后测得NH3的浓度为0.6mol·L-1则此时间内,下列反应速率表示正确的是( )
A.v (NH3)= 0.1 mol˙L-1˙min-1B.v (N2) = 1.0 mol˙L-1˙min-1
C.v (H2) = 1.67 mol˙L-1˙min-1D.v (H2) = 0.3 mol˙L-1˙min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在298 K条件下,2mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )。
A.2H2(g) + O2(g) = 2H2O(1) △H = - 484 kJ·mol-1
B.H2O(g) = H2(g) + ![]() O2(g) △H = + 242 kJ·mol-1
O2(g) △H = + 242 kJ·mol-1
C.H2(g) + ![]() O2(g) = H2O(g) △H = + 242 kJ·mol-1
O2(g) = H2O(g) △H = + 242 kJ·mol-1
D.2H2(g) + O2(g) = 2H2O(g) △H = + 484 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在100℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为______________,混合气体的平均摩尔质量为______________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将_______________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将______________(填“向左移动”“向右移动”或“不移动”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】高温时空气中的N2和O2会反应生成NO而污染大气:N2(g)+O2(g)=2NO(g)。试通过计算说明在1 200 ℃的条件下,此反应能否正向自发进行?估算自发进行的最低温度是多少______?[已知该反应:ΔH=+180.50 kJ·mol-1,ΔS=247.7 J·mol-1·K-1]
查看答案和解析>>
科目: 来源: 题型:
【题目】(要求写出计算过程)现有一定温度下的密闭容器中存在如下反应:2SO2(g) + O2(g)![]() 2SO3(g),已知c(SO2)始=0.4mol/L,c(O2)始=1mol/L,经测定该反应在该温度下的平衡常数K≈19,试判断:
2SO3(g),已知c(SO2)始=0.4mol/L,c(O2)始=1mol/L,经测定该反应在该温度下的平衡常数K≈19,试判断:
(1)当SO2转化率为50%时,该反应是否达到平衡状态?________,若未达到,哪个方向进行?__________
(2)达平衡状态时, SO2的转化率应为________?
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将N2、H2混合气体100 mL通入密闭容器内,达到平衡时,容器内的压强比反应前减小![]() ,测得此时混合气体的平均相对分子质量为9。试求:
,测得此时混合气体的平均相对分子质量为9。试求:
(1)原混合气中N2、H2各多少毫升______?
(2)H2的转化率是多少______?
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化剂H2O2在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。
I.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(1)实验①和②的目的是_________________________________。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是_________________________(填一种方法即可)。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。
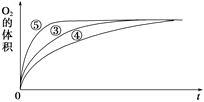
分析该图能够得出的实验结论是________________________________。
II.资料显示,某些金属离子或金属氧化物对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如下图所示的实验装置进行实验。
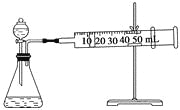
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量_______或______来比较。
(2)0.1 g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。请解释化学反应速率变化的原因:_____________。请计算H2O2的初始物质的量浓度为________________(保留两位有效数字)。
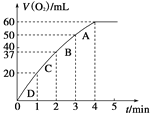
为探究MnO2在此实验中对H2O2的分解起催化作用,需补做下列实验(无 需写出具体操作):/span>a._________________;b.___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com