
科目: 来源: 题型:
【题目】在接触法制硫酸中,将SO2与空气按1∶3的体积比混合(空气中氮气与氧气的体积比为4∶1)后进入接触室,在一定条件下反应达到平衡后,气体总体积减少为原来的88%(体积均在相同情况下测定),求反应达到平衡时SO2的转化率_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知热化学方程式 2SO3(g)![]() 2SO2(g) + O2(g);△H1 = +197kJ/mol, 热化学方程式:2SO2(g) + O2(g)
2SO2(g) + O2(g);△H1 = +197kJ/mol, 热化学方程式:2SO2(g) + O2(g)![]() 2SO3(l);△H2 = — a kJ/mol 则下列说法正确的是( )
2SO3(l);△H2 = — a kJ/mol 则下列说法正确的是( )
A.a>197
B.a<197
C.a=197
D.热方程式中化学计量数可表示分子个数
查看答案和解析>>
科目: 来源: 题型:
【题目】居室装修用石材的放射性常用![]() 作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖。下列叙述中正确的是 ( )
作为标准,居里夫人(Marie Curie)因对Ra元素的研究两度获得诺贝尔奖。下列叙述中正确的是 ( )
A.Ra元素位于元素周期表中第六周期ⅡA族B.RaCl2的熔点比CaCl2高
C.一个![]() 原子中含有138个中子D.Ra(OH)2是一种两性氢氧化物
原子中含有138个中子D.Ra(OH)2是一种两性氢氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质的分类正确的是( )
A.同位素: H2 D2 T2B.非电解质: NH3、C2H5OH
C.非极性分子:C60、CO2、CH2Cl2D.同系物: ![]() -OH、CH3-
-OH、CH3-![]() -OH、CH3-
-OH、CH3-![]() -CH2OH
-CH2OH
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在800K时,反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),若起始浓度c(CO)=2mol/L,c(H2O)=3mol/L,反应达到平衡时,CO转化成CO2的转化率为60%。若将H2O的起始浓度加大为6 mol·L-1,试求CO转化为CO2的转化率____。
CO2(g)+H2(g),若起始浓度c(CO)=2mol/L,c(H2O)=3mol/L,反应达到平衡时,CO转化成CO2的转化率为60%。若将H2O的起始浓度加大为6 mol·L-1,试求CO转化为CO2的转化率____。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在一个1L的密闭容器中放入4mol N2O5气体后会发生如下两种反应:①N2O5(g)![]() N2O3(g)+O2(g);②N2O3(g)
N2O3(g)+O2(g);②N2O3(g)![]() N2O(g)+O2(g)。在某温度下达到平衡后c(O2)=4.4mol/L,c(N2O3)=1.6mol/L。求反应中N2O5的分解率____。
N2O(g)+O2(g)。在某温度下达到平衡后c(O2)=4.4mol/L,c(N2O3)=1.6mol/L。求反应中N2O5的分解率____。
查看答案和解析>>
科目: 来源: 题型:
【题目】甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补血剂。实验室以绿矾(FeSO4·7H2O)为铁源制备补血剂甘氨酸亚铁。有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物,相对分子质量为75 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶乙醇 |
Ⅰ.配制FeSO4溶液
用绿矾(FeSO4·7H2O)配制100mL1.00mol·L-1的FeSO4溶液。
(1)除托盘天平、药匙、烧杯、玻璃棒、量筒外,还需要的仪器有__。
Ⅱ.制备FeCO3
将配制好的绿矾溶液倒入烧杯中,缓慢加入200mL1.10mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
(2)反应的离子方程式为__。
Ⅲ.制备(NH2CH2COO)2Fe
制备装置如图所示(夹持和加热仪器已省略)。将Ⅱ中制备得到的FeCO3转移到装置D的三颈烧瓶中,检查气密性后,按如图所示加入足量的相关试剂,按以下操作进行实验。
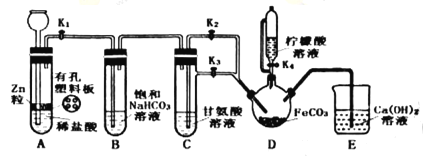
(3)关闭K2、打开K1、K3,此操作的目的是__;
(4)当观察到装置E中出现浑浊后,关闭K3、打开K2,此时可观察到的现象是__;
(5)关闭K1、K2、K3,打开K4,向三颈烧瓶中加入柠檬酸溶液,加热,使反应发生。加入柠檬酸溶液的目的除了调节溶液的pH促进FeCO3溶解,另一目的是__;
(6)反应结束后,将三颈烧瓶中所得到的混合物过滤,滤液经___(填操作)、过滤、洗涤、干燥得到产品。洗涤操作所选用的最佳洗涤试剂是__。
A.蒸馏水 B.乙醇 C.FeSO4溶液 D.柠檬酸溶液
Ⅳ.产率计算
(7)若得到的产品质量为17.96g,则产率为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+=I2+5SO42-+H2O,生成的I2可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
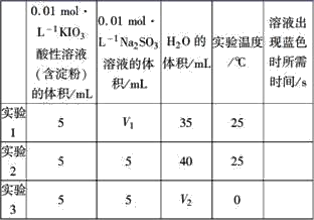
该实验的目的是_________;表中V2=_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为分别验证温度、浓度、催化剂颗粒大小对化学反应速率的影响规律,某同学设计了如下4组实验。

(1)上表中,反应速率最快的是_______;
(2)实验3、4预期可得出的结论是_______;
(3)设计实验2、3的目的是_________;
(4)设计一个实验证明在其它条件相同时,改变温度对过氧化氢分解速率的影响(写出操作步骤)__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚砜(SOCl2)在农药、制药行业中用途广泛,沸点为77℃,遇水剧烈反应,液面上产生白雾,并产生带有刺激性气味的气体。实验室用干燥的Cl2和SO2与SCl2反应合成SOCl2,反应原理是:SO2+Cl2+SCl2=2SOCl2。回答以下问题:
Ⅰ.氯化亚砜的制备
实验室拟用以下装置完成氯化亚砜的制备:
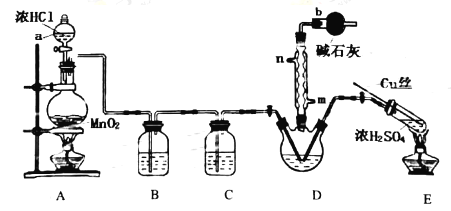
(1)仪器a的名称是__;装置D中冷凝管的冷凝水入口是__。
(2)装置A中反应的离子方程式__;装置E中反应的化学方程式__。
(3)B、C所盛试剂分别是__、__;装置D中干燥管b的作用是__。
(4)本实验的主要副产物是SCl2,已知:SOCl2沸点为77℃,SCl2的沸点为50℃,提纯SOCl2的实验操作是__;
Ⅱ.氯化亚的性质与检测
经分析,某实验小组的同学认为,SOCl2与水反应后的溶液中有盐酸和亚硫酸生成。
(5)欲证明SOCl2与水反应后形成的溶液中有H2SO3生成,可以使用的试剂是__;欲证明纯净SOCl2与水反应后形成的溶液中有Cl-,实验的操作方法是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com