
科目: 来源: 题型:
【题目】亚硝酰硫酸(NOSO4H)主要用于染料、医药等工业。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。
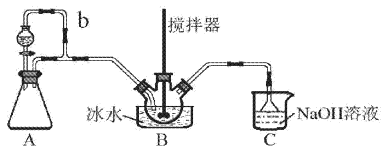
(1)装置A制取SO2
①A中反应的化学方程式为___。
②导管b的作用是___。
(2)装置B中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①该反应必须维持体系温度不得高于20℃,采取的措施除了冷水浴外,还可以是___(只写1种)。
②开始反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速度明显加快,其原因是___。
(3)装置C的主要作用是___(用离子方程式表示)。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是___。
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.380g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
①配平:__MnO4-+__C2O42-+__=__Mn2++__+__H2O
②滴定终点时的现象为___。
③亚硝酰硫酸的纯度=___。(精确到0.1%)[M(NOSO4H)=127g·mol-1]
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.35Cl与37Cl互为同素异形体
B.O2与O3互为同位素
C.![]() 与CH3CH2CH2CH3互为同分异构体
与CH3CH2CH2CH3互为同分异构体
D.乙烯与CH3—C≡CH互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、J、Q、W为前四周期元素,原子序数依次增大。元素Y在地壳中含量最高,W的一种常见高价氧化物是红棕色粉末,常用于油漆、涂料、油墨的红色染料,25℃X、Z、J、Q的最高价氧化物对应水化物溶液(浓度均为0.01mol·L-1)的pH与原子序数的关系如图所示。

根据上述信息进行判断,并回答下列问题:
(1)W在周期表中的位置__。比较X、Y、Z的简单离子半径大小为__<____<__(用离子符号表示);
(2)元素的非金属性Y__J(填“>”或“<”)。下列各项中,不能说明这一结论的有__(填序号)。
A.J的氢化物的水溶液放置在空气中会变浑浊
B.Y与J之间形成的化合物中元素的化合价。
C.Y和J的单质的状态
D.Y和J在周期表中的位置
(3)X、J、Q这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是_____(填化学式);酸根呈三角锥结构的酸是___(填化学式)。
(4)Y和Q形成的化合物Q2Y的立体构型为__,Q的单质与湿润的Na2CO3反应可制备Q2Y,其化学方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,将1L0.3mol L1HA溶液与0.1molNaOH固体混合,使之充分反应得到溶液(a)。然后向该溶液中通入HCl或加入NaOH固体(忽略体积和温度变化),溶液pH随通(加)入物质的量的变化如图。下列叙述错误的是

A. HA是一种弱酸
B. 向a点对应溶液中通入HCl,充分反应后,c(H+)/c(HA)增大
C. b点对应溶液中:c(Na+)=c(Cl-)>c(HA)>c(H+)>c(OH-)
D. c点对应溶液中:c(Na+)=c(A-)
查看答案和解析>>
科目: 来源: 题型:
【题目】稠环芳烃如萘![]() 、菲
、菲 、芘
、芘 等均为重要的有机化工原料。下列说法正确的是
等均为重要的有机化工原料。下列说法正确的是
A. 萘、菲、芘互为同系物B. 萘、菲、芘的一氯代物分别为2、5、3种
C. 萘、菲、芘中只有萘能溶于水D. 萘、菲、芘的所有原子不可能处于同一平面
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。请回答:
(1)Y元素的名称是____________。
(2)XZ3化合物的电子式是______________ 分子的立体构型_______________
(3)分别写出X、Y的最高价含氧酸的分子式_____________、______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂。实验室制备四碘化锡的主要步骤如下:
步骤1:在干燥的圆底烧瓶中加入少量碎锡箔和稍过量的I2,再加入30mL冰醋酸和30mL醋酸酐[(CH3CO)2O]。实验装置如图所示,组装好后用煤气灯加热至沸腾约1-1.5h,至反应完成;
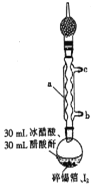
步骤2:冷却结晶,过滤得到四碘化锡粗品;
步骤3:粗品中加入30mL氯仿,水浴加热回流溶解后,趁热过滤;
步骤4:将滤液倒入蒸发皿中,置于通风橱内,待氯仿全部挥发后得到四碘化锡晶体。
回答下列问题:
(1)图中仪器a的名称为__________;冷却水从接口__________(填“b”或“c”)进入。
(2)仪器a上连接装有无水CaCl2的干燥管的目的是__________;锡箔需剪碎的目的是__________;加入醋酸酐的目的是__________。
(3)烧瓶中发生反应的化学方程式为__________;单质碘需过量的主要目的是__________。
(4)反应已到终点的现象是__________。
(5)步骤3和步骤4的目的是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(15分)周期表前四周期的元素X、Y、Z、T、W,原子序数依次增大。X的核外电子总数与其周期数相同,Y基态原子的p电子数比s电子数少1个,Z基态原子的价电子层中有2个未成对电子,T与Z同主族,W基态原子的M层全充满,N层只有一个电子。回答下列问题:
(1)Y、Z、T中第一电离能最大的是 (填元素符号,下同),原子半径最小的是 。
(2)T的原子结构示意图为 ,W基态原子的电子排布式为 。
(3)X和上述其他元素中的一种形成的化合物中,分子呈三角锥形的是 (填化学式);分子中既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写一种)。
(4)T与Z形成的化合物中,属于非极性分子的是 (填化学式)。
(5)这5种元素形成的一种阴阳离子个数比为1:1型的配合物中,阴离子呈四面体结构,阳离子的结构如图所示。该配合物的化学式为 ,阳离子中存在的化学键类型有 。
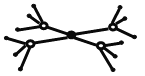
查看答案和解析>>
科目: 来源: 题型:
【题目】为了寻找高效低毒的抗肿瘤药物,化学家们合成了一系列新型的1,3- 二取代酞嗪酮类衍生物。
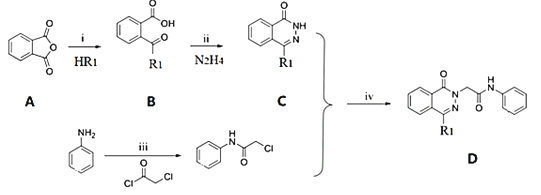
(1)化合物B 中的含氧官能团为__________和__________(填官能团名称)。
(2)反应i-iv中属于取代反应的是___________。
(3)ii的反应方程式为___________。
(4)同时满足下列条件的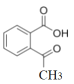 的同分异构体共有_____种,写出其中一种的结构简式: _______
的同分异构体共有_____种,写出其中一种的结构简式: _______
I.分子中含苯环;II.可发生银镜反应;III.核磁共振氢谱峰面积比为1∶2∶2∶2∶1
(5)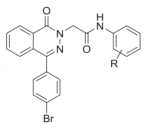 是一种高效低毒的抗肿瘤药物,请写出以
是一种高效低毒的抗肿瘤药物,请写出以![]() 和
和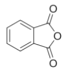 和
和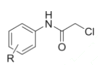 为原料制备该化合物的合成路线流程图(无机试剂任用):______________。
为原料制备该化合物的合成路线流程图(无机试剂任用):______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化硫(SO2)是一种在空间地理、环境科学、地质勘探等领域受到广泛研究的一种气体。
Ⅰ.某研究小组设计了一套制备及检验SO2部分性质的装置,如图所示:
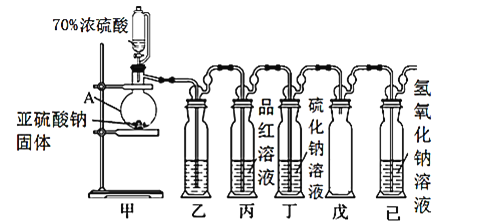
(1)仪器A的名称____________。
(2)装置乙的作用是为了观察生成SO2的速率,则装置乙中加入的试剂是____________。
(3)①实验前有同学提出质疑:该装置没有排空气,而空气中的O2氧化性强于SO2,因此装置丁中即使有浑浊现象也不能说明是SO2导致的。请你写出O2与Na2S溶液反应的化学反应方程式____________。
②为进一步检验装置丁产生浑浊现象的原因,进行新的实验探究。实验操作及现象见表:
序号 | 实验操作 | 实验现象 |
1 | 向10 mL 1 mol/L Na2S溶液中通O2 | 15 min后,溶液才出现浑浊 |
2 | 向10 mL 1 mol/L Na2S溶液中通SO2 | 溶液立即出现黄色浑浊 |
由实验现象可知:该实验条件下Na2S溶液出现浑浊现象是SO2导致的。你认为上表实验1反应较慢的原因可能是____________。
Ⅱ.铁矿石中硫元素的测定可以使用燃烧碘量法,其原理是以氮气为载体,以稀盐酸、淀粉和碘化钾的混合溶液为吸收液,用0.0010 mol·L-1KIO3标准溶液进行滴定。检测装置如图所示:
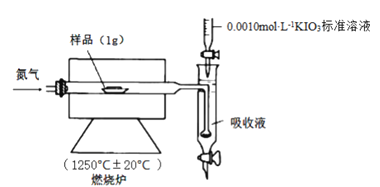
[查阅资料] ①实验进行5min样品中的S元素都可转化为SO2
②2IO3-+5SO2+4H2O=8H++5SO42-+I2
③I2+SO2+2H2O=2I-+SO42-+4H+
④IO3-+5I-+6H+=3I2+3H2O
(4)工业设定的滴定终点现象是____________。
(5)实验一:不放样品进行实验,5 min后测得消耗标准液体积为V1
实验二:加入1 g样品再进行实验,5 min后测得消耗标准液体积为V2
①比较数据发现V1远远小于V2,可忽略不计。则设置实验一的目的是___________。
②测得V2的体积如表:
序号 | 1 | 2 | 3 |
KIO3标准溶液体积/mL | 10.02 | 9.98 | 10.00 |
该份铁矿石样品中硫元素的质量百分含量为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com