
科目: 来源: 题型:
【题目】实验室为标定一种烧碱样品的物质的量浓度,称取该烧碱样品4.0g配成1L溶液,取出20.00mL置于锥形瓶中,以甲基橙为指示剂,用0.10mol·L-1HCl标准溶液滴定,恰好完全中和时消耗标准盐酸19.00mL,若烧碱中只含有一种杂质,则不可能是( )
A.NaClB.Ca(OH)2C.Na2CO3D.NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】普鲁苯辛用于治疗胃炎、胰腺炎、胆汁排泄障碍、多汗症、孕妇呕吐及遗尿。普鲁苯辛的合成路线如下:

回答下列问题:
(1)有机物A的名称是_____,F中官能团的名称是 ____。
(2)碳原子上连有四个不同的原子或基团时,该碳称为手性碳。普鲁苯辛结构式中____(填“有”或“没有”)手性碳原子。
(3)A→B的反应类型为____。
(4)C→D反应的化学方程式为____。
(5)X是C的同分异构体,X中除苯环外不含其他环状结构,X能与FeCl3溶液发生显色反应,符合条件的X 的结构有____种,其中核磁共振氢谱为3组峰,峰面积之比为1:2:2的X的结构简式为____。
(6)参考上述流程,设计以CH2=CHCH2OH、乙酸、甲醇为起始原料合成![]() 的合成线路(无机试剂任选)____
的合成线路(无机试剂任选)____
查看答案和解析>>
科目: 来源: 题型:
【题目】据报道,在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实:2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g),下列叙述错误的是
CH3CH2OH(g)+3H2O(g),下列叙述错误的是
A.使用Cu-Zn-Fe催化剂可大大提高生产效率
B.反应需在300℃进行可推测该反应是吸热反应
C.充入大量CO2气体可提高H2的转化率
D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用空气氧化(NH4)2SO3的方法制取(NH4)2SO4,某研究小组用如图装置模拟该过程,并通过测定反应后溶液中SOT的浓度来计算该反应的转化率。

实验步骤如下:
①按图连接好装置,检查装置气密性;
②取200 mL 0.5000 molL-1(NH4)2SO3溶液(调节pH = 8)装入三颈烧瓶中,加入催化剂,控制气体流速为300 Lh-1,在温度为50℃下进行实验;
③反应2.5 h后,测定反应后溶液中SO32-的浓度。
回答下列问题:
(1)仪器M的名称为_____,仪器M中装有H2O2溶液,则装置A中发生反应的化学方程式为_______。
(2)实验中通如N2的目的是_____。
(3)装置B的作用是_____(任答一条)。
(4)装置C中采用多孔球泡的目的是_____,已知亚硫酸铵溶液的pH小于8,要调节装置C中溶液的pH=8,应向该溶液中加入一定量的_____(填标号
a NH3 H2O b Ba(OH)2 c 澄清石灰水
(5)该实验缺少的装置是_____。
(6)取VmL反应后的溶液(反应前后体积不变)于碘量瓶中,滴入3滴淀粉溶液,用a molL-1的标准碘溶 液滴定至终点时,消耗碘水的体积为b mL,则(NH4 )2SO3的转化率为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
A.升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大
C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动
D.25℃时,欲使醋酸溶液pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中可以证明反应H2(g)+I2(g)![]() 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是
①单位时间内生成nmol H2的同时生成nmol HI;②一个H-H键断裂的同时有两个H-I键断裂;③百分含量w(HI)=w(I2);④反应速率v(H2)=v(I2)=v(HI);⑤c(HI)∶c(H2)∶c(I2)=2∶1∶1;⑥温度和体积一定时,生成物浓度不再变化;⑦温度和体积一定时,容器内的压强不再变化;⑧条件一定时,混合气体的平均相对分子质量不再变化;⑨温度和体积一定时,混合气体颜色不再变化;⑩温度和压强一定时,混合气体的密度不再变化
A.①②③④B.②⑥⑨C.②⑥⑨⑩D.③⑤⑥⑦⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:①H2(g)+ ![]() O2(g)=H2O(g);ΔH1= akJ·mol-1
O2(g)=H2O(g);ΔH1= akJ·mol-1
②2H2(g)+O2(g) = 2H2O(g);ΔH2= b kJ·mol-1 ③ H2(g)+ ![]() O2(g)=H2O(l);ΔH3= c kJ·mol-1
O2(g)=H2O(l);ΔH3= c kJ·mol-1
④2H2(g)+O2(g) = 2H2O(l);ΔH4= d kJ·mol-1,下列关系式中正确的是( )
A.2a=b<0B.b>d>0C.a<c<0D.2c=d>0
查看答案和解析>>
科目: 来源: 题型:
【题目】钛、铬、铁、镍、铜等金属及其化合物在工业上都有重要用途。
(1)基态钛原子外围电子的轨道表达式为_____。与钛同周期的元素中,基态原子的未成对电子数与钛原子相同的有_____种。
(2)TiCl4是氯化法制取钛的中间产物。TiCl4和SiC14在常温下都是液体,分子结构相同。采用蒸馏的方法分离TiCl4和SiCl4的混合物,先获得的馏分是_____(填化学式)。
(3)[Cr(C2O4)2(H2O2)]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有_____键。
(4)雷氐盐(Reinecke salt)的化学式为NH4[Cr(NCS)4(NH3)2] H2O,是一种易溶于水和乙醇的暗红色固体。
①雷氏盐中铬元素的化合价为_____。
②NCS的立体构型是_____,其中碳原子的杂化轨道类型为_____。
③SO2、CO2、BeCl2、SCl2四种分子中,与NCS-互为等电子体的有_____(填化学式)。
(5)Ni和La的合金是目前使用广泛的储氢材料,具有容量大、寿命长、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
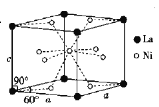
①晶体的化学式为_____。
②该晶胞的密度为dgcm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是____(用含d、NA的代数式表示)cm3。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知: a=511pm,c=397pm;标准状况下,氢气的密度为8.98X10-5 g, ![]() ,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_____(保留整数)。
,若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为_____(保留整数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
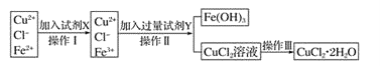
请参照下表给出的数据填空。

(1)操作I加入X的目的是___________________________ 。
(2)下列物质都可以作为X,适合本实验的X物质可以是_________(填字母)。
A KMnO4 B NaClO C H2O2 D Cl2
(3)操作II的Y试剂为____________(填化学式),并调节溶液的pH在______范围。
(4)实验室在配制CuCl2溶液时需加入少许_________(填物质名称),理由是(文字叙述并用有关离子方程式表示)__________________________________________。
(5)若将CuCl2溶液蒸干灼烧,得到的固体是_________________(填化学式);若要得无水CuCl2,请简述操作方法______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】3—对甲苯丙烯酸甲酯(E)是一种用于合成抗血栓药的中间体,其合成路线如图:
![]() +CO
+CO![]()
![]()
![]() B
B![]()
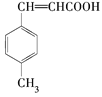
![]() E
E
已知:HCHO+CH3CHO![]() CH2=CHCHO+H2O
CH2=CHCHO+H2O
(1)遇FeCl3溶液显紫色且苯环上有两个取代基的A的同分异构体有____种。B中含氧官能团的名称为____。
(2)试剂C可选用下列中的____。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.新制Cu(OH)2悬浊液
(3) 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为____。
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为____。
(4)E在一定条件下可以生成高聚物F,F的结构简式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com