
科目: 来源: 题型:
【题目】硫在自然界中以游离态和多种化合态形式出现,硫的化合物大多具有氧化性或还原性,许多金属硫化物难溶于水。完成下列填空:
【1】硫化氢具有还原性,可以和许多氧化剂反应。在酸性条件下,H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式____________。
【2】向ZnSO4溶液中滴加饱和H2S溶液,没有沉淀生成,继续滴加一定量的氨水后,生成ZnS沉淀。用电离平衡原理解释上述现象。____
【3】为了使Na2S溶液中![]() 的比值变小,可适量加入(或通入)的物质是_______。
的比值变小,可适量加入(或通入)的物质是_______。
a.H2S气体 b.NaOH固体 c.HCl气体 d.KOH固体
向Na2S固体中分别加入浓硫酸和稀硫酸,所得产物____________(填“相同”或“不同”),由此可知硫酸氧化性的强弱与______________有关。
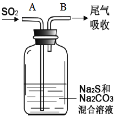
【4】在如图中,从A管通入一定量SO2后,在B处检测到有新的气体生成。B处排出的气体中(填“含”或“不含”)________ H2S,原因是__________。
【5】常压下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
温度(℃) | c(氨水)(mol/L) | 电离程度(%) | c(OH-)(mol/L) |
0 | 16.56 | 9.098 | 1.507×10-2 |
10 | 15.16 | 10.18 | 1.543×10-2 |
20 | 13.63 | 11.2 | 1.527×10-2 |
表中c(OH-)基本不变的原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用可逆反应N2(g)+3H2(g) ![]() 2NH3(g)合成氨,下列叙述正确的是( )
2NH3(g)合成氨,下列叙述正确的是( )
A.合成氨的适宜条件是高温高压催化剂,其中催化剂不改变该反应的逆反应速率
B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,NH3 (g)的浓度分别是c1、c2,则时间间隔t1~t2内,NH3 (g)生成的平均速率为v=![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X2 (g) + H2(g)![]() 2HX(g)+ Q(X2 表示Cl2、Br2)。
2HX(g)+ Q(X2 表示Cl2、Br2)。

如图表示上述反应的平衡常数K与温度T的关系。
①Q表示X2(g)与H2(g)反应的反应热,Q_____0(填“>”、“<”或 “=”)。写出曲线b表示的平衡常数K的表达式,K=_________(表达式中写物质的化学式)。
②对于固定容器的平衡体系的反应:I2 (g)+ H2(g)![]() 2HI(g)+ Q,加压同时降温,平衡将_____(向正,向逆,不移动);充入氢气时,K值__________(增大,减小,不变)。
2HI(g)+ Q,加压同时降温,平衡将_____(向正,向逆,不移动);充入氢气时,K值__________(增大,减小,不变)。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据反应:2Na2CO3+ SnO2+4S![]() Na2SO4 + Na2SnS3+2CO2↑ ,回答下列问题:
Na2SO4 + Na2SnS3+2CO2↑ ,回答下列问题:
【1】①写出碳原子最外电子层的轨道表示式______。在上述反应的生成物中,属于分子晶体的化合物的结构式为______。
②在上述反应中非金属元素的非金属性由强到弱顺序为:______;其中的单质原子核外有______种不同能量的电子。
【2】上述反应中,金属性最强的元素与铝元素相比较,可以作为判断两者金属性强弱依据的是_________(选填编号)。
a.能否置换出硫酸铜溶液中的铜离子
b.Al(OH)3能否溶解在该元素最高价氧化物对应的水化物中
c.单质与氯气化合时失去电子数目的多少
d.单质与同浓度的稀盐酸发生反应的剧烈程度
【3】在上述反应中氧化剂与还原剂的物质的量之比是________。常温下,测得Na2SnS3溶液pH>7,请用离子方程式解释其原因:________。
【4】锡(Sn)元素的单质有两种常见的同素异形体——灰锡和白锡。已知:Sn(s、灰)![]() Sn(s、白)-2.1 kJ,根据以上信息得出的结论正确的是__________。
Sn(s、白)-2.1 kJ,根据以上信息得出的结论正确的是__________。
a.灰锡和白锡的互相转化是可逆反应
b.常温下锡主要以灰锡的状态存在
c.白锡所具有的能量高
d.同素异形体的相互转化肯定也是化学变化,但却不属于氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】用以下图示装置研究物质的性质,能够获得可靠结论的是
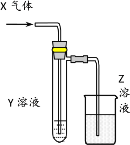
X | Y | Z | 结论 | |
A | HCHO | 新制Cu(OH)2 | NaOH(aq) | 验证甲醛的还原性 |
B | CH3Cl | AgNO3(aq) | NaOH(aq) | 验证一氯甲烷含氯元素 |
C | SO2 | KMnO4(aq) | NaOH(aq) | 验证二氧化硫的漂白性 |
D | Cl2 | 淀粉KI(aq) | NaOH(aq) | 验证氯气的强氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )

A. 每生成2 mol AB吸收bkJ热量
B. 该反应热△H= + (a-b)kJ mol-1
C. 该反应中反应物的总能量高于生成物的总能量
D. 断裂1 mol A—A和1 mol B—B键,放出akJ能量
查看答案和解析>>
科目: 来源: 题型:
【题目】测定0.1 mol·L-1 Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是
A. Na2SO3溶液中存在水解平衡:![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的Kw值相等
查看答案和解析>>
科目: 来源: 题型:
【题目】40℃硝酸钾饱和溶液先升温至80℃,在恒温下蒸发部分溶剂至析出少量溶质,然后将溶液逐渐冷却至60℃.下列示意图中能正确表示整个过程中溶液浓度a%与时间t关系的是( )
A.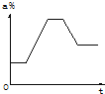 B.
B. C.
C. D.
D.
查看答案和解析>>
科目: 来源: 题型:
【题目】用测量压强的仪器测定生铁在90%醋酸溶液中发生腐蚀的装置及容器内压强随时间变化如图所示,下列分析错误的是

A.0~t1,可能发生了析氢腐蚀压强增大
B.0~t1,可能反应放热温度升高压强增大
C.t2时压强小于起始压强,一定发生了吸氧腐蚀
D.整个过程中铁粉发生了还原反应生成Fe2+
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是
A.25℃时,pH=13的1.0LBa(OH) 2溶液中含有的OH-的数目为0.1NA
B.2 gH218O中含有的质子数为NA
C.8 g CuO与足量H2充分反应生成Cu,该反应转移的电子数为0.2NA
D.标准状况下,11.2 L Cl2溶于水,溶液中Cl—、ClO—和HClO的微粒数之和为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com