
科目: 来源: 题型:
【题目】α﹣苯基丙烯酸可用于合成人造龙涎香,现以甲苯为原料,按下列方法合成(从F开始有两条合成路线)
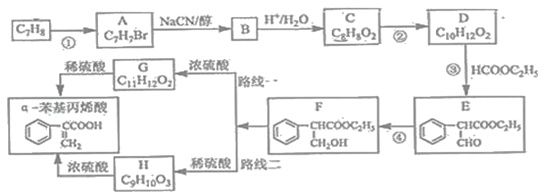
已知:①CH3CH2Br+NaCN![]() CH3CH2CN+NaBr
CH3CH2CN+NaBr
②CH3CH2CN![]() CH3CH2COOH
CH3CH2COOH
完成下列填空:
(1)写出D的结构简式______。
(2)写出反应类型:反应④______。
(3)写出反应所需要试剂与条件:反应①______,反应②______。
(4)写出一种满足下列条件的D的同分异构体的结构简式______。
①能发生银镜反应
②能与FeCl3溶液发生显色反应
③分子中有5种不同化学环境的氢原子
(5)检验E是否完全转化为F的方法是______。
(6)路线二与路线一相比不太理想,理由是______。
(7)利用已知条件,设计一条由![]() 制备
制备![]() 的合成路线_________________。(合成路线的表示方法为:A
的合成路线_________________。(合成路线的表示方法为:A![]() B…
B…![]() 目标产物)
目标产物)
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是一个石墨作电极,电解稀的Na2SO4溶液的装置,通电后在石墨电极A和B附近分别滴加一滴石蕊溶液。下列有关叙述正确的是
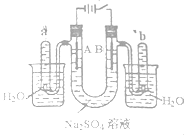
A.逸出气体的体积,A电极的小于B电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.A电极附近呈红色,B电极附近呈蓝色
D.电解一段时间后,将全部电解液转移到同一烧杯中,充分搅拌后溶解呈中性
查看答案和解析>>
科目: 来源: 题型:
【题目】碳碳双键在酸性高锰酸钾溶液中发生断键氧化过程:![]()
![]()
![]() +
+![]()
完成下列填空:
(1)月桂烯是一种常见香料,其结构如图所示![]() 。
。
①月桂烯与等物质的量的Br2发生加成反应,可以得到______种产物。
②月桂烯与酸性高锰酸钾溶液反应时可生成多种有机产物,其中碳原子数最多的一种产物的结构简式为______。
③金刚烷(见图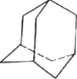 )是月桂烯的一种同分异构体,其一氯代物有______种。
)是月桂烯的一种同分异构体,其一氯代物有______种。
(2)烃X在酸性高锰酸钾溶液中生成等物质的量的丙酮(CH3COCH3)与羧酸Y(C5H10O2),且Y中仅含两种不同化学环境的氢原子,则Y的结构简式是______,X的系统命名为______。
(3)化学式为C8H12的烃Z,在酸性高锰酸钾溶液中生成CH3COCH2COOH,写出Z可能的结构简式:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硝酸铝是一种常用皮革鞣剂.工业上用铝灰(主要含Al、A12O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3﹒nH2O]的流程如下:
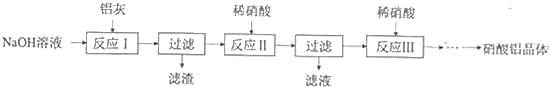
完成下列填空:
(1)用NaOH固体配制30%的NaOH溶液,所需的玻璃仪器除烧杯外,还有______。
a.容量瓶 b.量筒 c.烧瓶
(2)反应Ⅱ中为避免铝的损失,需要解决的问题是______。
(3)从反应Ⅲ所得溶液中得到硝酸铝晶体的步骤依次是:减压蒸发、______、过滤、______、低温烘干.
(4)有人建议将反应Ⅱ、Ⅲ合并以简化操作,说明工业上不采用这种方法的原因______。
(5)某同学在实验室用铝灰制各硝酸铝晶体,其流程如下:
氢氧化物 | Fe(OH)3 | Al(OH)3 |
开始沉淀pH | 1.9 | 4.2 |
沉淀完全pH | 3.2 | 5.4 |
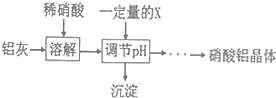
调节pH的目的是______,为使得到的硝酸铝晶体较纯净,所用的X物质可以是______(填编号)。
A.氨水 B.铝 c.氢氧化铝 D.偏铝酸钠
(6)该实验室制法与工业上制法相比,其缺点是______。
(7)称取7.392g硝酸铝晶体样品,加热灼烧使其分解完全,最终得到1.020gAl2O3,计算硝酸铝晶体样品中结晶水的数目为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】空气质量评价的主要污染物为PM10、PM2.5、SO2、NO2、O3和CO等物质.其中,NO2与SO2都是形成酸雨的主要物质.在一定条件下,两者能发生反应:NO2(g)+SO2(g)SO3(g)+NO(g)
完成下列填空:
(1)在一定条件下,将等物质的量的NO2、SO2气体置于体积固定的密闭容器中发生反应,下列能说明反应已经达到平衡状态的是______.
a.v(NO2)生成=v(SO2)消耗 b.混合物中氧原子个数不再改变
c.容器内气体颜色不再改变 d.容器内气体平均相对分子质量不再改变
(2)当空气中同时存在NO2与SO2时,SO2会更快地转变成H2SO4,其原因是______.
(3)科学家正在研究利用催化技术将NO2和CO转变成无害的CO2和N2,反应的化学方程式:2NO2(g)+4CO(g)![]() 4CO2(g)+N2(g)+Q(Q>0),若在密闭容器中充入NO2和CO,下列措施能提高NO2转化率的是______.
4CO2(g)+N2(g)+Q(Q>0),若在密闭容器中充入NO2和CO,下列措施能提高NO2转化率的是______.
A.选用高效催化剂 B.充入NO2C.降低温度 D.加压
(4)请写出N原子最外层电子轨道表达式______,写出CO2的电子式______.
(5)关于S、N、O、C四种元素的叙述正确的是______.
A.气态氢化物均为极性分子 B.最高化合价均等于原子最外层电子数
C.单质一定为分子晶体 D.原子最外层均有两种不同形状的电子云
(6)写出一个能够比较S元素和C元素非金属性强弱的化学反应方程式:______.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为以Pt为电极的氢氧燃料电池的工作原理示意图,稀H2SO4溶液为电解质溶液。下列有关说法不正确的是

A. a极为负极,电子由a极经外电路流向b极
B. a极的电极反应式:H2-2e-===2H+
C. 电池工作一段时间后,装置中c(H2SO4)增大
D. 若将H2改为CH4,消耗等物质的量的CH4时,O2的用量增多
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.恒温恒压容器中,反应A(s)+2B(g) ![]() 2C(g)达平衡后,再通入气体C,再达平衡时气体B的浓度保持不变
2C(g)达平衡后,再通入气体C,再达平衡时气体B的浓度保持不变
B.恒温恒容容器中,通入一定量的N2O4,反应 N2O4 (g) ![]() 2NO2 (g)达平衡后,再通入N2O4,平衡正向移动,再达平衡时N2O4的转化率增大
2NO2 (g)达平衡后,再通入N2O4,平衡正向移动,再达平衡时N2O4的转化率增大
C.恒温下,向密闭容器中加入NH2COONH4固体,发生反应NH2COONH4(s) ![]() 2NH3(g)+CO2(g) ,混合气体的平均相对分子质量不再随时间变化时反应达平衡状态
2NH3(g)+CO2(g) ,混合气体的平均相对分子质量不再随时间变化时反应达平衡状态
D.恒温恒容容器中,N2(g)+3H2(g) ![]() 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大
2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大
查看答案和解析>>
科目: 来源: 题型:
【题目】a、b、c、d四种短周期元素在周期表中分布如图所示,下列说法正确的是( )

A.若四种元素均为主族元素,则d元素的原子半径最大
B.若b最外层电子占据三条轨道,则a的单质可用于冶炼金属
C.若a为非金属元素,则c的气态氢化物的水溶液可能呈碱性
D.若a最外层有两个未成对电子,则d的单质常温下不可能为气体
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 向0.1 mol·L1 Na2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. 常温下,pH=6的NaHSO3溶液中:c(![]() )c(H2SO3)=9.9×107 mol·L1
)c(H2SO3)=9.9×107 mol·L1
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:![]() <
<![]()
D. 0.1 mol·L1 Na2C2O4溶液与0.1 mol·L1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学反应的表述正确的是
A.电解熔融NaCl:2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B.NaHS溶液显碱性:HS-+H2O![]() H3O++S2-
H3O++S2-
C.明矾净水:Al3++3H2O=Al(OH)3(胶体)+3H+
D.制备TiO2纳米粉:TiCl4+(x+2)H2O(过量) = TiO2·xH2O↓+4HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com