
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩш![]() ЮЊАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
ЮЊАЂЗќМгЕТТоГЃЪ§ЕФжЕЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
A.ГЃЮТГЃбЙЯТЃЌ![]() жаЫљКЌжазгЪ§ЮЊ
жаЫљКЌжазгЪ§ЮЊ![]()
B.![]() ШмвКжаКЌга
ШмвКжаКЌга![]() Ъ§ФПаЁгк
Ъ§ФПаЁгк![]()
C.ШлШкзДЬЌЯТЃЌ![]() жаЫљКЌбєРызгЪ§ФПЮЊ2
жаЫљКЌбєРызгЪ§ФПЮЊ2![]()
D.25ЁуCЪБЃЌ![]() ЕФЬМЫсФЦШмвКжаЃЌгЩЫЎЕчРыГіЕФ
ЕФЬМЫсФЦШмвКжаЃЌгЩЫЎЕчРыГіЕФ![]() Ъ§ФПЮЊ
Ъ§ФПЮЊ![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПН№ЪєютЃЈ![]() ЃЉдкЙЄвЕКЭЙњЗРНЈЩшжагаживЊЕФзїгУЁЃютЕФГЃМћЛЏКЯМлЮЊ
ЃЉдкЙЄвЕКЭЙњЗРНЈЩшжагаживЊЕФзїгУЁЃютЕФГЃМћЛЏКЯМлЮЊ![]() ЁЃгЩютОЋПѓЃЈжївЊГЩЗжЪЧ
ЁЃгЩютОЋПѓЃЈжївЊГЩЗжЪЧ![]() ЃЉжЦБИЕЅжЪютКЭютЫсФЦОЇЬхЃЈ
ЃЉжЦБИЕЅжЪютКЭютЫсФЦОЇЬхЃЈ![]() ЃЉЃЌВПЗжСїГЬШчЯТЭМЫљЪОЃК
ЃЉЃЌВПЗжСїГЬШчЯТЭМЫљЪОЃК
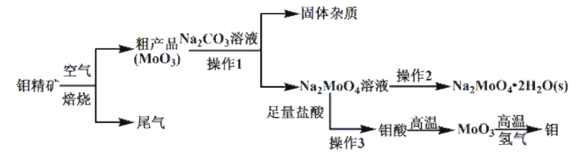
вбжЊЃКютЫсЮЂШмгкЫЎЃЌПЩШмгкМюШмвКЁЃ
ЛиД№ЯТСаЮЪЬтЃК
(1)ютОЋПѓдкПеЦјжаБКЩеЪБЃЌЗЂЩњЕФжївЊЗНГЬЪНЮЊ_______________________ЁЃ
(2)ютОЋПѓБКЩеЪБХХЗХЕФЮВЦјЖдЛЗОГЛсВњЩњЮЃКІЃЌЧыФуЬсГівЛжжЪЕбщЪвГ§ШЅИУЮВЦјЕФЗНЗЈ________________________ЁЃ
(3)Вйзї2ЕФУћГЦЮЊ_________________________________ЁЃ
(4)ЪЕбщЪвгЩютЫсОИпЮТжЦ![]() ЃЌЫљгУЕНЕФЙшЫсбЮВФСЯвЧЦїЕФУћГЦЪЧ____________________________ЁЃ
ЃЌЫљгУЕНЕФЙшЫсбЮВФСЯвЧЦїЕФУћГЦЪЧ____________________________ЁЃ
(5)Вйзї1жаЃЌМгШыЬМЫсФЦШмвКГфЗжЗДгІКѓЃЌМюНўвКжа![]() ЁЂ
ЁЂ![]() ЃЌдкНсОЇЧАашМгШы
ЃЌдкНсОЇЧАашМгШы![]() ЙЬЬхвдГ§ШЅШмвКжаЕФ
ЙЬЬхвдГ§ШЅШмвКжаЕФ![]() ЁЃЕБ
ЁЃЕБ![]() ПЊЪМГСЕэЪБЃЌ
ПЊЪМГСЕэЪБЃЌ![]() ЕФШЅГ§ТЪЪЧ_________ЁЃ[
ЕФШЅГ§ТЪЪЧ_________ЁЃ[![]() ЁЂ
ЁЂ![]() ЃЌШмвКЬхЛ§БфЛЏПЩКіТдВЛМЦ]
ЃЌШмвКЬхЛ§БфЛЏПЩКіТдВЛМЦ]
(6)БКЩеютОЋПѓЫљгУЕФзАжУЪЧЖрВуБКЩеТЏЃЌЭМ2ЮЊИїТЏВуЙЬЬхЮяСЯЕФЮяжЪЕФСПЕФАйЗжЪ§ЃЈ![]() ЃЉЁЃ
ЃЉЁЃ
Ђй![]() ___________ЁЃ
___________ЁЃ
ЂкБКЩеТЏжавВЛсЗЂЩњ![]() гы
гы![]() ЗДгІЩњГЩ
ЗДгІЩњГЩ![]() КЭ
КЭ![]() ЃЌЛЙдМСЮЊ_________ЁЃШєЗДгІжазЊвЦ
ЃЌЛЙдМСЮЊ_________ЁЃШєЗДгІжазЊвЦ![]() ЃЌдђЯћКФЕФЛЙдМСЕФЮяжЪЕФСПЮЊ______________ЁЃ
ЃЌдђЯћКФЕФЛЙдМСЕФЮяжЪЕФСПЮЊ______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПюмЕФЛЏКЯЮядкЙЄвЕЩњВњЁЂЩњУќПЦММЕШаавЕгаживЊгІгУЁЃ
(1)ЛљЬЌCo2+ЕФКЫЭтЕчзгХХВМЪНЮЊ____ЁЃ
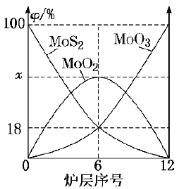
(2)FeЁЂCoОљФмгыCOаЮГЩХфКЯЮя,ШчFe(CO)5ЁЂCo2(CO)8ЕФНсЙЙШчЭМ1ЁЂЭМ2ЫљЪО,ЭМ1жа1 mol Fe(CO)5КЌга____molХфЮЛМќ,ЭМ2жаCдзгЕФдгЛЏЗНЪНЮЊ____,аЮГЩЩЯЪіСНжжЛЏКЯЮяЕФЫФжждЊЫижаЕчИКадзюДѓЕФЪЧ____(ЬюдЊЫиЗћКХ)ЁЃ
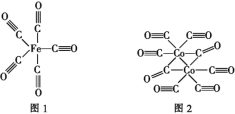
(3)Н№ЪєюмЕФЖбЛ§ЗНЪНЮЊСљЗНзюУмЖбЛ§,ЦфХфЮЛЪ§ЪЧ____,юмОЇЬхОЇАћНсЙЙШчЭМ3ЫљЪО,ИУОЇАћжадзгИіЪ§ЮЊ____;ИУОЇАћЕФБпГЄЮЊa nm,ИпЮЊc nm,ИУОЇАћЕФУмЖШЮЊ____(NAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕ,СаГіДњЪ§ЪН)gЁЄcm-3ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТЃЌЯђШнЛ§ЮЊ1LЕФУмБеШнЦїжаГфШы2mol AКЭ1![]() BЃЌЗЂЩњШчЯТЗДгІЃК
BЃЌЗЂЩњШчЯТЗДгІЃК![]() ЃЌ5minКѓЗДгІДяЕНЦНКтЃЌетЪБCЕФХЈЖШЮЊ1.2
ЃЌ5minКѓЗДгІДяЕНЦНКтЃЌетЪБCЕФХЈЖШЮЊ1.2![]() ЃЌЧыЛиД№ЃК
ЃЌЧыЛиД№ЃК
ЃЈ1ЃЉ5minФкAЯћКФЫйТЪ![]() ________________________________ЃЛ
________________________________ЃЛ
ЃЈ2ЃЉФмХаЖЯИУЗДгІДяЕНЛЏбЇЦНКтзДЬЌЕФвРОнЪЧ__________________ЃЛ
AЃЎЛьКЯЦјЬхЕФбЙЧПБЃГжВЛБф BЃЎЕЅЮЛЪБМфФкЩњГЩ2molAЕФЭЌЪБЩњГЩ1mol B
CЃЎЛьКЯЦјЬхЕФУмЖШБЃГжВЛБф DЃЎAЁЂBЁЂCЕФЮяжЪЕФСПжЎБШЮЊ![]()
ЃЈ3ЃЉИУЗДгІЕФЦНКтГЃЪ§БэДяЮЊK=_______________________ЃЌИУЮТЖШЯТЗДгІЕФЦНКтГЃЪ§ЪЧ_________ЃЛ
ЃЈ4ЃЉBдкДЫЬѕМўЯТЕФзЊЛЏТЪЮЊ___________________ЃЛ
ЃЈ5ЃЉЩ§ИпЮТЖШЃЌЛьКЯЦјЬхЕФЦНОљЯрЖдФІЖћжЪСПМѕаЁЃЌдђе§ЗДгІЮЊ________ЃЈЬюЁАЮќШШЁБЛђЁАЗХШШЁБЃЉЗДгІЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПБНбѕВМТхЗвОпгаСМКУЕФНтШШЁЂеђЭДЁЂПЙбзЁЂПЙЗчЪЊзїгУ ,БНбѕВМТхЗвЕФКЯГЩТЗЯп:
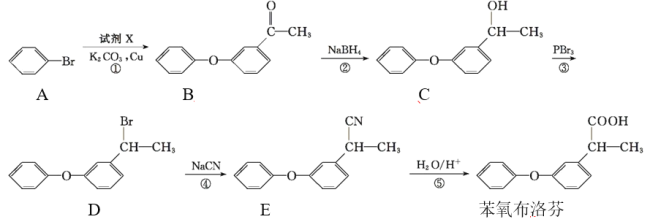
ЛиД№ЯТСаЮЪЬт:
(1)БНбѕВМТхЗвжаЙйФмЭХЕФУћГЦЮЊ____ЁЃ
(2)ЬМдзгЩЯСЌга4ИіВЛЭЌЕФдзгЛђЛљЭХЪБ,ИУЬМГЦЮЊЪжадЬМЁЃA~DЫФжжЮяжЪжа,КЌгаЪжадЬМЕФгаЛњЮяЮЊ____(ЬюзжФИ)ЁЃ
(3)ЗДгІЂкЕФЗДгІРраЭЪЧ____ЁЃ
(4)ШєЙ§ГЬЂйЗЂЩњЕФЪЧШЁДњЗДгІ,ЧвСэвЛжжВњЮяЮЊHBr,гЩAЩњГЩBЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____ЁЃ
(5)гаЛњЮяMгыCЛЅЮЊЭЌЗжвьЙЙЬх,MТњзуЯТСаЬѕМў:
Ђё.ФмгыFeCl3ШмвКЗЂЩњЯдЩЋЗДгІ,1 mol MПЩЯћКФ2 mol NaOH;
Ђђ.MЗжзгжага6жжВЛЭЌЛЏбЇЛЗОГЕФЧт,КЫДХЙВеёЧтЦзЮЊ3ЁУ2ЁУ2ЁУ2ЁУ2ЁУ3,ЧвЗжзгжаКЌга![]() НсЙЙЁЃ
НсЙЙЁЃ
аДГіЗћКЯЬѕМўЕФMЕФвЛжжНсЙЙМђЪН:____ЁЃ
(6)ИљОнвбгажЊЪЖВЂНсКЯЯрЙиаХЯЂ,аДГівдБћЭЊ(CH3COCH3)ЮЊдСЯжЦБИ2-МзЛљБћЫсЕФКЯГЩТЗЯпСїГЬЭМ(ЮоЛњЪдМСШЮгУ)ЁЃ_________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвгУЫсадЪДПЬЗЯвК(КЌCu2+ЁЂH+ЁЂCuC![]() ЁЂCl-ЕШ)КЭМюадЪДПЬЗЯвК[N
ЁЂCl-ЕШ)КЭМюадЪДПЬЗЯвК[N![]() ЁЂCu(NH3
ЁЂCu(NH3![]() ЁЂNH3ЁЄH2OЕШ]жЦБИCuI(АзЩЋЙЬЬх)ЕФЪЕбщСїГЬШчЯТ:
ЁЂNH3ЁЄH2OЕШ]жЦБИCuI(АзЩЋЙЬЬх)ЕФЪЕбщСїГЬШчЯТ:

(1)ВНжшЂёжаЗЂЩњСЫЖрИіЗДгІ,ЦфжаCu(NH3![]() гыбЮЫсЗДгІЩњГЩCu(OH)ClЕФРызгЗНГЬЪНЮЊ______ЁЃ
гыбЮЫсЗДгІЩњГЩCu(OH)ClЕФРызгЗНГЬЪНЮЊ______ЁЃ
(2)ВНжшЂєашПижЦpHЮЊ1~2,80 ЁцЯТНјаа,КЯЪЪЕФМгШШЗНЪНЪЧ______ЁЃ
(3)ВНжшЂѕЕФОпЬхВНжшЪЧеєЗЂХЈЫѕЁЂ______ЁЂ____ЁЃ
(4)ВНжшЂідкЯТСазАжУ(МаГжМАМгШШзАжУвбЪЁТд)жаНјааЁЃ

ЂйзАжУaжаЪЂзАХЈСђЫсЕФвЧЦїЕФУћГЦЪЧ____,дВЕзЩеЦПжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ____ЁЃ
ЂкгУзАжУdжаЕФШмвКЯДЕгжЦЕУЕФCuIЕФФПЕФЪЧ____,ШЛКѓдйгУЮоЫЎввДМЯДЕгЕФФПЕФЪЧ____ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПаПвјЕчГиФмСПДѓЁЂЕчбЙЦНЮШЃЌЙуЗКгУгкЕчзгЪжБэЁЂееЯрЛњЁЂМЦЫуЦїКЭЦфЫћЮЂаЭЕчзгвЧЦїЁЃЕчНтжЪШмвКЪЧKOHШмвКЃЌЕчГизмЗДгІЮЊZnЃЋAg2O=ZnOЃЋ2AgЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉИУЕчГиЕФе§МЋВФСЯЪЧ________ЃЛЕчГиЙЄзїЪБЃЌбєРызгЯђ________ЃЈЬюЁАе§МЋЁБЛђЁАИКМЋЁБЃЉвЦЖЏЃЛИКМЋЕФЗДгІЪНЮЊ__________ЁЃ
ЃЈ2ЃЉЂйЕчМЋВФСЯаППЩгЩЩСаППѓдкПеЦјжаьбЩеГЩбѕЛЏаПЃЌШЛКѓгУЬМЛЙдРДжЦШЁЃЌЛЏбЇЗДгІЗНГЬЪНЮЊZnOЃЋC![]() ZnЃЋCOЁќЃЌДЫЗЈЮЊ_____ЁЃ
ZnЃЋCOЁќЃЌДЫЗЈЮЊ_____ЁЃ
A ЕчНтЗЈЁЁB ШШЛЙдЗЈЁЁC ШШЗжНтЗЈ
ЃЈ3ЃЉПЩгУЪЏФЋзїЕчМЋЕчНтЬсДПЧтбѕЛЏМиЕчНтвКЁЃЕчНтГиФкЕФбєРызгНЛЛЛФЄжЛдЪаэбєРызгЭЈЙ§ЃЌЦфЙЄзїдРэШчЭМЫљЪОЁЃ
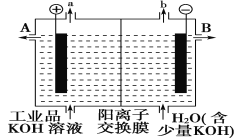
ЂйИУЕчНтГиЕФбєМЋЃЌвѕМЋЗДгІЪНЮЊбєМЋЃК_________вѕМЋЃК________
ЂкГ§ШЅдгжЪКѓЕФЧтбѕЛЏМиШмвКДгГіПк________ЃЈЬюЁАAЁБЛђЁАBЁБЃЉЕМГіЁЃ
ЂлдкЯрЭЌЬѕМўЯТЃЌaДІгыbДІВњЩњЕФЦјЬхЬхЛ§БШЮЊ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЧтЦјЛЙдЪЏИрЕФЙ§ГЬЛсЗЂЩњЖрИіЗДгІ,ЦфжажївЊЗДгІЮЊЂёЁЂЂђЁЂЂѓ,ЕБCaSO4(s)гыH2(g)ЕФЦ№ЪМЮяжЪЕФСПжЎБШЮЊ1ЁУ1ЪБ,ВтЕУЦНКтЪБЮяжЪЕФСПШчЭМЫљЪОЁЃ
Ђё:CaSO4(s)+H2(g)![]() CaO(s)+H2O(g)+SO2(g)ЁЁІЄH1>0
CaO(s)+H2O(g)+SO2(g)ЁЁІЄH1>0
Ђђ:CaSO4(s)+4H2(g)![]() CaS(s)+4H2O(g)ЁЁІЄH2<0
CaS(s)+4H2O(g)ЁЁІЄH2<0
Ђѓ:3CaSO4(s)+CaS(s)![]() 4CaO(s)+4SO2(g)ЁЁІЄH3
4CaO(s)+4SO2(g)ЁЁІЄH3
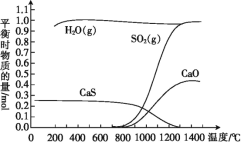
ЛиД№ЯТСаЮЪЬт:
(1)100 Ёц~700 ЁцжївЊЗЂЩњЗДгІ____(ЬюЁАЂёЁБЁАЂђЁБЛђЁАЂѓЁБ)ЁЃ
(2)ІЄH3=____(гУКЌІЄH1ЁЂІЄH2ЕФДњЪ§ЪНБэЪО),ІЄH3____(ЬюЁА>ЁБЛђЁА<ЁБ)0,ЗДгІЂѓДяЕНЦНКтКѓ,Щ§ИпЮТЖШ,ЦНКт____(ЬюЁАе§ЯђЁБЛђЁАФцЯђЁБ)вЦЖЏЁЃ
(3)ЯђФГКуЮТКуШнУмБеШнЦїжаМгШы0.3 mol CaSO4КЭ0.1 mol CaS,ИпЮТЯТШєжЛЗЂЩњЗДгІЂѓ,ДяЕНЦНКтЪБЯђШнЦїжадйГфШыЩйСПSO2,ЯТСаЫЕЗЈе§ШЗЕФЪЧ____(ЬюзжФИ)ЁЃ
A.жиаТЦНКтЪБ,ШнЦїФкЦјЬхзмбЙЧПдіДѓ
B.жиаТЦНКтЪБ,CaOЕФСПМѕЩй
C.жиаТЦНКтЪБ,SO2ЕФХЈЖШВЛБф
D.CaSO4(s)ЁЂCaS(s)ЕФжЪСПВЛБф
(4)ЦфЫћЬѕМўвЛЖЈЪБ,H2ЕФСїСПгыЪЏИрЕФЗжНтТЪКЭЭбСђТЪЙиЯЕШчЭМЫљЪОЁЃдкЦјЬхСїСПИпгк242 mLЁЄmin-1ЪБ,ЗжНтТЪКЭЭбСђТЪОљНЕЕЭ,ПЩФмЕФдвђЪЧ____(жЛаДвЛЬѕ)ЁЃ
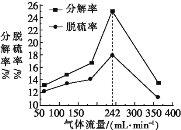
(5)вбжЊЦфжаИБЗДгІжЎвЛЮЊ2CaSO4(s)![]() 2CaO(s)+2SO2(g)+O2(g),дк1625 KЪБ,ЦНКтГЃЪ§Kp=1.45ЁС10-5 atm3(atmБэЪОДѓЦјбЙ,
2CaO(s)+2SO2(g)+O2(g),дк1625 KЪБ,ЦНКтГЃЪ§Kp=1.45ЁС10-5 atm3(atmБэЪОДѓЦјбЙ,![]() Ёж3.81)ЁЃИУЮТЖШЯТ,ЗДгІCaO(s)+SO2(g)+
Ёж3.81)ЁЃИУЮТЖШЯТ,ЗДгІCaO(s)+SO2(g)+![]() O2(g)
O2(g) ![]() CaSO4(s)ЕФK'p=____(БЃСєећЪ§ВПЗж)ЁЃ
CaSO4(s)ЕФK'p=____(БЃСєећЪ§ВПЗж)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПpHЃН1ЕФСНжжЫсШмвКAЁЂBИї1 mLЃЌЗжБ№МгЫЎЯЁЪЭЕН1000mLЃЌЦфpHгыШмвКЬхЛ§VЕФЙиЯЕШчЭМЫљЪОЃЌдђЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ

A.СНжжЫсШмвКЕФЮяжЪЕФСПХЈЖШвЛЖЈЯрЕШB.ЯЁЪЭКѓAЫсШмвКЕФЫсадБШBЫсШмвКШѕ
C.ШєaЃН4ЃЌдђAЪЧЧПЫсЃЌBЪЧШѕЫсD.Шє1ЃМaЃМ4ЃЌдђAЁЂBЖМЪЧШѕЫс
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПН№ЪєюбдкКНЬьЁЂЧБКЃКЭвНСЦЗНУцгІгУЙуЗКЁЃвдюбЬњПѓ[жївЊГЩЗжЮЊюбЫсбЧЬњ(FeTiO3),КЌЩйСПFe2O3]ЮЊдСЯжЦБИюбЕФЙЄвеСїГЬШчЭМЫљЪОЁЃ
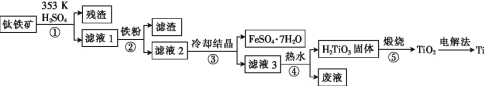
(1)ВНжшЂкЁЂЂлЁЂЂмжа,ОљашНјааЕФВйзїЪЧ____(ЬюВйзїУћГЦ)ЁЃ
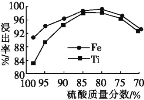
(2)ТЫвК1жаюбдЊЫивдTiO2+аЮЪНДцдк,ВНжшЂйжаЩњГЩTiO2+ЕФЛЏбЇЗНГЬЪНЮЊ____,СђЫсжЪСПЗжЪ§ЖдюбЁЂЬњНўГіТЪЕФгАЯьШчЭМЫљЪО,ОнДЫХаЖЯ,ЫсНўЪБЫљМгСђЫсЕФжЪСПЗжЪ§гІЮЊ____(ЬюЗЖЮЇ)ЁЃ
(3)ЧыНсКЯРызгЗНГЬЪННтЪЭВНжшЂмжаМгШШЫЎЕФдвђ:____ЁЃ
(4)ЕчНтЗЈжЦБИTiЕФзАжУЪЧвдЪЏФЋЮЊбєМЋ,TiO2ЮЊвѕМЋ,ШлШкCaOЮЊЕчНтжЪЁЃTiдк___(ЬюЁАбєМЋЁБЛђЁАвѕМЋЁБ)ЩњГЩ,____(ЬюЁАФмЁБЛђЁАВЛФмЁБ)НЋШлШкCaOЛЛГЩЪЏЛвШщЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com