
科目: 来源: 题型:
【题目】某温度时,VIA元素单质与H2反应生成气态H2X的热化学方程式如下:
1/2O2(g) + H2(g) =H2O(g) ΔH = -242 kJ·mol-1
S(g) + H2(g) =H2S(g) ΔH = -20 kJ·mol-1
Se(g) + H2(g)![]() H2Se(g) ΔH = +81 kJ·mol-1
H2Se(g) ΔH = +81 kJ·mol-1
下列说法正确的是( )
A. 稳定性:H2O > H2S > H2Se
B. 降温有利于Se与H2反应生成H2Se
C. O2(g) + 2H2S(g)=2H2O(g) + 2S(g) ΔH = 444 kJ·mol-1
D. 随着核电荷数的增加,VIA族元素单质与H2的化合反应越容易发生
查看答案和解析>>
科目: 来源: 题型:
【题目】(14分)氟化钙为无色结晶体或白色粉末,难溶于水,主要用于冶金、化工、建材三大行业,目前我国利用氟硅酸(H2SiF6)生产氟化钙有多种方案,氨法碳酸钙法是制备氟化钙的常见方案,其工艺流程如图所示。请回答下列问题:
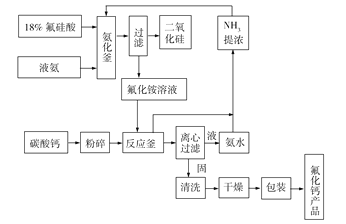
(1)萤石含有较多的氟化钙,在炼钢过程中,要加入少量的萤石,推测萤石的主要作用是________(填字母)。
A.还原剂 B.助熔剂 C.升温剂 D.增碳剂
(2)请写出氨化釜中反应的化学方程式:_______________________________。
(3)反应釜中产生两种气体,溶于水后一种显酸性,一种显碱性,请写出反应釜中反应的离子方程式:__________________________________。
(4)从经济效益和环境效益上分析,本工艺为了节约资源,经过必要的处理可循环利用的物质是________。
(5)本工艺用CaCO3作原料的优点为___________________________________(任写两条);查文献可知3Ca(OH)2+H2SiF6![]() 3CaF2+SiO2+4H2O,请叙述此方法制备CaF2的最大难点是______________。
3CaF2+SiO2+4H2O,请叙述此方法制备CaF2的最大难点是______________。
(6)以1 t 18%氟硅酸为原料,利用上述氨法碳酸钙法制备CaF2,最后洗涤、干燥、称量得到0.25 t 纯净的CaF2,请计算CaF2的产率为__________%(保留整数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z是位于不同周期的主族元素、原子序数依次增大且均小于18,Z为金属元素,X、Y、Z的最外层电子数之和为8,X、Y、Z组成的物质可发生反应:ZX2+2YX3![]() Z(YX2)2+2X2。下列有关说法正确的是
Z(YX2)2+2X2。下列有关说法正确的是
A.1 mol ZX2发生上述反应转移电子的物质的量为4 mol
B.YX3与Y2X4中Y元素的化合价相同
C.上述反应中的离子化合物的所有元素原子的最外层都满足8电子稳定结构
D.Y元素在同周期和同主族元素的最高价含氧酸中酸性最强
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应A2(g)+B(g)=2AB(g)的能量交化如图所示。下列有关叙述不正确的是

A.AB(g)的键能为b kJ·mol-1
B.反应热△H=+(a-b)kJ·mol-1
C.该反应中反应物的总能量低于生成物的总能量
D.断裂1 mol A-A键和1 mol B-B键,吸收a kJ能量
查看答案和解析>>
科目: 来源: 题型:
【题目】过渡金属硫化物作为一种新兴的具有电化学性能的电极材料,在不同的领域引起了研究者的兴趣,含有过渡金属离子废液的回收再利用有了广阔的前景,下面为S2与溶液中金属离子的沉淀溶解平衡关系图,若向含有等浓度Cu2+、Cd2+、Zn2+、Co2+、Fe2+的废液中加入含硫的沉淀剂,则下列说法错误的是
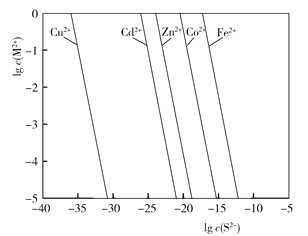
A.由图可知溶液中金属离子沉淀先后顺序为Cu2+、Cd2+、Zn2+、Co2+、Fe2+
B.控制S2浓度可以实现铜离子与其他金属离子的分离
C.因Na2S、ZnS来源广、价格便宜,故常作为沉铜的沉淀剂
D.向ZnS中加入Cu2+的离子方程式为:S2+Cu2+![]() CuS↓
CuS↓
查看答案和解析>>
科目: 来源: 题型:
【题目】在环境和能源备受关注的今天,开发清洁、可再生新能源已成为世界各国政府的国家战略,科学家发现产电细菌后,微生物燃料电池(MFC)为可再生能源的开发和难降解废物的处理提供了一条新途径。微生物燃料电池(MFC)示意图如下所示(假设有机物为乙酸盐)。下列说法错误的是
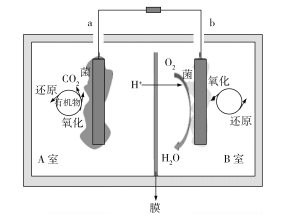
A.A室菌为厌氧菌,B室菌为好氧菌
B.A室的电极反应式为CH3COO8e +2H2O![]() 2CO2 +8H+
2CO2 +8H+
C.微生物燃料电池(MFC)电流的流向为b→a
D.电池总反应式为CH3COO+2O2+H+![]() 2CO2 +2H2O
2CO2 +2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】丙烯是石油化学工业的重要基础原料,我国科学家利用甲醇转化制丙烯反应过程如下:
3CH3OH +H3AlO6 →3![]() +
+![]() +3H2O
+3H2O
3![]() +
+![]() →H3AlO6 + 3C○↑↓H2
→H3AlO6 + 3C○↑↓H2
3C○↑↓H2 → CH2=CHCH3
下列叙述错误的是
A.甲醇转化制丙烯反应的方程式为3CH3OH→CH2=CHCH3+3H2O
B.甲醇转化制丙烯反应的过程中H3AlO6作催化剂
C.1.4 g C○↑↓H2所含的电子的物质的量为1 mol
D.甲基碳正离子![]() 的电子式为
的电子式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】固氮作用有3种途径:生物固氮、人工固氮和大气固氮。如表列举了不同温度下大气固氮的部分平衡常数K值。![]() 时,向
时,向![]() 的恒容密闭容器中充入
的恒容密闭容器中充入![]() 和
和![]() ,10s时反应达到平衡。
,10s时反应达到平衡。
反应 | 大气固氮 | |
温度/℃ | 27 | 2260 |
K |
| 1 |
下列说法正确的是( )
A.大气固氮反应属于放热反应
B.10 s末,![]() 的转化率约为
的转化率约为![]()
C.10 s内,用![]() 表示的平均反应速率为
表示的平均反应速率为![]()
D.10 s末,再向容器中充入![]() mol
mol ![]() 和
和![]() mol
mol ![]() ,
,![]() 的平衡转化率不变
的平衡转化率不变
查看答案和解析>>
科目: 来源: 题型:
【题目】G是良好的生物医药缓释材料,其合成路线:
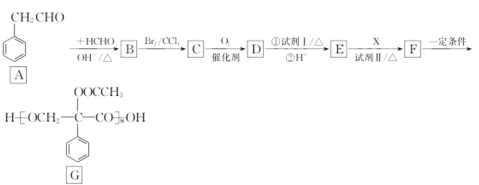
已知: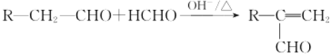
回答下列问题:
(1)A的化学名称为_______;B中官能团的名称为_________。
(2)由F生成G的反应类型为________。
(3)无机试剂I 、II分别为________、__________。
(4)物质X的结构简式是__________。
(5)写出D与试剂I的化学反应方程式:_____________________。
(6)Y是比D多1个碳原子的同系物,写出两种符合下列条件的Y的结构简式:________。
①能与饱和Na2CO3溶液反应放出气体;②苯环上有3个侧链,核磁共振氢谱显示有4种不同化学环境的氢,且峰面积比为6:2:1:1。
(7)参照以上合成路线,写出以甲醛、乙醛和乙二醇为主要原料合成功能高分子材料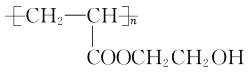 的路线:_______________________________(其他无机试剂任用)。
的路线:_______________________________(其他无机试剂任用)。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚甲基蓝(Methylnene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White),亚甲基蓝的结构简式:
著名的蓝瓶子实验操作步骤如下:
①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色;
②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。
试回答下列问题:

(1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是_________(填“A”或“B”);
(2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色_________(填“能”或“不能”);若塞紧锥形瓶塞并打开a、b通入足量氧气,溶液能否由无色变为蓝色_________(填“能”或“不能”);
(3)上述转化过程中,葡萄糖的作用是_________,亚甲基蓝的作用是_________;
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有_____;
(5)该实验中③、④操作能否无限次重复进行_________(填“能”或“不能”),理由是 _____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com