
科目: 来源: 题型:
【题目】已知:A、B、F是家庭中常见的有机物,A和B碳原子数相等,E是石油化工发展水平的标志,F是一种常见的高分子材料。下面是几种物质的转化关系图:
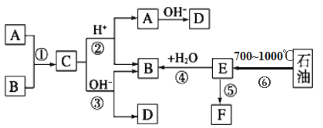
完成下列填空:
(1)操作⑥的名称为:_____________________________________,上述反应中属于取代反应的是___________(填序号)
(2)写出比B多两个碳原子,且不能发生非燃烧性氧化反应的同系物的结构简式:___。
(3)写出反应③所用的碱液为氢氧化钠溶液,写出反应③的化学方程式____________。
(4)写出F的名称________________________,反应⑤的反应类型为_________。
(5)写出检验B的催化氧化产物的化学方程式____________,实验现象是______。
(6)写出两个既能发生银镜反应又能发生酯化反应的C的同分异构体结构简式。
________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图),用环己醇制环己烯。
已知:![]()
密度( | 熔点℃ | 沸点℃ | 溶解性 | |
环己醇 | 0.096 | 25 | 161 | 能溶于水 |
环己烯 | 0.081 | -103 | 83 | 难溶于水 |
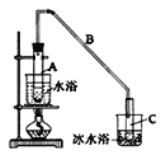
制备粗品:
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
(1)A中瓷片的作用是______,导管B除了导气外还具有的作用是______;
(2)试管C置于冰水浴中的目的是__________________________。
制备精品:
(3)环己烯粗品中含有环己醇和少量酸性杂质等。加入少量食盐水,振荡、静置、分层,环己烯在_______层(填“上”或“下”),分液后用_________(填入编号)洗涤;
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
(4)再将环己烯按图2装置蒸馏,冷却水从_______(填f或g)口进入,蒸馏时要加入生石灰,目的是______________。收集产品时,温度应控制在_____左右。
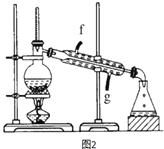
(5)以下区分环己烯精品与粗品的方法,合理的是_________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
若用上述装置制备乙酸乙酯,回答下列问题。
(6)用分液漏斗提纯试管C中的乙酸乙酯,在操作时要注意振荡洗涤后,静置分液前必须放气,具体操作方法是__________(填编号)
a.将仪器正放在架子或铁圈上打开上部塞子
b.将仪器正放在架子或铁圈上打开活塞
c.用手心抵住仪器上部塞子倒置后打开活塞
d.将该仪器平放在实验台上打开活塞
(7)所制得的酯应从该分液漏斗的__________(填编号)
a.下部流出 b.上口倒出 c.都可以
(8)在提纯乙酸乙酯时,为什么要使用饱和碳酸钠溶液,而不用NaOH溶液洗涤?
______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】交联聚合物K合成路线如下(图中表示链延长)
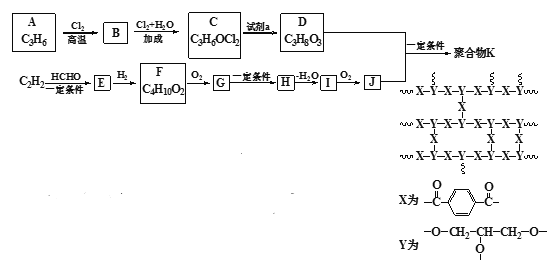
已知: ;
;

(1)按官能团分类,A的类别是__________。
(2)A→B的反应类型是________________。
(3)C可能的结构简式是__________。
(4)C→D所需的试剂a是__________。
(5)C2H2生成E的方程式是__________。
(6)G→H的方程式是__________。
(7)含有苯环,且与I互为同分异构体的酯有_____种。写出其中的一种结构简式___________
查看答案和解析>>
科目: 来源: 题型:
【题目】苯乙烯(![]() )是重要的化工原料,根据要求填写下列空格。
)是重要的化工原料,根据要求填写下列空格。
(1)苯乙烯中含官能团的名称是_________________,苯乙烯合成聚苯乙烯的化学方程式是__________________________________
(2)取10.4g苯乙烯与足量氢气反应,消耗标况下氢气的体积为___________L,生成产物的结构简式为______________,其一氯代物共有___________种。
(3)下列属于苯乙烯的性质有___________
A.能溶于水 B.能发生氧化反应
C.能发生缩聚反应 D.常温常压下为气体
(4)苯乙烯属于___________
A.环烷烃 B.不饱和烃 C.烯烃 D.芳香烃
(5)苯乙烯和氯气加成产物H,写出H与氢氧化钠溶液共热的化学方程式___________________________。其反应类型是_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】氧和硫属于同主族元素,其单质和化合物在生产生活中用途很广。
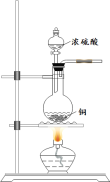
SO2可用于防腐剂、消毒剂,也是一种重要的冷冻介质。实验室可用如图所示装置制备SO2,并用纯净SO2进行相关实验。
(1)上述方法制备的SO2,往往因伴有硫酸小液滴而呈白雾状。除去白雾可在制备装置后连接除杂装置,请画出除杂装置并标明装置中的试剂___________。

(2)将SO2通入0.1mol/L Ba(NO3)2溶液得到白色沉淀,该反应的离子方程式为_______。
分别用煮沸和未煮沸过的蒸馏水配制Ba(NO3)2和BaCl2溶液,进行如下实验:
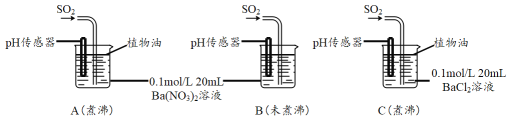
(3)实验C中,没有观察到白色沉淀,但pH传感器显示溶液呈酸性,用化学用语表示其原因______________________________。
(4)实验B中出现白色沉淀比实验A快很多。由此得出的结论是_________________。
(5)测定水中溶解O2的量,常用的方法是:
i.量取a mL水样,迅速加入足量MnSO4溶液及含有NaOH的KI溶液,立即塞好塞子,振荡使反应均匀。
ii.开塞,迅速加入适量的硫酸,此时有I2生成。
iii.向ii所得溶液中滴加2滴淀粉溶液为指示剂,用b mol/LNa2S2O3标准溶液滴定至终点共消耗了Na2S2O3溶液V mL。
有关反应方程式为:2Mn2+ + O2+ 4OH- = 2MnO(OH)2(反应很快)
MnO(OH)2 + 2I- + 4H+= Mn2+ + I2 + 3H2O
I2 + 2S2O32- = 2I- + S4O62-
①水中溶解 O2的量(以mg/L为单位)为___________________。
②判断达到滴定终点的实验依据为 __________。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeSO4溶液放置在空气中容易变质,因此为了方便使用Fe2+,实验室中常保存硫酸亚铁铵晶体[俗称“摩尔盐”,化学式为(NH4)2Fe(SO4)26H2O],它比绿矾或绿矾溶液更稳定。
I.某兴趣小组设计实验制备硫酸亚铁铵晶体。
本实验中,配制溶液以及后续使用到的蒸馏水都经过煮沸、冷却后再使用。向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过操作_______、冷却结晶、过滤、洗涤和干燥后得到一种浅蓝绿色的晶体。
II.实验探究影响溶液中Fe2+稳定性的因素
(1)配制0.8 mol/L的FeSO4溶液(pH=4.5)和0.8 mol/L的(NH4)2Fe(SO4)2溶液(pH=4.0),各取2 mL上述溶液于两支试管中,刚开始两种溶液都是浅绿色,分别同时滴加2滴0.01mol/L的KSCN溶液,15min后观察可见:(NH4)2Fe(SO4)2溶液仍然为浅绿色透明澄清溶液,FeSO4溶液则出现淡黄色浑浊。
(资料1)
沉淀 | Fe(OH)2 | Fe(OH)3 |
开始沉淀 pH | 7.6 | 2.7 |
完全沉淀 pH | 9.6 | 3.7 |
①请用离子方程式解释FeSO4溶液产生淡黄色浑浊的原因___________________。
②讨论影响Fe2+稳定性的因素,小组同学提出以下3种假设:
假设1:其他条件相同时,NH4+的存在使(NH4)2Fe(SO4)2溶液中Fe2+稳定性较好。
假设2:其他条件相同时,在一定 pH范围内,溶液 pH越小Fe2+稳定性越好。
假设3:__________________________________________________。
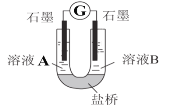
(2)小组同学用如图装置(G为灵敏电流计),滴入适量的硫酸溶液分别控制溶液A(0.2 mol/L NaCl)和溶液B(0.1mol/L FeSO4)为不同的 pH,观察记录电流计读数,对假设2进行实验研究,实验结果如下表所示。
序号 | A 0.2mol/LNaCl | B 0.1mol/LFeSO4 | 电流计读数 |
实验1 | pH=1 | pH=5 | 8.4 |
实验2 | pH=1 | pH=1 | 6.5 |
实验3 | pH=6 | pH=5 | 7.8 |
实验4 | pH=6 | pH=1 | 5.5 |
(资料2)原电池装置中,其他条件相同时,负极反应物的还原性越强或正极反应物的氧化性越强,该原电池的电流越大。
(资料3)常温下,0.1mol/LpH=1的FeSO4溶液比pH=5的FeSO4溶液稳定性更好。
根据以上实验结果和资料信息,经小组讨论可以得出以下结论:
①U型管中左池的电极反应式_________________。
②对比实验1和2(或3和4),在一定pH范围内,可得出的结论为______ 。
③对比实验_____和_____ 还可得出在一定 pH范围内,溶液酸碱性变化是对O2氧化性强弱的影响因素。
④对(资料3)实验事实的解释为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组中两种物质无论以何种比例混合,只要混合的总物质的量一定,则完全燃烧时生成水的质量和消耗O2的质量均不变的是( )
A.C3H6、C3H8OB.C2H4、C2H6O
C.CH4O、C2H4O3D.C2H2、C6H6
查看答案和解析>>
科目: 来源: 题型:
【题目】工业排放物可能对环境和人体健康产生危害,必须经过处理才可排放。根据题意回答下列问题。
Ⅰ.处理含SO2、NO的烟气
在323 K温度下,向盛有NaClO2溶液的鼓泡反应器中通入含有SO2和NO的烟气。
(1)写出NaClO2溶液脱硝过程中反应的离子方程式___________________ 。
(2)由实验测得,脱硫反应速率大于脱硝反应速率,原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(3)采用NaClO、Ca(ClO) 2替代NaClO2,也能较好的除去SO2。从化学平衡原理分析,Ca(ClO) 2相比NaClO具有的优点是___________________。
Ⅱ.处理含H2S的烟气
生物脱H2S原理为:
H2S(g) + Fe2(SO4)3(aq) = S(s) + 2FeSO4(aq) + H2SO4(aq) ΔH1
4FeSO4(aq) + O2(g) + 2H2SO4(aq) ![]() 2Fe2(SO4)3(aq) + 2H2O(l) ΔH2
2Fe2(SO4)3(aq) + 2H2O(l) ΔH2
(1)反应2H2S(g) + O2 (g) = 2S(s) + 2H2O(l) 的ΔH3=___________________。
(2)若反应温度过高,反应速率下降(如图),其原因是______________。

Ⅲ.处理污水的化学方法有许多,混凝法、氧化还原法、中和法、电解法等。处理含Na2SO4的废水常用三室式电渗析法,原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。

(1)负极反应式为___________________。
(2)当电路中通过1![]() 电子的电量时,会有_________
电子的电量时,会有_________![]() 的O2生成。
的O2生成。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组利用如图装置进行乙醇的催化氧化实验制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:
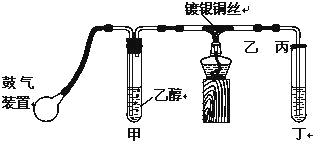
(1)甲装置常常浸在7080℃的水浴中,目的是___________
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。乙醇的催化氧化反应是__________反应(填“放热”或“吸热”),该反应的化学方程式为________
(3)该小组将丁中收集到的产物继续做实验探究:
①在试管中加入2毫升10%的_____溶液,在滴加四到五滴2%的_______溶液,配制成氢氧化铜悬浊液。然后加入丁中的产物,在酒精灯上加热,可以看到_________
②写出丁种物质与新制氢氧化铜反应的化学方程式___________
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以电石主要成分是CaC2)为原料制备乙炔,装置如图所示:
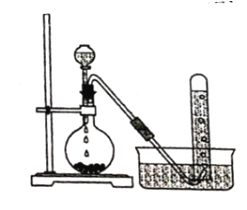
(1)实验室制取乙炔的化学方程式为 ______________。
(2)为除去乙炔中混有的少量硫化氢杂质,可将气体通过 ____________ (选填编号)。
a.酸性KMnO4溶液 b.CCl4 c.NaOH溶液
(3)氧炔焰是乙炔在氧气中燃烧的高温火焰,可用于______________________ 。
(4)乙炔在一定条件下三聚得到CH2=CHC≡CCH=CH2,写出与该三聚物具有相同化学式且不能使溴的CCl4溶液褪色和酸性高锰酸钾溶液褪色的物质的结构简式_________
(5)乙炔聚合得到聚乙炔,聚乙炔__________导电(选填“能”或“不能”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com