
科目: 来源: 题型:
【题目】有机物A的结构简式如图所示,下列有关该物质的说法不正确的是
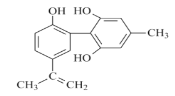
A.A分子中的所有碳原子可能共平面
B.1mol A与碳酸钠溶液反应,最少消耗1.5mol Na2CO3
C.向A中滴入酸性KMnO4溶液,紫色褪去,不能证明A的结构中存存碳碳双键
D.1mol A分别与浓溴水和H2反应,最多消耗的Br2和H2的物质的量分别为4mol、7mol
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。下列说法不正确的是
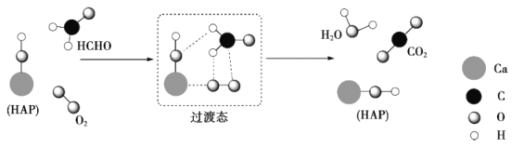
A.HAP能提高HCHO与O2的反应速率
B.根据图示信息,CO2分子中的氧原子全部来自O2
C.HCHO在反应过程中,有C-H键发生断裂
D.该反应可表示为: HCHO+O2![]() CO2+H2O
CO2+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列“烧杯中的物质”和“向烧杯中分别加入的试剂”不能完成“实验目的”的是
① ②
② 
实验目的 | 烧杯中的物质 | 向烧杯中分别加入的试剂 | |
A | 醋酸的酸性强于苯酚 | ①醋酸 ②苯酚溶液 | 碳酸氢钠溶液 |
B | 羟基对苯环的活性有影响 | ①苯 ②苯酚溶液 | 饱和溴水 |
C | 甲基对苯环的活性有影响 | ①苯 ②甲苯 | 酸性高锰酸钾溶液 |
D | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 | ①水 ②乙醇 | 金属钠 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】反应N2(g)+O2(g)=2NO(g)的能量变化如图所示:
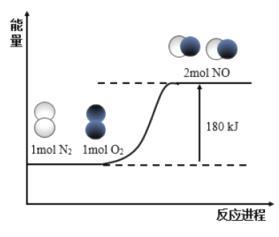
已知:断开1mol N2(g)中化学键需吸收946kJ能量,断开1mol O2(g)中化学键需吸收498kJ能量。下列说法正确的是
A.断开1mol NO(g)中化学键需要吸收632kJ能量
B.NO(g)=![]() N2(g)+
N2(g)+![]() O2(g) H=+90kJ/mol
O2(g) H=+90kJ/mol
C.N2(g)+O2(g)=2NO(g) H=-180kJ/mol
D.形成1mol NO(g)中化学键时释放90kJ能量
查看答案和解析>>
科目: 来源: 题型:
【题目】ClO2是一种极易溶于水且几乎不与冷水反应的黄绿色气体(沸点11℃),实验室制备纯净ClO2溶液的装置如图所示:

已知下列反应:NaClO3+HCl→NaCl+ClO2+Cl2+H2O;NaClO2+HCl→NaCl+ClO2+H2O;NaClO2+Cl2→NaCl+ClO2(均未配平)。下列说法正确的是
A.a中通入的N2可用CO2或SO2代替B.b中NaClO2可用饱和食盐水代替
C.c中广口瓶最好放在冰水浴中冷却D.d中吸收尾气后只生成一种溶质
查看答案和解析>>
科目: 来源: 题型:
【题目】脱氢醋酸钠是FAO和WHO认可的一种安全型食品防霉、防腐保鲜剂,它是脱氢醋酸的钠盐。脱氢醋酸的一种制备方法如图:
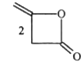 (a双乙烯酮)
(a双乙烯酮)![]()
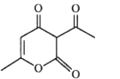 (b脱氢醋酸)
(b脱氢醋酸)
下列说法错误的是
A.a分子中所有原子处于同一平面B.a.b均能使酸性KMnO4溶液褪色
C.a、b均能与NaOH溶液发生反应D.b与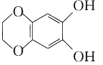 互为同分异构体
互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组按如下实验过程(固定、加热及盛接仪器略)证明了海带中存在碘元素:

下列说法不正确的是
A.步骤①需要将干海带放入坩埚中灼烧
B.步骤②反应的离子方程式为:2I-+2H++H2O2=I2+2H2O
C.步骤③操作后,观察到试管中溶液变为蓝色,可以说明海带中含有碘元素
D.若步骤③加入的试剂是CCl4,振荡、静置后,液体分层,上层紫色,下层无色
查看答案和解析>>
科目: 来源: 题型:
【题目】一种以NH4Cl酸性蚀铜废液[含NH4Cl、Cu(NH3)4Cl2、CuCl、CuSO4及盐酸等]为原料制备CuCl并回收Cu(OH)2的工艺流程如图:

回答下列问题:
(1)“反应1”中,NaCl、Cu、CuSO4反应的离子方程式为____;生产中常将“过滤1”的滤渣返回到“反应1”中,其目的是______。
(2)“水解”步骤中,加入大量水稀释即可析出CuCl,原因是 ____________(结合离子方程式,从平衡角度分析)。
(3)湿的CuCl在空气中易被氧化为Cu2(OH)3Cl,该反应的化学方程式为____;“洗涤”时稀盐酸和乙醇洗涤的目的是______________ 。
(4)“反应2”需加入的试剂X是 ___;“吹脱”出来的NH3可用于生产碳铵化肥,主要反应的化学方程式为 ______ 。
(5)测定产品中CuCl质量分数的步骤如下:称取ag产品,加入稍过量的FeCl3溶液,待溶解后用邻非罗啉作指示剂,立刻用c mol/L的Ce(SO4)2标准溶液滴定到终点,消耗标准溶液VmL。则产品中CuCl的质量分数为____(已知滴定反应为 Ce4++Fe2+=Ce3++Fe3+,列出计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物M是一种有机高分子,其合成路线如下:
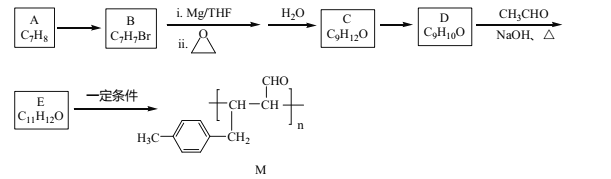
已知:①R-Br![]()
![]() R-CH2CH2OH
R-CH2CH2OH
②R-CHO![]() R-CH=CHCHO
R-CH=CHCHO
回答下列问题:
(1)A→B的反应试剂及条件是_______________。
(2)C→D的反应类型是_______________。
(3)化合物C的名称是_____________。
(4)D与银氨溶液反应的化学方程式为__________。
(5)E中官能团的名称是_______。
(6)化合物X(C10H10O)是E的同系物,且苯环上只有两个取代基,则X的同分异构体有______种,其中核磁共振氢谱为六组峰,峰面积之比为3:2:2:1:1:1的结构简式为________。
(7)设计由CH3Cl、环氧乙烷和乙醛制备CH3CH2CH=CHCHO的合成路线________(其他试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组为了验证SO2的还原性并测定产生SO2的质量,组装了下图装置。回答下列问题:
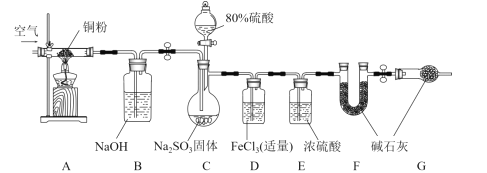
(1)C中发生反应的化学方程式是________,B装置的名称是_________,关于该套装置说法正确的是_________(填标号)。
a 组装仪器、加入药品后检查气密性 b 实验开始和最后时均需要通入空气
c 利用A、B装置是为了减小实验误差 d F、G中的碱石灰可以换为无水CaCl2
(2)甲同学认为很快可以看到D装置的现象,他的依据是_________(用离子方程式表示)。乙同学做实验时发现和甲同学预测的现象不一样,先出现棕红色,经过一段时间后变为浅绿色。于是查阅资料发现反应分为两步:
第一步:![]() (快反应)
(快反应)
第二步:![]() (慢反应)
(慢反应)
如果需要验证第一步反应是快反应,可以事先在D装置中滴加数滴_________试剂,相应的实验现象是________。
(3)学习小组通过实验后D和F装置中的数据来计算SO2的质量。D中加入足量的BaCl2溶液充分反应,经过________操作,测得沉淀为m1g,F的质量差为m2g,C中产生SO2的体积(标准状况下)为_________L。该实验的设计中,仍然存在系统误差的可能原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com