
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
10°¢œ÷”–H2 SO4°¢BaCl2 °¢NaOH°¢Na2CO3°¢MgSO4°¢Ca(OH)2ŒÂ÷÷»Ð“∫∫Õ“ª÷÷∆¯ÃÂCO2£¨”–Õº1À˘ 浃œýª•∑¥”¶πÿœµ£¨Õº÷–√øÃı¡¨œþ±Ì æ¡Ω∂ÀµƒŒÔ÷
°¢NaOH°¢Na2CO3°¢MgSO4°¢Ca(OH)2ŒÂ÷÷»Ð“∫∫Õ“ª÷÷∆¯ÃÂCO2£¨”–Õº1À˘ 浃œýª•∑¥”¶πÿœµ£¨Õº÷–√øÃı¡¨œþ±Ì æ¡Ω∂ÀµƒŒÔ÷  ø…“‘∑¢…˙ªØ—ß∑¥”¶£¨ ‘Ω´À¸√«µƒªØ—ß ΩÃÓ»ÎÕº1÷–œý”¶µƒ¡˘∏ˆ∑ΩøÚ÷–°£
ø…“‘∑¢…˙ªØ—ß∑¥”¶£¨ ‘Ω´À¸√«µƒªØ—ß ΩÃÓ»ÎÕº1÷–œý”¶µƒ¡˘∏ˆ∑ΩøÚ÷–°£
 °°
°°
[Ω‚Œˆ]ø…œ»’“≥ˆŒÔ÷ º‰µƒ»´≤øœýª•∑¥”¶πÿœµ£¨»ÁÕº2°£
9°¢”–A£¨B£¨C£¨D£¨EŒÂ∆ø ß»•±Í«©µƒŒÞ…´»Ð“∫£¨“—÷™À¸√«∑÷± «NaOH°¢HCl°¢MgSO4°¢BaCl2∫ÕK2CO3÷–µƒ“ª÷÷°£Œ™¡Àº¯±£¨∏˜»°…Ÿ¡ø»Ð“∫¡Ω¡ΩªÏ∫œ£¨ µ—ÈΩ·π˚»Áœ¬±Ì“ªÀ˘ æ°£±Ì÷–°∞°˝°±±Ì æ…˙≥…ƒ—»ÐªÚŒ¢»Ðµƒ≥¡µÌ£ª°∞°¸°±±Ì æ”–∆¯ÃÂ≤˙…˙£ª°∞-°±±Ì æπ€≤Ï≤ªµΩ√˜œ‘µƒœ÷œÛ±‰ªØ(±æ µ—ÈÃıº˛œ¬£¨…˙≥…µƒŒ¢»ÐŒÔæ˘“‘≥¡µÌ–Œ Ω≥ˆœ÷)°£ °°°°±Ì1°°¡Ω¡ΩªÏ∫œµƒ µ—Èœ÷œÛ
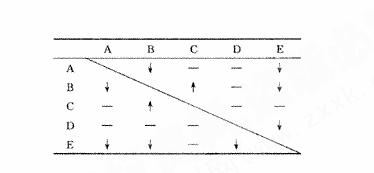
°°(1)∏˘æð µ—Èœ÷œÛ£¨ø…“‘≈–∂œA-EµƒŒÔ÷ √˚≥∆ «£∫ °°A________£¨B________£¨C________£¨D________£¨E________°£ °°(2)«Î¥”A-E’‚5÷÷ŒÔ÷ ÷–—°»° µ±ŒÔ÷ £¨Õ®π˝“ª÷÷∫œ¿ÌµƒÕææ∂÷∆»°—ıªØ√æ°£∞¥À≥–Ú–¥≥ˆ∏˜≤Ω∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°£ °°°°±Ì2°°∏¯∂® ‘º¡µƒ∑¥”¶«Èøˆ
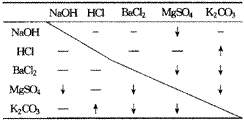
[Ω‚Œˆ]Ω´’‚ŒÂ÷÷ ŒÔ÷ ¡Ω¡ΩªÏ∫œ£¨¡–±Ì‘⁄œý”¶Œª÷√±Í≥ˆ”–πÿµƒ µ—Èœ÷œÛ£¨»Á±Ì2°£
°°¡Ω±Ì
ŒÔ÷ ¡Ω¡ΩªÏ∫œ£¨¡–±Ì‘⁄œý”¶Œª÷√±Í≥ˆ”–πÿµƒ µ—Èœ÷œÛ£¨»Á±Ì2°£
°°¡Ω±Ì ∂‘’’÷™AŒ™¬»ªØ±µ£¨BŒ™ÃºÀ·ºÿ£¨CŒ™—ŒÀ·£¨DŒ™«‚—ıªØƒ∆£¨EŒ™¡ÚÀ·√æ°£
∂‘’’÷™AŒ™¬»ªØ±µ£¨BŒ™ÃºÀ·ºÿ£¨CŒ™—ŒÀ·£¨DŒ™«‚—ıªØƒ∆£¨EŒ™¡ÚÀ·√æ°£
[“◊¥Ìµ„µ„æ¶]∏¯≥ˆ¡ÀŒÔ÷ ∑∂Œß∫Õ“‘±Ì∏Òµƒ–Œ Ω¬Þ¡–≥ˆ¡À µ—Èœ÷œÛ£¨“™«Ûøº…˙Õ∆∂œ≥ˆŒ¥÷™ŒÔ°£’‚¿ý–Õø…≤…”√£∫¡–±Ì∂‘’’∑®Ω‚¥°£
8°¢“ª÷÷≤ª¥øµƒÃ˙ø…ƒÐ∫¨”–√æ°¢¬¡°¢∏∆°¢Õ≠‘”÷  ÷–µƒƒ≥º∏÷÷°£»°∏√—˘∆∑5.6øÀ”Î◊„¡ø
÷–µƒƒ≥º∏÷÷°£»°∏√—˘∆∑5.6øÀ”Î◊„¡ø
µƒœ°—ŒÀ·∑¥”¶£¨µ√µΩ0.2øÀ«‚∆¯£¨‘Ú’‚÷÷Ã˙÷–“ª∂®∫¨”–µƒΩ Ù‘”÷ «_________°£
[Ω‚Œˆ]»ÙÃ˙÷–÷ª∫¨√æ°¢¬¡°¢∏∆÷–µƒ“ª÷÷£¨ƒ«√¥≤˙…˙µƒH2÷ ¡ø“ª∂®¥Û”⁄0.2øÀ£ª»ÙÀ˘∫¨‘”÷ ÷ª”–Õ≠£¨“ÚŒ™Õ≠”Îœ°—ŒÀ·≤ª∑¥”¶£¨À˘µ√«‚∆¯“ª∂®–°”⁄0.2øÀ£¨π Ã˙÷–À˘∫¨‘”÷ ≤ªø…ƒÐ «√æ°¢¬¡°¢Õ≠°¢∏∆÷–µƒ“ª÷÷£¨÷ª”–µ±Ã˙÷–∫¨”–‘”÷ Õ≠∫Õ¡ÌÕ‚“ª÷÷ªÚº∏÷÷Ω Ù ±£¨≤≈ƒÐµ√µΩÂ÷–À˘Àµµƒ0.2øÀ«‚∆¯£¨À˘“‘£¨Ã˙÷–“ª∂®∫¨”–µƒΩ Ù‘”÷ «Õ≠°£œÒ’‚¿ýÕ∆∂œÃ‚£¨∆‰Ãÿµ„ «º»“™∏˘æðªØ—ß∑¥”¶∑Ω≥Ã ΩΩ¯––º∆À„£¨”÷“™∏˘æðÀ˘∏¯≥ˆµƒ ˝æðΩ¯––—œ√ÐÕ∆¿Ì£¨≤≈ƒÐÀ≥¿˚µ√µΩÀ˘«Û¥∞∏°£
ΩΩ¯––º∆À„£¨”÷“™∏˘æðÀ˘∏¯≥ˆµƒ ˝æðΩ¯––—œ√ÐÕ∆¿Ì£¨≤≈ƒÐÀ≥¿˚µ√µΩÀ˘«Û¥∞∏°£
[“◊¥Ìµ„µ„æ¶]CœÓ”–“ª∂®µƒ√‘ªÛ–‘£¨“™«Û»´√Êøº¬«≤≈ƒÐ—°≥ˆ’˝»∑¥∞∏°£
7°¢”–“ª∞¸∑€ƒ©£¨ø…ƒÐ∫¨”–úÀ·∏∆°¢¡ÚÀ·Õ≠°¢ÃºÀ·ƒ∆°¢¡ÚÀ·ƒ∆°¢¬»ªØ±µ÷–µƒ“ª÷÷ªÚº∏÷÷°£“‘œ¬ «ƒ≥Õ¨—ßΩ¯–– µ—È≤¢π€≤ÏµΩµƒœ÷œÛ£∫»°…Ÿ¡ø∑€ƒ©∑≈»Î ‘πÐ÷–£¨º”ÀÆ°¢’Òµ¥°¢æ≤÷√∫Û£¨ ‘πÐ÷–”–∞◊…´≥¡µÌ∫Ռޅ´»Ð“∫£ª‘Ÿ œÚ ‘πÐ÷–µŒ»Î◊„¡øµƒœ°œıÀ·∫Û£¨∞◊…´≥¡µÌ”–≤ø∑÷»ÐΩ‚°£”…¥ÀÕ∆∂œ£¨∏√∞¸∑€ƒ©µƒø…ƒÐ◊È≥… «£∫(1)________£ª(2)_______£ª(3)________°£
œÚ ‘πÐ÷–µŒ»Î◊„¡øµƒœ°œıÀ·∫Û£¨∞◊…´≥¡µÌ”–≤ø∑÷»ÐΩ‚°£”…¥ÀÕ∆∂œ£¨∏√∞¸∑€ƒ©µƒø…ƒÐ◊È≥… «£∫(1)________£ª(2)_______£ª(3)________°£
[Ω‚Œˆ]¥À¿ýÕ∆∂œÃ‚µƒΩ‚ÂÀº¬∑ «£∫Õ®π˝Ã‚÷–√Ë ˆµƒœ÷œÛ£¨»∑∂®ƒ≥–© ŒÔ÷ ªÚ≈≈≥˝ƒ≥–©ŒÔ÷ °£”…Â÷–œ÷œÛ°∞ ‘πÐ÷–”–∞◊…´≥¡µÌ∫Ռޅ´»Ð“∫°±ø…÷™£¨∑€ƒ©÷–ø…ƒÐ”–≤ª»ÐπÃÃÂ
ŒÔ÷ ªÚ≈≈≥˝ƒ≥–©ŒÔ÷ °£”…Â÷–œ÷œÛ°∞ ‘πÐ÷–”–∞◊…´≥¡µÌ∫Ռޅ´»Ð“∫°±ø…÷™£¨∑€ƒ©÷–ø…ƒÐ”–≤ª»ÐπÃÃÂ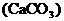 ªÚœýª•÷ƺ‰∑¥”¶ƒÐ…˙≥…∞◊…´≥¡µÌµƒŒÔ÷ ◊È∫œ(
ªÚœýª•÷ƺ‰∑¥”¶ƒÐ…˙≥…∞◊…´≥¡µÌµƒŒÔ÷ ◊È∫œ( ∫Õ
∫Õ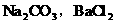 ∫Õ
∫Õ )£¨“ª∂®≤ª∫¨¡ÚÀ·Õ≠£ª”÷∏˘æðÂ∏¯–≈œ¢°∞µŒ»Î◊„¡øµƒœ°œıÀ·∫Û£¨∞◊…´≥¡µÌ”–≤ø∑÷»ÐΩ‚°±ø…÷™£¨¥À∞◊…´≥¡µÌ÷–“ª∂®”–
)£¨“ª∂®≤ª∫¨¡ÚÀ·Õ≠£ª”÷∏˘æðÂ∏¯–≈œ¢°∞µŒ»Î◊„¡øµƒœ°œıÀ·∫Û£¨∞◊…´≥¡µÌ”–≤ø∑÷»ÐΩ‚°±ø…÷™£¨¥À∞◊…´≥¡µÌ÷–“ª∂®”–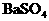 £¨ªπ∫¨”–
£¨ªπ∫¨”– ∫Õ
∫Õ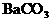 ÷–µƒ“ª÷÷ªÚ¡Ω÷÷£¨‘Ú‘≠πÃÃÂ∑€ƒ©÷–“ª∂®∫¨”–
÷–µƒ“ª÷÷ªÚ¡Ω÷÷£¨‘Ú‘≠πÃÃÂ∑€ƒ©÷–“ª∂®∫¨”– ∫Õ
∫Õ £¨“ª∂®≤ª∫¨¡ÚÀ·Õ≠£¨ø…ƒÐ∫¨”–
£¨“ª∂®≤ª∫¨¡ÚÀ·Õ≠£¨ø…ƒÐ∫¨”– ∫Õ
∫Õ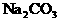 ÷–µƒ“ª÷÷ªÚ¡Ω÷÷°£π ’‚∞¸∑€ƒ©µƒø…ƒÐ◊È≥… «£∫(1)
÷–µƒ“ª÷÷ªÚ¡Ω÷÷°£π ’‚∞¸∑€ƒ©µƒø…ƒÐ◊È≥… «£∫(1)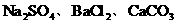 £ª(2)
£ª(2)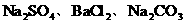 £ª(3)
£ª(3)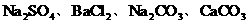 °£
°£
[“◊¥Ìµ„µ„æ¶]¥À¿ý“ª∞„ƒ—∂»Ωœ¥Û£¨…ʺ∞µƒ÷™ ∂√ʱ»Ωœπ„°£∑÷Œˆ’‚¿ýƒø ±£¨Õ∑ƒ‘“™¿‰æ≤£¨≤ª“™∞—Œ œε√ô∏¥‘”£¨∑Ò‘ÚΩ´œð‘⁄ƒø…˺∆µƒ√‘π¨÷–°£
6°¢»Áœ¬ÕºÀ˘ 浃 µ—È÷–£¨Õ®»Îµƒ∆¯ÃÂA ««‚∆¯∫Õ“ª—ıªØú÷–µƒ“ª÷÷ªÚ¡Ω÷÷£¨∫⁄…´∑€ƒ©B «—ıªØÕ≠∫ÕƒæÃø∑€÷–µƒ“ª÷÷ªÚ¡Ω÷÷°£ µ—È÷–π€≤ÏµΩµƒœ÷œÛ «£∫∫⁄…´∑€ƒ©±‰∫Ï…´£¨ŒÞÀÆ¡ÚÀ·Õ≠±‰¿∂…´£¨≥Œ«Â ت“ÀƱ‰ªÎ◊«°£”…¥À≈–∂œ£∫∆¯ÃÂA∫Õ∫⁄…´∑€ƒ©Bµƒø…ƒÐ◊È∫œ”–ƒƒº∏÷÷£ø(√ø÷÷◊È∫œ÷–A∫ÕBµƒ≥…∑÷æ˘“™«Û”√ªØ—ß Ω±Ì æ)
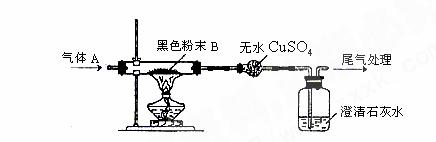
[Ω‚Œˆ]”…Â÷–œ÷œÛ°∞∫⁄…´∑€ƒ©±‰∫Ï…´£¨ŒÞÀÆ¡ÚÀ·Õ≠±‰¿∂…´£¨≥Œ«Â ت“ÀƱ‰ªÎ◊«°±ø…÷™£¨∑¥”¶∫Û“ª∂®…˙≥…¡À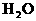 ∫Õ
∫Õ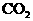 £¨ø…ƒÐ∑¢…˙µƒ∑¥”¶”–£∫¢Ÿ
£¨ø…ƒÐ∑¢…˙µƒ∑¥”¶”–£∫¢Ÿ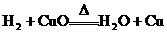 £¨¢⁄
£¨¢⁄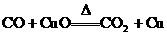 £¨¢€
£¨¢€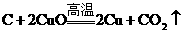 °£“Ú¥À£¨ÀƵƒ¿¥‘¥÷ª”–“ª∏ˆ£¨‘Ú∆¯ÃÂA÷–±ÿ∫¨”–
°£“Ú¥À£¨ÀƵƒ¿¥‘¥÷ª”–“ª∏ˆ£¨‘Ú∆¯ÃÂA÷–±ÿ∫¨”–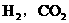 µƒ¿¥‘¥”–¡Ω∏ˆ£¨‘ÚC∫ÕCOø…ƒÐ÷ª∫¨∆‰÷–÷Æ“ª£¨“≤ø…ƒÐ¡Ω’þ∂º∫¨”–°£π ∆¯ÃÂA∫Õ∫⁄…´∑€ƒ©Bø…ƒÐ”–»˝÷÷◊È∫œ£∫¢ŸAŒ™
µƒ¿¥‘¥”–¡Ω∏ˆ£¨‘ÚC∫ÕCOø…ƒÐ÷ª∫¨∆‰÷–÷Æ“ª£¨“≤ø…ƒÐ¡Ω’þ∂º∫¨”–°£π ∆¯ÃÂA∫Õ∫⁄…´∑€ƒ©Bø…ƒÐ”–»˝÷÷◊È∫œ£∫¢ŸAŒ™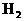 £¨BŒ™CuO∫ÕC£ª¢⁄AŒ™
£¨BŒ™CuO∫ÕC£ª¢⁄AŒ™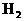 ∫ÕCO£¨BŒ™CuO£ª¢€AŒ™
∫ÕCO£¨BŒ™CuO£ª¢€AŒ™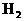 ∫ÕCO£¨BŒ™CuO∫ÕC°£
∫ÕCO£¨BŒ™CuO∫ÕC°£
[“◊¥Ìµ„µ„æ¶]¥À¿ýÂ÷˜“™ «øº≤ÈÕ¨—ß√«µƒ◊€∫œ∑÷ŒˆƒÐ¡¶£¨≤ªµ´“™«ÛÕ¨—ß√«æþ±∏”–πÿªØ∫œŒÔµƒª˘¥°÷™ ∂£¨∂¯«““™”– µ—È≤Ÿ◊˜µƒæ≠¿˙∫Õ∑÷Œˆ°¢Ω‚æˆªØ—ß µ—ÈŒ µƒƒÐ¡¶°£Ω‚ ±–Ë“™»œ’Ê∑÷ŒˆÃ‚ƒø∏¯≥ˆµƒÃıº˛£¨¡™œµ µº £¨÷“ª∑÷ŒˆÕ∆∂œ°£
5°¢±æÂ…ʺ∞µƒ∑¥”¶∂º Ù”⁄∏¥∑÷Ω‚∑¥”¶£¨A-F «≥ı÷–ªØ—ß÷–≥£º˚µƒ≤ªÕ¨ªØ∫œŒÔ£Æ
°°°° ¢ŸA»Ð“∫∫ÕB»Ð“∫ªÏ∫œ∑¢…˙ªØ—ß∑¥”¶£Æµ´ŒÞ√˜œ‘œ÷œÛ£ª
°°°° ¢⁄c°¢DµƒªÏ∫œ»Ð“∫÷–µŒº”—ŒÀ·£¨œ» ŒÞ√˜œ‘œ÷œÛ£¨∫Û≤˙…˙ŒÞ…´°¢ŒÞ∆¯Œ∂µƒ∆¯Ã£ª
ŒÞ√˜œ‘œ÷œÛ£¨∫Û≤˙…˙ŒÞ…´°¢ŒÞ∆¯Œ∂µƒ∆¯Ã£ª
°°°° ¢€E°¢FµƒªÏ∫œ»Ð“∫÷–µŒº”«‚—ıªØƒ∆»Ð“∫£¨œ»ŒÞ√˜œ‘œ÷œÛ£¨∫Û…˙≥…¿∂…´≥¡µÌ£Æ
°°°° «Îªÿ¥œ¬¡–Œ £Æ(◊¢“‚£∫√ø–°Ã‚∂º”–∂ý÷÷ø…ƒÐ£¨÷ª¥≥ˆ“ª÷÷ø…ƒÐº¥ø…£Æ)
°°°° (1)¢Ÿ÷–ªØ—ß∑Ω≥Ã ΩŒ™£∫ °°°°°°°°°°°°°°°°°°°°°°°°°°£Æ
°°°° (2)C°¢DµƒªØ—ß Ω£∫C°°°° °¢D°° °°°°£ª
(3)¢€÷–…ʺ∞µƒ¡Ω∏ˆªØ—ß∑Ω≥Ã Ω£∫°°°°°°°°°°°° °°°¢°°°°°°°°°°°°°°°°°° °£
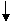 [Ω‚Œˆ]Ω‚¥ÀµƒÕª∆∆ø⁄‘⁄”⁄∑¥”¶(2)∫Õ(3)÷–œ»ŒÞ√˜œ‘œ÷œÛ£¨∫Û≤˙…˙œ÷œÛ£¨¥”¢⁄º¥ø…Õ∆÷™C∫ÕDµƒªÏ∫œ»Ð“∫÷–”–“ªŒÔ÷ ”ΗŒÀ·œ»∑¥”¶∫Û£¨¡Ì“ªŒÔ÷ ‘Ÿ”ΗŒÀ·∑¥”¶£¨≤˙…˙∆¯Ã£¨Õ¨¿ÌÀºøº¢€£¨±æÂø…—°¥∞∏Ωœ∂ý£¨”¶œ»»∑∂®C°¢D°¢E°¢FÀƒ÷÷ŒÔ÷ ∫Û£¨‘Ÿ»∑∂®A°¢B°£
[Ω‚Œˆ]Ω‚¥ÀµƒÕª∆∆ø⁄‘⁄”⁄∑¥”¶(2)∫Õ(3)÷–œ»ŒÞ√˜œ‘œ÷œÛ£¨∫Û≤˙…˙œ÷œÛ£¨¥”¢⁄º¥ø…Õ∆÷™C∫ÕDµƒªÏ∫œ»Ð“∫÷–”–“ªŒÔ÷ ”ΗŒÀ·œ»∑¥”¶∫Û£¨¡Ì“ªŒÔ÷ ‘Ÿ”ΗŒÀ·∑¥”¶£¨≤˙…˙∆¯Ã£¨Õ¨¿ÌÀºøº¢€£¨±æÂø…—°¥∞∏Ωœ∂ý£¨”¶œ»»∑∂®C°¢D°¢E°¢FÀƒ÷÷ŒÔ÷ ∫Û£¨‘Ÿ»∑∂®A°¢B°£
(¢ŸNaOH + HCl°° ===°° NaCl+H2O°°°° (2)CŒ™KOH°¢DŒ™Na2CO3°°°° (3) 2NaOH+H2SO4===Na2SO4+2H2O°¢°° CuSO4+2NaOH===Cu(OH)2°° +°° Na2SO4°°°° )
[“◊¥Ìµ„µ„æ¶]Ω‚¥¥À¿ýµƒ∑Ω∑® «œ»¿Ì«Âƒø÷–∏¯≥ˆµƒ∏˜÷÷–≈œ¢÷ƺ‰µƒπÿœµ£¨’“≥ˆÕª∆∆ø⁄£¨÷“ªÕ∆∂œ≥ˆ¿¥°£
4°¢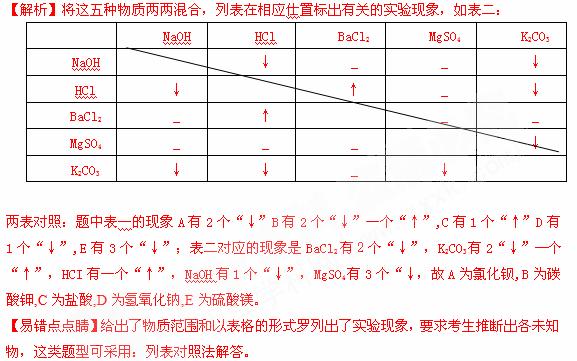 “—÷™A°¢B°¢C°¢D°¢E°¢F6÷÷ŒÔ÷ µƒ◊™ªØπÿœµ»Áœ¬£∫
“—÷™A°¢B°¢C°¢D°¢E°¢F6÷÷ŒÔ÷ µƒ◊™ªØπÿœµ»Áœ¬£∫
(1)A+B°˙C+H2O°°°° (2)C+KOH°˙D°˝(¿∂…´)+E°°°° (3)B+D°˙C+H2O°°°° °°°°(4)E+BaCl2°˙F°˝(∞◊…´£¨≤ª»Ð”⁄œ°œıÀ·)+KCl
∏˘æð…œ ˆ±‰ªØπÿœµ£¨ Õ∆∂œ”–πÿŒÔ÷ µƒªØ—ß Ω£∫
Õ∆∂œ”–πÿŒÔ÷ µƒªØ—ß Ω£∫
A°°°°°°°° £ªB°°°°°°°° £ªC°°°°°°°° £ªD°°°°°°°° £ªE°°°°°°°°°° £ªF°°°°°°°° °£
[Ω‚Œˆ]∆‰ µ∏√¿ý”Ϋ∞“ª¿ý–Õ“ª—˘£¨Õ˘Õ˘ª·≥ˆœ÷√˜œ‘µƒœ÷œÛÃÿ’˜°£±æµƒÕª∆∆ø⁄‘⁄∑¥”¶ Ω(4)£¨”…∏¥∑÷Ω‚∑¥”¶µƒ÷™ ∂ø…÷™£∫F÷–∫¨Ba£¨”÷FŒ™°∞∞◊…´«“≤ª»Ð”⁄œ°œıÀ·µƒŒÔ÷ °±£¨π FŒ™BaSO4,÷Æ∫Û”÷ø…Õ∆µ√EŒ™KCl°£¡Ì“ª∏ˆÕª∆∆ø⁄‘⁄∑¥”¶ Ω(2)£¨“ÚŒ™DŒ™°∞¿∂…´≥¡µÌ°±£¨π ø…Õ∆µ√DŒ™Cu(OH)2£ª‘ŸΩ·∫œEŒ™KCl£¨ø…Õ∆µ√CŒ™CuCl2°£»ª∫Û‘⁄(3)÷–ø…Õ∆µ√BŒ™HCl£¨‘⁄(1)÷–ø…Õ∆µ√AŒ™CuO°£
[“◊¥Ìµ„µ„æ¶]∆‰ µ∏√¿ý”Ϋ∞“ª¿ý–Õ“ª—˘£¨Õ˘Õ˘ª·≥ˆœ÷√˜œ‘ µƒœ÷œÛÃÿ’˜°£±æµƒÕª∆∆ø⁄‘⁄∑¥”¶ Ω(4)£¨”…∏¥∑÷Ω‚∑¥”¶µƒ÷™ ∂ø…÷™£∫F÷–∫¨Ba£¨”÷FŒ™°∞∞◊…´«“≤ª»Ð”⁄œ°œıÀ·µƒŒÔ÷ °±£¨π FŒ™BaSO4°£
µƒœ÷œÛÃÿ’˜°£±æµƒÕª∆∆ø⁄‘⁄∑¥”¶ Ω(4)£¨”…∏¥∑÷Ω‚∑¥”¶µƒ÷™ ∂ø…÷™£∫F÷–∫¨Ba£¨”÷FŒ™°∞∞◊…´«“≤ª»Ð”⁄œ°œıÀ·µƒŒÔ÷ °±£¨π FŒ™BaSO4°£
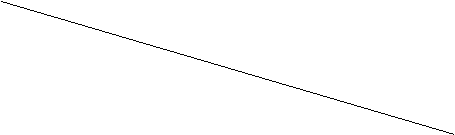
3°¢”–A°¢B°¢C°¢D°¢EŒÂ∆ø ß»•±Í«©µƒŒÞ…´»Ð“∫£¨À¸√«∑÷± «NaOH°¢HCI°¢MgSO4°¢K2CO3÷–µƒ“ª÷÷°£Œ™¡Àº¯±£¨∏˜»°…Ÿ¡ø»Ð“∫¡Ω¡ΩªÏ∫œ µ—ÈΩ·π˚»Á±Ì“ªÀ˘ æ°£±Ì÷–°∞°˝°±±Ì æ…˙≥…ƒ—»ÐªÚŒ¢»Ðµƒ≥¡µÌ£ª°∞°¸°±±Ì æ”–∆¯ÃÂ≤˙…˙£ª°∞£≠°±±Ì æπ€≤Ï≤ªµΩ√˜œ‘µƒœ÷œÛ±‰ªØ(±æ µ—ÈÃıº˛œ¬£¨…˙≥…µƒŒ¢»ÐŒÔæ˘“‘≥¡µÌ–Œ Ω≥ˆœ÷)°£±Ì“ª:
 |
A |
B |
C |
D |
E |
|
A |
°° |
°˝ |
_ |
_ |
°˝ |
|
B |
°˝ |
°° |
°¸ |
_ |
°˝ |
|
C |
_ |
°¸ |
|
_ |
_ |
|
D |
_ |
_ |
_ |
°° |
°˝ |
|
E |
°˝ |
°˝ |
_ |
°˝ |
°° |
°°(1)∏˘æð µ—Èœ÷œÛ£¨ø…“‘≈–∂œA----EµƒŒÔ÷ √˚≥∆ «£∫A ___ B___C___ D___ E____
(2)«Î¥”A---E’‚5÷÷ŒÔ÷ ÷–—°»° µ±ŒÔ÷ £¨Õ®π˝“ª÷÷∫œ¿ÌµƒÕææ∂÷∆»°—ıªØ√æ°£∞¥À≥–Ú–¥≥ˆ∏˜≤Ω∑¥”¶µƒªØ—ß∑Ω≥Ã Ω°£
2°¢œ¬Õº÷–µƒ∏˜ŒÔ÷ æ˘Œ™≥ı÷–ªØ—ß≥£º˚ŒÔ÷ °£«Î∏˘æðÕº æπÿœµªÿ¥£∫
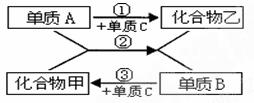
¢≈º◊ŒÔ÷ ÷–µƒ‘™Àÿπ≤”–___÷÷°£
¢∆∑¥”¶¢⁄µƒª˘±æ∑¥”¶¿ý–ÕŒ™______°£
¢«»Ù≥£Œ¬œ¬““Œ™ŒÞ…´“∫㨑ÚAŒ™__£ª∑¥”¶¢⁄µƒªØ—ß∑Ω≥à Ωø…ƒÐŒ™___________°£
|
|
[“◊¥Ìµ„µ„æ¶]’‚¿ý–Փª∞„≤ªœÞ∂®ŒÔ÷ ∑∂Œß£¨∏¯≥ˆ∏˜ŒÔ÷ ◊™ªØπÿœµ£¨“™«Ûøº…˙Õ∆∂œ≥ˆ∏˜Œ¥÷™ŒÔ°£¥À–Փ™“‘ŒÔ÷ µƒ◊™ªØπÿœµŒ™“¿æ𣨔√ƒÊÕ∆∑®”…π˚«Û“Ú£¨‘Ÿ”√À≥Õ∆∑®º”“‘—È÷§°£
1°¢‘≠◊”µƒ∫ÀµÁ∫… ˝–°”⁄18µƒƒ≥‘™ÀÿX£¨‘≠◊”µƒµÁ◊”≤„ ˝Œ™n(nŒ™’˝’˚ ˝)£¨◊ÓÕ‚≤„µÁ◊” ˝Œ™£¨‘≠◊”÷–µƒ÷ ◊” ˝Œ™£¨”–πÿXµƒÀµ∑®≤ª’˝»∑µƒ «( )
A. XƒÐ–Œ≥…ªØ—ß ΩŒ™ µƒºÓ°°°°°°°°°° B. Xøœ∂®ƒÐ–Œ≥…ªØ—ß ΩŒ™ µƒ∫¨—ıÀ·ƒ∆—Œ
C. X‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝∫Õ∫ÀµÁ∫… ˝øœ∂®Œ™∆Ê ˝°°°°°° D. X «∑«Ω Ù‘™Àÿ]
[ Ω‚Œˆ]Ω‚¥Àµƒπÿº¸ « ◊œ»»∑∂®XŒ™∫Œ÷÷‘™Àÿ°£“ÚŒ™n «µÁ◊”≤„ ˝£¨µ± ±£¨◊ÓÕ‚≤„µÁ◊” ˝Œ™3£¨÷ ◊” ˝Œ™1£¨’‚≤ª ««‚‘≠◊”£ªµ±ªÚ3 ±£¨◊ÓÕ‚≤„µÁ◊” ˝∑÷±Œ™5°¢7°£÷ ◊” ˝∑÷±Œ™7°¢17°£÷ ◊” ˝∫Õ∫ÀÕ‚µÁ◊” ˝œýµ»£¨∑÷± «µ™‘™Àÿ∫Õ¬»‘™Àÿ£¨‘⁄–Œ≥…ªØ∫œŒÔ ±∂º“◊µ√µΩµÁ◊”£¨–Œ≥…Œ»∂®Ω·ππ£¨±Ìœ÷Œ™∏∫º€£¨≤ªø…ƒÐ”οÎ◊”Ω·∫œ≥…ºÓ£¨µ´¬»°¢µ™¡Ω‘™Àÿæ˘ø…”Ηı‘™ÀÿΩ·∫œ–Œ≥…∫¨—ıÀ·∏˘‘≠◊”Õ≈£¨∏˙Ω ÙªÚ∑«Ω Ù‘™Àÿ◊È≥…ªØ∫œŒÔ£¨œÒBœÓ÷–µƒ°£¥∞∏Œ™A°£
Ω‚Œˆ]Ω‚¥Àµƒπÿº¸ « ◊œ»»∑∂®XŒ™∫Œ÷÷‘™Àÿ°£“ÚŒ™n «µÁ◊”≤„ ˝£¨µ± ±£¨◊ÓÕ‚≤„µÁ◊” ˝Œ™3£¨÷ ◊” ˝Œ™1£¨’‚≤ª ««‚‘≠◊”£ªµ±ªÚ3 ±£¨◊ÓÕ‚≤„µÁ◊” ˝∑÷±Œ™5°¢7°£÷ ◊” ˝∑÷±Œ™7°¢17°£÷ ◊” ˝∫Õ∫ÀÕ‚µÁ◊” ˝œýµ»£¨∑÷± «µ™‘™Àÿ∫Õ¬»‘™Àÿ£¨‘⁄–Œ≥…ªØ∫œŒÔ ±∂º“◊µ√µΩµÁ◊”£¨–Œ≥…Œ»∂®Ω·ππ£¨±Ìœ÷Œ™∏∫º€£¨≤ªø…ƒÐ”οÎ◊”Ω·∫œ≥…ºÓ£¨µ´¬»°¢µ™¡Ω‘™Àÿæ˘ø…”Ηı‘™ÀÿΩ·∫œ–Œ≥…∫¨—ıÀ·∏˘‘≠◊”Õ≈£¨∏˙Ω ÙªÚ∑«Ω Ù‘™Àÿ◊È≥…ªØ∫œŒÔ£¨œÒBœÓ÷–µƒ°£¥∞∏Œ™A°£
[“◊¥Ìµ„µ„æ¶]Ω‚¥¥À¿ýµƒ∑Ω∑® «œ»¿Ì«Âƒø÷–∏¯≥ˆµƒ∏˜÷÷–≈œ¢÷ƺ‰µƒπÿœµ£¨’“≥ˆÕª∆∆ø⁄£¨÷“ªÕ∆∂œ≥ˆ¿¥°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com