
题目列表(包括答案和解析)
3、以下推理正确的是()
A、由甲酸可以发生银镜反应可推出其余的梭酸也均能发生银镜反应
B、NaCl与CsCl化学式相似,故NaC与CsCl的物理性质也相似
C、由“2Fe + 3Cl2= 2FeC13 ”反应可推出“2Fe + 3I2=ZFeI3”反应也能发生
D、由 H2O的沸点大于H2S的沸点可推知NH3 的沸点大于 PH3 的沸点
2、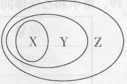 用右图表示的一些物质或概念间的从属关系中不正确的是( )
用右图表示的一些物质或概念间的从属关系中不正确的是( )
|
|
X |
Y |
Z |
|
例 |
氧化物 |
化合物 |
纯净物 |
|
A |
苯的同系物 |
芳香烃 |
芳香族化合物 |
|
B |
胶体 |
分散系 |
混合物 |
|
C |
电解质 |
离子化合物 |
化合物 |
|
D |
碱性氧化物 |
金属氧化物 |
氧化物 |
1、一定量的锎(98252Cf)是有用的中子源,1mg(98252Cf)每秒约放出2. 34xl99个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关锎的说法错误的是
A、(98252Cf)原子中,中子数为154 B、(98252Cf)原子中,质子数为98
C、(98252Cf)原子中,电子数为 98 D、锎元素的相对原子质量为252
29.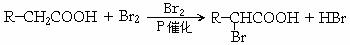 (16分)下面表示的是某有机物烃A在一定条件下转化为H与N的关系,其中N是高分子。已知:
(16分)下面表示的是某有机物烃A在一定条件下转化为H与N的关系,其中N是高分子。已知:
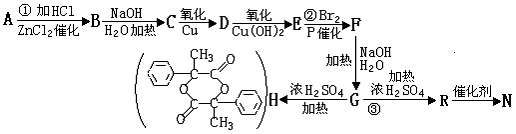
 回答下列问题:
回答下列问题:
(1)写出G具有的官能团名称
写出反应类型:② ,③ 。
(2)写出有机物的结构简式:F ,B 。
(3)写出下列化学方程式:
D→E: 。
R→N: 。
(4)F也可以经一步反应生成R,其反应条件是: 。
(5) E的同分异构体有多种,其中属于苯的二取代物,且既能起银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有6种,请写出其中任意一种的结构简式 。
28.(16分)某校化学小组学生利用下图所示装置进行“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中有CO2和CO。(图中夹持装置已略去)
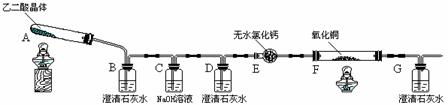
(1)装置C中盛放NaOH溶液的作用是 。
(2)①证明分解产物中有CO2的现象是 。
②证明分解产物中有CO的现象是
(3)实验结束后,装置F中黑色氧化铜变为红色固体。简述检验红色固体中是否含有Cu2O的实验方法(已知Cu2O溶于稀硫酸生成铜单质和硫酸铜):
(4)该装置有一个不足之处,请写出弥补这个不足之处的理由和具体方法:
。
(5)①草酸和草酸钠(Na2C2O4)可以在酸性条件下被KMnO4、MnO2氧化。KMnO4和草酸钠在稀硫酸中反应的离子方程式是
②实验室常用草酸钠标定KMnO4溶液。操作如下:准确称取0.2000 g草酸钠,放入锥形瓶中,加100 mL稀硫酸溶解,用配置好的KMnO4溶液滴定。当加入1滴KMnO4溶液后,锥形瓶中溶液立即由无色变为紫红色,且30 s不褪色,即达到滴定终点。重复上述滴定操作三次,实验数据如下表所示。
|
|
滴定前 |
第一次终点 |
第二次终点 |
第三次终点 |
|
滴定管 液面刻度 |
0.00 mL |
16.02 mL |
16.00mL |
16.01 mL |
KMnO4溶液的物质的量浓度的计算式是
c(KMnO4)= 。
27.(14分)某些物质的转化关系如下图所示。其中甲可由两种单质直接化合得到;乙为金属单质,常温下,它在G的浓溶液中不溶解;F的溶液中只含一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。
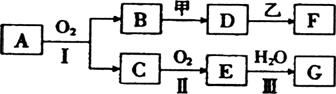
(1)若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近时,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。
① 写出B和甲反应的化学方程式 。
② 1.7 g A与O2反应生成气态的B和C时放出22.67 kJ热量,写出该反应的热化学方程式 。
③D与乙反应的离子方程式是 。(2)若B为红棕色固体,C能使品红试液褪色,D的水溶液中加人HNO3酸化的AgNO3溶液有白色沉淀生成,向F中加入过量的NaOH溶液,有沉淀产生。
① 工业上反应II在 中进行。
② D和乙反应的化学方程式是 。
③ B、D、F中含同一种元素,该元素在周期表中的位置是: 。④写出由B为原料,得到该元素单质的化学方程式: _______。
26.(14分)X、Y、Z、W为原子序数依次增大的四种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水。
(1)Y的元素符号是_______________XW的电子式是________________
(2)XW与YX3反应生成一种盐,该盐水溶液的pH______________7(填“大于”“小于”或“等于”),其原因是(用离子方程式表示)___________________________
(3)Z元素氢化物的沸点比H2O_________(填“低”或“高”)。Z元素的氢化物有毒,写出用CuSO4溶液吸收Z元素氢化物的离子方程式________ _____________
(4)用石墨电极电解W的钠盐饱和溶液,反应的离子方程式为___ ___ ,
若反应的溶液的体积为200mL,测得pH为13,则阳极得到的气体质量为 。
13.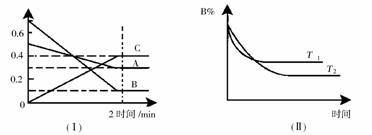 T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B和C物质的量变化与时间关系如下图(Ⅰ)所示。若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如下图(Ⅱ)所示。下列叙述正确的是( )
T℃时,在2L的密闭容器中,A气体与B气体发生可逆反应生成C气体,反应过程中A、B和C物质的量变化与时间关系如下图(Ⅰ)所示。若保持其它条件不变,温度分别为T1和T2时,B的物质的量分数与时间关系如下图(Ⅱ)所示。下列叙述正确的是( )
A.2min内A的化学反应速率为0.1mol/L min
B.在反应达到平衡时,保持其它条件不变,增大压强,正逆反应速率都增大,且平衡向逆反应方向移动
C.在反应达到平衡时,保持其它条件不变,升高温度,正逆反应速率都增大,且A的转化率增大
D.在T℃时,若A的浓度减少了1mol/L,则B的浓度会减少3mol/L,C的浓度会增加2mol/L
第Ⅱ卷(共4小题,共60分)
12.下列叙述正确的是 ( )
A.同一主族的元素,原子半径越大,其单质的熔点越高
|
C.位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元
素的最高化合价一定是X<Y
D.将pH=2,体积相同的盐酸和醋酸溶液均稀释100倍后,分别加入足量的相同颗粒大小的锌,产生H2的起始速率相同,醋酸放出的氢气多
11.有一种MCFC型燃料电池,该电池所用燃料为H2和空气,电解质为熔融的K2CO3。电
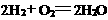 池的总反应为: ,负极反应为H2 + CO32--2e- = H2O + CO2。下列说法中正确的是( )
池的总反应为: ,负极反应为H2 + CO32--2e- = H2O + CO2。下列说法中正确的是( )
A.正极反应为4OH--4e-= 2H2O + O2↑
B.电池放电时,电池中CO32-的物质的量将逐渐减少 C.放电时CO32-向负极移动
D.电路中的电子经正极、负极、熔融的K2CO3后再转移到正极,形成闭合回路
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com