
题目列表(包括答案和解析)
2.下列物质:①苯酚 ②淀粉 ③油脂 ④蛋白质 ⑤硝基苯 ⑥明矾 ⑦氯乙烷 ⑧皓矾 ⑨水玻璃 ⑩碘化钠。不能发生水解的是 ( )
A.①⑤⑩ B.③⑥⑨ C.②④⑦⑧ D.①②④⑩
1.近几年,国际上提出了:“预防污染”这一概念,绿色化学是“预防污染”的根本手段。针对“吸烟”而言,下列活动属于实施绿色化学活动的是: ( )
A.处理废弃物--烟灰、烟蒂 B.治理 污染点--通风、排除烟雾
C.减少有毒物--使用过滤嘴、低焦油烟 D.杜绝污染物--禁烟、戒烟
23(8分)现有分子式均为C3H6O2的四种有机物A、B、C、D,且分子中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
|
|
NaOH溶液 |
银氨溶液 |
新Cu(OH)2 |
金属钠 |
|
A |
中和反应 |
-- |
溶解 |
产生氢气 |
|
B |
-- |
有银镜 |
加热后有红色沉淀 |
产生氢气 |
|
C |
水解反应 |
有银镜 |
加热后有红色沉淀 |
-- |
|
D |
水解反应 |
-- |
-- |
-- |
则A、B、C、D的结构简式分别为:
A__________,B_________,C__________,D__________。
24(10分)某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;H的三聚合物I也是一种六元环状化合物。(图中部分反应条件及产物没有列出)
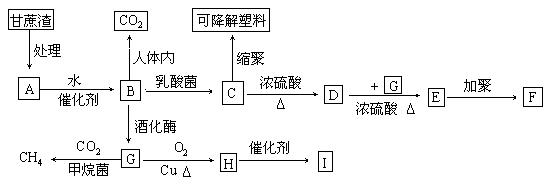 (1)写出下列物质的结构简式:
(1)写出下列物质的结构简式:
高分子化合物F_____________;六元环状化合物I_____________。
(2)C → D的反应类型为____________。D → E的反应类型为_____________。
(3)写出下列反应的化学方程式:A → B____________________________,
C →可降解塑料_____________________。
(4)H分子所含官能团的名称是__________,实验室中常用于检验该官能团的试剂的名称是(只写一种)__________________________。
(5)G转变成CH4的反应曾做过如下的同位素示踪实验(D、T为H的同位素):
 六、(本题包括2小题,共20分)
六、(本题包括2小题,共20分)
25(8分)已知pH = 2的高碘酸(H5IO6)溶液与pH = 12的NaOH溶液等体积混合,所得混合液显酸性;0.01 mol·L-1的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH = 12的NaOH溶液等体积混合,所得混合液显中性。
请回答下列问题:
(1)高碘酸是_______(填写“强酸”或“弱酸”),理由是_____________________。
(2)已知高碘酸和硫酸锰(MnSO4)在溶液中反应生成高锰酸,碘酸和硫酸,此反应的氧化剂是_________,反应的离子方程式可表示为________________________________。
26(12分)在定量分析化学反应中各物质的计量关系时,往往可利用质量守恒、离子电荷守恒和得失电子守恒等规律将问题简单化。
现有单质铁溶于稀硝酸反应的化学方程式可表示为:
aFe + bNO3- + cH+ = d Fe2+ + fFe3+ + gNO↑+ hN2O↑+ kH2O
试回答下列问题:
(1)下列各种情况下的数学等量关系式为:
①b、c、d、f的数学关系式为_____________。
②d、f、g、h的数学关系式为_____________。
③c、g、h的数学关系式为_______________。
(2)若a =16时,Fe和稀硝酸全部反应,则b的取值范围是_____________,C的取值范围是________________。
21(10分)A、B、C、D四种短周期元素的原子序数依次增大,A元素的气态氢化物与A元素的最高价氧化物对应的水化物能反应生成盐;B、C、D同周期,它们的最高价氧化物对应的水化物两两之间都能反应生成盐和水,B和D可组成化合物BD。回答下列问题:
(1)A元素的气态氢化物的结构式为:__________。D的最高价氧化物对应水化物的化学式:____________。
(2)在工业上常用________法制备单质C(填金属的冶炼方法)
(3)C、D组成的化合物溶于水的离子方程式:_________________。
(4)B、C最高价氧化物对应的水化物在溶液中反应的离子方程式为:_____________。
22(10分)已知A、B、C均为常见的单质,其中A为金属,B、C为非金属,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略)
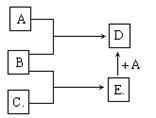
请回答:
(1)若常温下B、C均为气体,D为黑色晶体,E的电子式为_________,A和E在一定条件下反应生成D的化学方程式为_______________________。
(2)若常温下B为气体,C为黑色固体,则构成金属A的原子结构示意图为_______,E的结构式为________,A和E在一定条件下反应生成D的化学方程式为______________。
19、(4分)下图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其它用途。
错误!嵌入对象无效。
(1)医院里给病人输氧时,往往在氧气钢瓶与病人呼吸面具之间安装盛有水的该装置,用于观察气泡产生的情况,以便调节供氧速率,此时氧气应从_________(填标号,下同)管口导入。
(2)实验室用MnO2与浓HCl反应制Cl2的实验中,在将生成的Cl2通入NaOH溶液之前,先将Cl2从该装置_______管口导进,从_______管口导出,此时,该装置所起的作用是防止NaOH溶液倒流入反应器。
(3)当用此装置收集NO时,应采取的主要操作步骤是:
①__________________________;②____________________________。
20(16分)某校开展课外研究性学习活动。
I、第一小组对市场上的碘盐进行了研究。在碘盐里,碘以KIO3形式存在。请回答下列问题:
(1)正确食用碘盐才能起到补碘的作用,该小组对油炸食品时是否适宜放碘进行了课题研究。
请你协助拟定课题名称:________________。
其研究成果的最终形式是:______________。
(2)怎样检验碘盐中含有碘?(可供选择的试剂有:稀硝酸、稀盐酸、KCl、KI淀粉溶液、石蕊试液)用离子方程式表示______________________。
Ⅱ、第二小组利用废铜制取CuSO4:
(1)甲学生进行了下列实验:取含6.4g铜的废铜和10mL 18 mol·L-1浓硫酸放在圆底烧瓶中共热,直到反应完毕,最后发现烧瓶中还有铜片剩余。他根据自己所学的化学知识,认为烧瓶中还有较多的硫酸剩余。你认为他的判断是否正确_______(填是或否),其理由是________________________________。
(2)乙同学认为甲设计的方案不好,他自己设计的思路是:2Cu + O2  2CuO、CuO +H2SO4 = CuSO4 + H2O。
2CuO、CuO +H2SO4 = CuSO4 + H2O。
对比甲的方案,乙同学的优点是:__________________________。
(3)某地有丰富的电力源,为了同时具备乙同学的优点,你能不能根据该地的资源优势也设计一个用铜和硫酸制取CuSO4的方案?(其他材料任选)______________________。
18、已知某溶液中存在OH-、H+、NH4+、Cl-四种离子。经四位同学测定其浓度大小的关系如下,其中不可能的是( )
A、c(Cl-)> c(NH4+)> c(H+)> c(OH-)
B、c(Cl-)> c(H+)> c(NH4+)> c(OH-)
C、c(Cl-)> c(NH4+)> c(OH-)> c(H+)
D、c(OH-)> c(H+)> c(Cl-)> c(NH4+)
第Ⅱ部分 非选择题(共78分)
17、pH=12的X、Y两种碱溶液各10mL,分别稀释至1000mL,其pH与溶液体积(V)的关系如下图所示,下列说法正确的是( )
错误!嵌入对象无效。
A、X、Y两种碱的物质的量浓度一定相等
B、若10<a<12,则X、Y都是弱碱
C、完全中和X、Y两溶液时,消耗同浓度盐酸的体积VX > VY
D、稀释后,X溶液的碱性比Y溶液的碱性强
16、下列说法中正确的是( )
A、核外电子排布完全相同的两种微粒,其化学性质一定相同
B、同周期的主族元素从左到右,非金属性逐渐增强,气态氢化物稳定性逐渐增强
C、元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
D、原子最外层电子数大于4的元素一定是非金属元素
15、已知热化学方程式:2H2(g)+ O2(g)= 2H2O(g);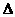 H1 =
-483.6 kJ·mol-1,则对于热化学方程式:2H2O(l)= 2H2(g)+ O2(g);
H1 =
-483.6 kJ·mol-1,则对于热化学方程式:2H2O(l)= 2H2(g)+ O2(g);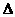 H2 = b,下列说法正确的是( )
H2 = b,下列说法正确的是( )
A、热化学方程式中化学计量数表示分子个数 B、该反应的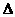 H2=
+483.6 kJ·mol-1
H2=
+483.6 kJ·mol-1
C、 D、
D、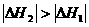
14、下列各组离子一定能在指定环境中大量共存的是( )
A、在c(HCO3-)= 0.1 mol·L-1的溶液中:NH4+、Al3+、Cl-、NO3-
B、在由水电离出的c(H+)= 1×10-12 mol·L-1的溶液中:Fe3+、ClO-、Na+、SO42-
C、在pH = 1的溶液中:NO3-、SO42-、Na+、K+
D、在pH = 13的溶液中:SO32-、S2-、Na+、K+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com