
题目列表(包括答案和解析)
18.分子式为C4H10O并能与金属钠发生反应的物质有
A.3种 B.4种 C.5种 D.6种
17.(10分)烃X是一种重要的化工原料。X能使Br2的四氯化碳溶液褪色,它的密度是同温同压下氢气密度的21倍。由烃X经下列反应可制得A-F等多种有机物。
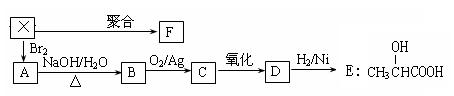
已知:RCH2Br + NaOH → RCH2OH + NaBr
⑴烃X的结构简式为 ,F的结构简式为 。
⑵由X→A、B→C的反应类型分别为 、 。
⑶B转化为C的化学方程式: ;
⑷在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物G,G的结构简式为: 。
以下是选考题,其中第18、19、20、21题为《有机化学基础》模块题,第22、23、24、25题为(物质结构与性质》模块题,第26、27、28、29题为《化学与技术》模块题。考生只能从三个模块中任选一个作答,不得跨模块答题,否则只能以所答的第一个模块计分。
《有机化学基础》模块
18-20为选择题,每小题只有一个正确选项,每小题3分
16.(12分).某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。
⑴方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。实验中加热至恒重的目的是____________。
⑵方案二:按下图装置进行实验。并回答以下问题。

①实验前先_____________________。分液漏斗中应该装_____(盐酸或硫酸)。D装置的作用是______________________________________。
②实验中除称量样品质量外,还需称__________________装置前后质量的变化。
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显缺陷,该缺陷是 _______________________________________________。
⑶方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯,漏斗外还用到的玻璃仪器有_______________。
②实验中判断沉淀是否完全的方法是____________________________。
③如加入试剂改为氢氧化钡,已知称得样品10.5g,干燥的沉淀质量为19.7g,测样品中碳酸钠的质量分数为____________。
15.(8分) 在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.020 |
0.01. |
0.008 |
0.007 |
0.007 |
0.007 |
⑴写出该反应的平衡常数表达式:K= 。
 已知:
已知: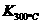 >
> ,则正反应是 热反应。
,则正反应是 热反应。
⑵右图中表示NO2的变化的曲线是 。
用O2表示从0-2s内该反应的平均速率v= 。
⑶能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正 (O2) d.容器内密度保持不变
⑷为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
14.(10分)中学化学中几种常见物质的转化关系如下:

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
⑴红褐色胶体E粒子直径大小的范围: 。
⑵A、B、H的化学式:A ,B ,H 。
⑶①H2O2分子的电子式
②写出C的酸性溶液与双氧水反应的离子方程式: 。
⑷写出鉴定E中阳离子的实验方法和现象: 。
13.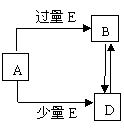 (8分)已知A、B、D、E均为中学化学常见单质或化合物,它
(8分)已知A、B、D、E均为中学化学常见单质或化合物,它
们之间的关系如图所示(部分产物略去)。
⑴若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
① B属于 分子(填“极性”或“非极性”),电子式为 ;
②4 g A单质完全燃烧放出131.2 kJ的热量,写出表示A单质燃烧热的热化学方程式 ;
⑵若A为第三周期中的元素所形成的氯化物。
① 写出A溶液→B的离子方程式 ;
② 写出A和B的溶液反应的离子方程式
12.下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1mol·L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c (OH-)
B.0.1mol·L-1的NaHCO3溶液中:c(Na+) = c(HCO3-) + c(H2CO3)+ 2c(CO32-)
C.0.1mol·L-1的NH4Cl溶液与0.05mol·L-1的NaOH溶液等体积混合:
c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2CO3]<c( NH4Cl)
第Ⅱ卷
本卷包括必考题和选考题两部分。第13题-第17题为必考题,每个试题考生都必须做答。第18题-第29题为选考题,考生根据要求做答。
11. 用铅蓄电池电解苦卤水 (含C1-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中正确的是
用铅蓄电池电解苦卤水 (含C1-、Br-、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中正确的是
A.铅蓄电池放电时,溶液的PH值变小
B.铅蓄电池负极的反应式为:Pb -2e-+SO42- = PbSO4
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a 电极首先放电的是 H+
10.下列离子方程式正确的是
A.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-===BaSO4↓+NH3·H2O+ H2O
B.澄清石灰水与稀盐酸反应:Ca(OH)2+2H+===Ca2++2H2O
C.钠与水反应:Na+2H2O===Na++2OH-+H2↑
D.碳酸钡中加入稀硫酸:BaCO3+2H+===Ba2++CO2↑+H2O
9.某些化学键键能数据如下:
|
化学键 |
H-H |
C1-Cl |
H-Cl |
键能 |
436 |
243 |
431 |
则下列热化学方程式不正确
A. H2(g)+
H2(g)+  Cl2(g)
Cl2(g) HCl(g);
HCl(g); = -91.5
= -91.5
B. H2(g)+ Cl2(g) 2HCl(g);
2HCl(g); = -183
= -183
C. H2(g)+
H2(g)+  Cl2(g)
Cl2(g) HCl(g);
HCl(g); = +91.5
= +91.5
D.2HCl(g) H2(g)+ Cl2(g);
H2(g)+ Cl2(g); = +183
= +183
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com