
题目列表(包括答案和解析)
11.下列反应的离子方程式正确的是
A.在H2C2O4中加入酸性KMnO4溶液:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
B.铁跟盐酸反应:2Fe+6H+=2Fe3++3H2↑
C.氯化铝溶液与过量的氨水反应:Al3++4NH3·H2O= AlO2-+4NH4++2H2O
D.表示HS-电离的方程式为:HS-+H2O  S2-+H3O+
S2-+H3O+
10.NA代表阿伏加德罗常数,下列说法正确的是
A.1 L pH为3的FeCl3溶液中,由水电离产生的H+离子数目为0.1NA
B.乙烯和丙烯的混合物1.4g中含有0.1NA个碳原子
C.标准状况下,22.4L 甲苯所含的分子数约为6.02×1023
D.0.1mol甲基(-CH3)所含电子数为0.8NA
9.常温下,加水稀释时c(H+)/c(OH-)值明显增大的溶液中,一定能大量共存的离子组是
① K+、Cl-、NO3-、AlO2- ② K+、Fe2+、I-、SO42- ③ Ba2+、Cl-、NO3-、Na+ ④Na+、Ca2+、Al3+、 Cl-
A.①② B.①③ C.②④ D.②③
8.某实验报告记录了如下数据,其中数据合理的是
A.用广泛试纸测得氯水的pH值为2.1 B.用50mL量筒量取23.00 mL浓盐酸
C.用温度计测量出酒精的沸点为78.5℃ D.用托盘天平称量氧化铜粉末为11.70g
7.高温及一定催化剂作用下,某反应达平衡,平衡常数K=。恒容时,温度升高,H2 浓度减小。下列说法正确的是
A.将容器体积变为原来2倍,CO的平衡浓度变为原来的2倍
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为CO2 + H2催化剂高温CO + H2O ;△H>0
6.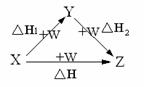 X、Y、Z、W有如右图所示的转化关系,已知焓变:△H=△H1+△H2, 则X、Y可能是:①C、CO ②AlCl3 、Al(OH)3 ③Fe 、Fe(NO3)2 ④Na2CO3 、NaHCO3
X、Y、Z、W有如右图所示的转化关系,已知焓变:△H=△H1+△H2, 则X、Y可能是:①C、CO ②AlCl3 、Al(OH)3 ③Fe 、Fe(NO3)2 ④Na2CO3 、NaHCO3
A.①②③④ B.①② C.③④ D.①②③
5.目前市场上的手提应急灯,主要是“无液干粉”铅酸蓄电池,其原理是将有腐蚀性的浓硫酸灌注到硅胶凝胶中去,使电解质溶液不易发生泄漏,大大改善了电池的性能。所用的原料仍然是铅--二氧化铅--硫酸。下列关于该铅酸蓄电池的说法正确的是
A.充电时电源的正极接蓄电池标“+”的一极
B.“无液干粉”铅酸蓄电池彻底改变了原来的铅酸蓄电池的反应原理
C.放电时在铅酸蓄电池的负极发生还原反应
D.充电时铅酸蓄电池上标有“-”的电极发生氧化反应
4.下列实验操作完全正确的是
|
编号 |
实 验 |
操 作 |
|
A |
钠与水反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
|
B |
配制一定物质的量浓度的氯化钾溶液1000 mL |
准确称取氯化钾固体,放入到1000 mL的容量瓶中,加水溶解,振荡摇匀,定容 |
|
C |
排除碱式滴定管尖嘴部分的气泡 |
将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
|
D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
3.信息、材料、能源被称为新科技革命的“三大支柱”。下列观点或做法错误的是
A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B.加大煤炭的开采速度,增加煤炭燃料的供应量,以缓解石油危机
C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅
D.高温结构陶瓷氮化硅(Si3N4)具有较高的硬度和耐磨性,可用于制造汽车发动机
2.油脂是主要营养物质之一,也是一种重要的化工原料。下列说法中,正确的是
A.油脂在酸性条件下水解生成甘油和肥皂
B.植物油氢化后可用作人造奶油
C.植物油不能使溴的四氯化碳溶液褪色
D.判断油脂皂化反应是否完成的方法是静置反应混合物,观察其是否分层
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com