
题目列表(包括答案和解析)
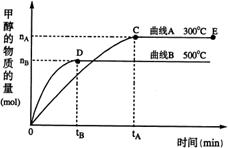
20.(8分)一定条件下,在体积为3 L的密闭容器中, 一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)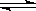 CH3OH(g)
CH3OH(g)
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K= , 升高温度,K值 (填“增大”、“减小”或“不变”);
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)= ;
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是 (填字母序号)。
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
19.(8分)乙基香草醛( 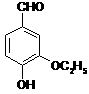 )是食品添加剂的增香原料,其香味比香草醛更加浓郁。
)是食品添加剂的增香原料,其香味比香草醛更加浓郁。
⑴写出乙基香草醛分子中两种含氧官能团的名称 。
⑵乙基香草醛的同分异构体A是一种有机酸,A可发生以下变化:
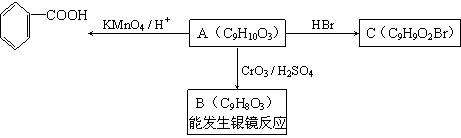
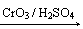
提示:①RCH2OH RCHO
②与苯环直接相连的碳原子上有氢时,此碳原子才可被酸性KMnO4溶液氧化为羧基
(a)由A→C的反应属于 (填反应类型)。
(b)写出A的结构简式 。
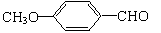
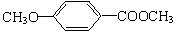 ⑶乙基香草醛的另一种同分异构体D(
)是一种医药中间体。请设计
⑶乙基香草醛的另一种同分异构体D(
)是一种医药中间体。请设计
合理方案用茴香醛( )合成D(其他原料自选,用反应流程图表示,并注明必要的反应条件)。
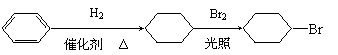 例如,
例如,
五。、本题包含1小题,共计8分
18.(10分)2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁·沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献。蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%-18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法。其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机
含氮化合物,反应式为:2(-NH2)+H2SO4+2H+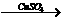 。
。
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7。
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量。
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为 。
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋
 白质的含量则为6.38%。不法分子通过在低蛋白含量的奶粉
白质的含量则为6.38%。不法分子通过在低蛋白含量的奶粉
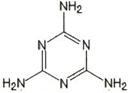
中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,
导致许多婴幼儿肾结石。
① 三聚氰胺的结构如图所示,其化学式为 ,
含氮量(氮元素的质量分数)为 ;
② 下列关于三聚氰胺的说法中,正确的有 ;
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③ 假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白
质含量为0的假奶粉中掺入 g的三聚氰胺就可使奶粉“达标”。
17.(12分)已知C、D、E、H为气体,反应①是工业生产中的重要反应,反应④⑥⑧是实验室重要的物质检验反应,这些物质有如图所示的转化关系(生成物中的水均已略出)。
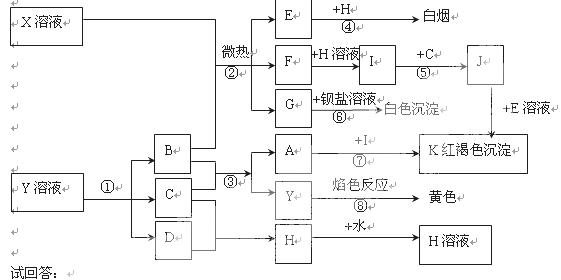
(1)写出化学式:K: H:
(2)反应⑦中A溶液显示的性质是 (填序号:A.氧化性;B.还原性;C酸性;D.碱性)
(3)若X是一种复盐(不考虑结晶水),X的化学式为: 。
(4)写出下列反应的离子方程式:
反应② ;
反应③ ;
反应⑤ 。
16.(12分)某化学研究性学习小组探讨Fe3+和SO32-之间发生怎样的反应,请你一起参与并协助他们完成实验。
(1)提出猜想:
甲同学认为发生双水解反应:Fe3++ SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3
乙同学认为发生氧化还原反应,其反应方程式为
(2)实验验证:丙同学设计了下列实验来探究反应的可能性。
①为了检验所用的Na2SO3是否变质,应选用的试剂是
②取5mLFeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红棕色(无气泡产生,也无沉淀生成)
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变为血红色
(3)得出结论:
①根据丙同学的实验得出的结论是:
②实验③中溶液变成血红色的离子方程式为
(4)拓展探究:
丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体。从形式上看,Na2CO3 和Na2SO3相似,但二者的水溶液与氯化铁溶液反应的现象差别很大,其原因是
15.(10分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用.
(1).下列关于实验的叙述正确的有 .
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.滴定用的锥形瓶和滴定管都要用所盛溶液润洗
C.测量溶液的pH时,应先将pH试纸润湿
D.用溴水除去乙烯中混有的二氧化硫气体
E.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
F.附着于试管内壁上的硫,可用热碱液洗涤
G.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在玻璃棒搅拌下慢慢加入浓硫酸
H.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
(2).下列实验没有错误的是 .
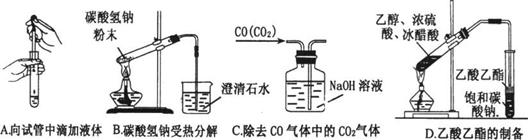
(3).下图为常见仪器的部分结构(有的仪器被放大)
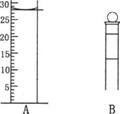
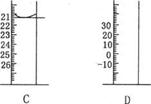
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为N mL,仰视时读数为M mL,若M>N,则所使用的仪器是 (填字母标号).
14.在密闭容器中,将1.0 mol CO与1.0 mol
H2O混合加热到800℃,发生下列反应:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
一段时间后该反应达到平衡,测得CO的物质的量为0.5 mol。则下列说法正确的是
A.800℃下,该反应的化学平衡常数为0.25
B.427℃时该反应的平衡常数为9.4,则该反应的△H<0
C.同温下,若继续向该平衡体系中通入1.0 mol的CO(g),则平衡时CO物质的量分数为33.3%
D.同温下,若继续向该平衡体系中通入1.0 mol的H2O(g),则平衡时CO转化率为66.7%
第II卷 非选择题(共72分)
13.下列操作会使H2O的电离平衡向电离方向移动,且pH<7的是
A.向水中加少量Na2CO3 B.向水中加少量FeCl3
C.向水中加少量NaHSO4 D.将纯水加热到90℃
12.室温时,下列混合溶液的pH一定小于7的是
A.pH=3的盐酸和pH=11的氨水等体积混合
B.pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合
C.pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合
D.pH=3的硫酸和pH=11的氨水等体积混合
11.设NA为阿伏加德罗常数,下列叙述中正确的是
A.14g乙烯和丙烯的混合物中总原子数为3NA个
B.常温下11.2L的甲烷气体含有甲烷分子数为0.5NA个
C.0.1mol/L的氢氧化钠溶液中含钠离子数为0.1NA个
D.5.6g铁与足量的稀硫酸反应失去电子数为0.3NA个
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com