
题目列表(包括答案和解析)
18、通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)目前,用超临界CO2(其状态介于气态和液态之间)代替氟利昂作致冷剂已成为一种趋势,这一做法对环境的积极意义在于 _____。
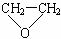 (2)利用二氧化碳制造全降解塑料,可以缓解温室效应。已知过氧键(
(2)利用二氧化碳制造全降解塑料,可以缓解温室效应。已知过氧键(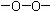 )不稳定,请写出环氧乙烷(
)与CO2通过加聚制造全降解塑料的化学方程式:
)不稳定,请写出环氧乙烷(
)与CO2通过加聚制造全降解塑料的化学方程式:
。
(3)CCTV《科技博览》报道:2004年3月中科院首创用CO2合成可降解塑料聚二氧化碳(CO2)n。下列相关说法合理的是 。
A.聚二氧化碳塑料是通过加聚反应制得的
B.聚二氧化碳塑料与干冰互为同分异构体
C.聚二氧化碳塑料与干冰都是纯净物
D.聚二氧化碳塑料的使用会产生白色污染
(4)最近有科学家提出“绿色自由”构想:把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
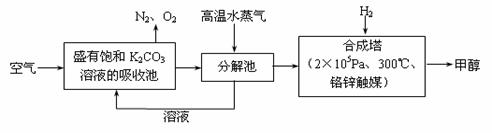
①分解池中反应的化学方程式为_ _。
②在合成塔中,若有4.4kgCO2与足量H2恰好完全反应,可放出4947 kJ的热量,试写出合成塔中发生反应的热化学方程式_ _。
(5)小李同学拟用沉淀法测定空气中CO2的体积分数,为了提高测量的精确度,小李应该选用的试剂为____ _(填序号)。
A.Ca(OH)2 B.Ba(OH)2 C.BaCl2 D. BaCl2和NaOH
17.氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1) 氢气燃烧热值高。实验测得,在常温常压下,1gH2完全燃烧生成液态水,放出142.9 kJ 热量。则H2燃烧的热化学方程式为 ▲ 。
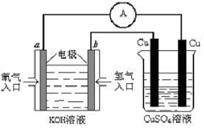 (2)氢氧燃料电池具有广阔的发展前景。右图所示的氢氧燃料电池中,电池负极的反应式是 ▲ 。
(2)氢氧燃料电池具有广阔的发展前景。右图所示的氢氧燃料电池中,电池负极的反应式是 ▲ 。
(3)氢气是合成氨的重要原料。工业上合成氨的反应是:N2(g)
+ 3H2(g) 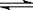 2NH3(g);ΔH= -92.2 kJ·mol-1。
2NH3(g);ΔH= -92.2 kJ·mol-1。
①一定条件下,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中加入催化剂引起反应速率变化的时间段是 ▲ (填,如0-t1等)。
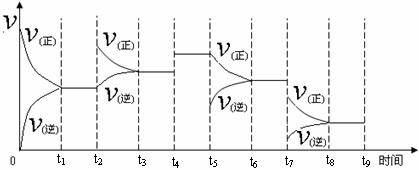 ②温度为T℃时,将2amolH2和amolN2放入0 . 5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该温度下反应的平衡常数为 ▲ (用含a的代数式表示)。
②温度为T℃时,将2amolH2和amolN2放入0 . 5L密闭容器中,充分反应后测得N2的转化率为50﹪。则该温度下反应的平衡常数为 ▲ (用含a的代数式表示)。
(4)工业上生产氢气是将水蒸气通过红热的炭,产生水煤气:
C(s)
+ H2O(g) 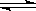 H2(g) + CO(g) △H = +131.3 kJ/mol
H2(g) + CO(g) △H = +131.3 kJ/mol
该反应在低温下不能自发进行的原因是 ▲ 。
A.△H >0 B.温度较低时,△H影响为主
C.△S<0 D.温度较低时,△S影响为主
16.下图是无机物A-M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是第三周期半径最小的金属元素组成的单质,K是一种红棕色气体。
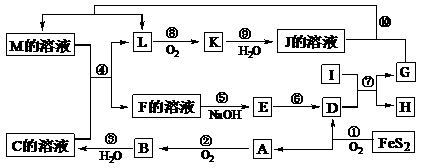
请填写下列空白:
(1)A的化学式为 ,I的原子结构示意图为 。
(2)在周期表中,组成单质G的元素在周期表中的位置是___________________________。
(3)写出反应⑦的化学方程式 当有0.3 mol电子转移时,生成G的物质的量为 。
(4)在反应②、③、⑥、⑨中,既属于化合反应又能属于非氧化还原反应的是____________(填写序号)。
(5)反应④的离子方程式是:____________________________________________。
(6)将化合物D与KNO3、KOH混合,在高温条件下可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:
15、某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀。
甲同学认为沉淀可能是CuCO3;
乙同学认为沉淀可能是Cu(OH)2;
丙同学认为沉淀可能是CuCO3和Cu(OH)2的混合物。(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.(1)乙同学的观点,你认为其原理是 ▲ ;
(2)在探究沉淀成分前,须将沉淀从溶液中过滤、洗涤、低温干燥,检验沉淀是否洗涤干净的方法是 ▲ 。
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分。
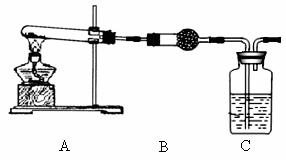
(3)B装置中试剂的化学式是 ▲ ,
C装置中试剂的名称是 ▲ 。
(4)能证明乙同学观点正确的实验现象是 ▲ 。
(5) 若丙同学的观点正确,用上述装置通过B、C中质量的增加来定量测定沉淀的组成,请你说说该装置主要存在的缺点 ▲ (至少二点)
14、向某NaOH溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的 关系有下列图示四种情况,且(2)、(3)、(4)图中分别有OA<AB,OA=AB,OA>AB, 则下列分析与判断不正确的是(不计CO2的溶解)
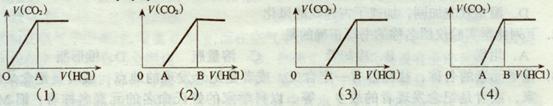 A.M中只有一种溶质的有(1)和(3) B.M中有两种溶质的有(2)和(4)
A.M中只有一种溶质的有(1)和(3) B.M中有两种溶质的有(2)和(4)
C.(2)图显示M中c(NaHCO3)>c(Na2CO3) D.(4)图显示M中c(NaHCO3)>c(Na2CO3)
第二卷(非选择题 共72分)
13、用某氢氧燃料电池(用氢氧化钾水溶液为电解质溶液)电解饱和亚硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极。下列说法正确的是
A.当燃料电池正极消耗mg气体时,电解池阴极同时有mg气体生成
B.电解池的阳极反应式为: 4OH--4e-=O2↑+2H2
C.电解池中溶液pH变小
D.燃料电池中溶液pH变大
12、下列离子方程式的书写正确的是
A.实验室用浓盐酸与MnO2反应制Cl2:
MnO2 +4HCl(浓) Cl2↑+Mn2+ +2Cl-+2H2O
Cl2↑+Mn2+ +2Cl-+2H2O
B.将标准状况下1.12 L氯气通入10 mL 1 mol / L的溴化亚铁溶液中:
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
C.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:
Ca2++ HCO3- +OH- =CaCO3↓+H2O
D.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+ =BaSO4↓+ NH3·H2O +H2O
11、羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸反应制得。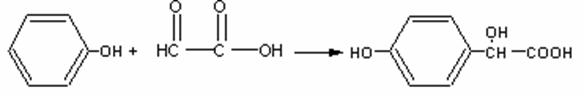

(羟基扁桃酸)
下列有关说法正确的是
A.苯酚和羟基扁桃酸互为同系物
B.常温下,1mol羟基扁桃酸只能与1molBr2反应
C.乙醛酸在核磁共振氢谱中只有1个吸收峰
D.羟基扁桃酸分子中至少有12个原子共平面
10、下列比较中,正确的是
A.同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液大
B.0.2 mol ·L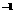 NH4Cl和0.1 mol·L
NH4Cl和0.1 mol·L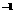 NaOH溶液等体积混合后:
NaOH溶液等体积混合后:
c(NH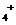 )>c(Cl
)>c(Cl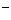 )>c(Na
)>c(Na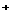 )>c(OH
)>c(OH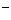 )>c(H
)>c(H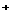 )
)
C.物质的量浓度相等的H2S和HaHS混合溶液中:
c(Na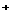 )+c(H
)+c(H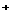 )=c(S
)=c(S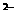 )+c(HS
)+c(HS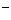 )+c(OH
)+c(OH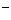 )
)
D.同浓度的下列溶液中,①NH2Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH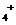 )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④
9、根据下列实验现象,所得结论正确的是
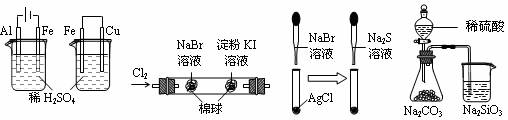
A. B. C. D.
|
实验 |
实验现象 |
结论 |
|
A. |
左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
|
B. |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
|
C. |
白色固体先变为淡黄色,后变为黑色(Ag2S) |
Ksp:AgCl>AgBr>Ag2S |
|
D. |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:S>C>Si |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com