
题目列表(包括答案和解析)
20.(12分)某溶液中可能含有SO32-、SO42-、 HCO3- 三种离子中的两种或三种。为探究其组成,小明取出两份相同的样品溶液于试管中,向一份中加入过量的盐酸,产生无色气泡;向另一份中滴加过量的氯化钡溶液,产生白色沉淀。请设计合理实验,做进一步的探究,对小明的实验给出结论。
仅限选择的仪器、用品和试剂:烧杯、试管、玻璃棒、胶头滴管、量筒、集气瓶、铁架台、漏斗、滤纸、酒精灯、带单孔胶塞的导管;lmol/L硫酸;2mol/L盐酸;2mol/L硝酸、;lmol/L氯化钡、澄清石灰水、品红溶液、蒸馏水。
完成下列探究过程:
(l)提出假设:
假设 l :溶液中存在SO32-、SO42- 假设 2 :
假设 3 : 假设 4 :溶液中存在SO32-、SO42-、 HCO3-
(2) 基于假设4 , 设计出实验方案,将实验操作、预期的实验现象和结论填在下表中。
[提示]I、在答题卡上按照下表的方式作答,注意前后内容的对应。
Ⅱ、注意文字简洁,超出答题卡空间视为无效。
III 、可不填满,也可增加步骤。
|
步骤编号 |
实验操作 |
预期现象和结论 |
|
① |
|
|
|
② |
|
|
|
③ |
|
|
|
④ |
|
|
|
…… |
…… |
…… |
19.(10分)已探明我国锰矿储量占世界第三位,但富矿仅占6.4%,每年尚需进口大量锰矿石。有人设计了把我国的贫菱锰矿(MnCO3含量较低)转化为高品位“菱锰矿砂”(MnCO3含量高)的绿色工艺。该工艺流程如下图所示:

已知焙烧反应①的化学方程式:(NH4)2SO4+MnCO3MnSO4+2NH3↑+CO2↑+H2O。
(1)写出反应②的离子方程式_______________________________________。
(2)上述工艺流程中,可以循环利用的物质有(NH4)2SO4、____________、__________。从物料平衡角度看,理论上生产过程中_________(填“需要”或者“不需要”)添加(NH4)2SO4。
(3)向物质的量浓度均为0.01mol·L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的是________(填离子符号);当两种沉淀共存时,溶液中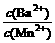 =________。
=________。
[Ksp(BaCO3)=8.1×10-9,Ksp(MnCO3)=1.8×10-11]
18.在一密闭容器中有如下反应:aX(g)+bY(g) 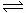 nW(g);ΔH=Q。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g);ΔH=Q。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
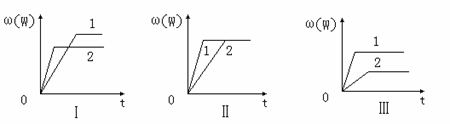 其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析可能正确的是
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b<n
B.图Ⅲ可能是不同温度对反应的影响,且T1>T2,ΔH<0
C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b
D.图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好
第Ⅱ卷(共87分)
17.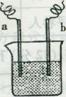 右图中,两电极上发生的电极反应为: a极:Cu2++2e一=Cu b极:Fe一2e一=Fe2+,下列说法中不正确的是( )
右图中,两电极上发生的电极反应为: a极:Cu2++2e一=Cu b极:Fe一2e一=Fe2+,下列说法中不正确的是( )
A.该装置可能是电解池
B.a极上发生的是氧化反应
C.a、b可能是同种电极材料
D.该装置在工作时,溶液中的阳离子可能向b极移动
16.下列溶液中有关物质的量浓度关系正确的是
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:
c(H+) + c(M+) == c(OH-) + c(A-)
B. pH相等的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) +2c(OH-) == 2c(H+) + c(CH3COOH)
D.0.1mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
15.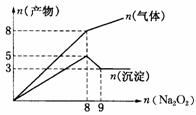 将
将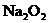 逐渐加入到含有
逐渐加入到含有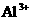 、
、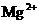 、
、 的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入
的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入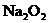 的物质的量(mol)的关系如图所示,则原溶液中
的物质的量(mol)的关系如图所示,则原溶液中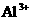 、
、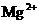 、
、 的物质的量分别为
的物质的量分别为
A.2 mol、3 mol、8 mol
B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol
D.3 mol、2 mol、4 mol
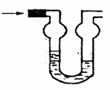
14.双球洗气管是一种多用途仪器,常用于除杂质、气体干燥、气体吸收(能防止倒吸)等实验操作。右图是用水吸收下列某种气体时的情形,根据下表数据判断由左方进入的被吸收气体是
 A.Cl2
B.HCl
C.H2S
D.CO2
A.Cl2
B.HCl
C.H2S
D.CO2
|
气 体 |
Cl2 |
HCl |
H2S |
CO2 |
|
1体积水约能吸收气体体积数 |
2 |
500 |
2.6 |
1 |
13.下列离子方程式正确的是
A.碳酸钠溶液显碱性:CO32-
+ 2H2O  H2CO3
+2OH-
H2CO3
+2OH-
B.过量铁粉溶于稀硝酸中:Fe + 4H+ + NO3- == Fe3+ + NO↑+ 2H2O
C.电解精炼铜的阴极反应是:Cu2++2e-=Cu
D.向次氯酸钙溶液中通入少量二氧化硫:
Ca2++ClO-+SO2+H2O CaSO3+2HClO
CaSO3+2HClO
12.a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为
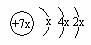
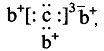 ,b与c形成化合物的电子式为下列比较中正确的是
,b与c形成化合物的电子式为下列比较中正确的是
A.原子半径:a>c>d>b B.最高价含氧酸的酸性c>d>a
C.原子序数:a>d>b>c D.单质的氧化性a>b>d>c
11.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.1mol金刚石晶体中含碳碳键数为2 NA
B.常温常压下,22.4L的D2、H2组成的气体分子数为NA
C. 100 mL 0.5 mol/L的(NH4)2SO4溶液中,含有0.1NA个NH4+
D.1molNa2O2与足量CO2反应转移的电子数NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com