
题目列表(包括答案和解析)
2、掌握愿电池的形成条件
知识点:
1、 掌握原电池的工作原理
7.(1)①铁屑 ②稀硫酸 ③稀硝酸 ④氢氧化钠 ⑤氢氧化钠
(2)Fe+2H+=Fe2++H2↑ 2Fe3++Fe=3Fe2+ Cu2++Fe=Cu+Fe2+ 2Au3++3Fe=2Au+3Fe2+
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(3)Fe2O3 用作红色涂料
6.(1)CaCO3+2HCl=CaCl2+H2O+CO2↑
(2)
|
仪器 |
加入试剂 |
加入该试剂的目的 |
|
B |
(饱和NaHCO3溶液) |
除去CO2气体中混入的HCl |
|
C |
过氧化钠 |
与CO2和水气反应,产生O2 |
|
D |
NaOH溶液 |
吸收未反应的CO2气体 |
(注:C中实际加入过过氧化钠和石棉绒得混合物,这里只要求填写化学试剂)
(3)2Na2O2+2CO2==2Na2CO3+O2
5.(1)Al C Na2O2 (2) 2H2O +Na2O2 =4NaOH+O2↑ 2Al+ 2NaOH+2H2O=2NaAlO2+3H2↑
(3) CO2 CO (4) Na2CO3 (5) 2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
4.⑴Cu、O; ⑵b、c;
⑶2Fe3++2I-=2Fe2++I2;S2O82-+2Fe2+=2SO42-+2Fe3+;(离子方程式不配平不扣分)
⑷a:2Al3++4OH-=AlO2-+2H2O[或Al3++4OH-=Al(OH)4-];b:稀硫酸、KMnO4溶液;稀硫酸浸取炉渣所得溶液使KMnO4溶液褪色
3.(1)H2+S H2S(写成可逆反应也正确)
(2)H2SO3
+ 2H2S=3S + 3H2O
H2S(写成可逆反应也正确)
(2)H2SO3
+ 2H2S=3S + 3H2O
(3)C+2H2SO4(浓) CO2
↑+2SO2 ↑+2H2O或Cu+ 2H2SO4(浓)
CO2
↑+2SO2 ↑+2H2O或Cu+ 2H2SO4(浓) CuSO4
+SO2 ↑+ 2H2O等
CuSO4
+SO2 ↑+ 2H2O等
(4)①H2SO3 +2OH- = SO32- + 2H2O
②大于;Na2SO3溶液中SO32-发生水解使溶液显碱性。
③增大;升高温度促进Na2SO3溶液的水解。
2. (1)①KI+IBr==KBr+I2 ②C6H6+ICl→C6H5I+HCl;或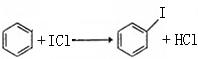
1.
 (1)AsH3
(1)AsH3 (2)Br2
(2)Br2 (3)a c
(3)a c  (4)
(4) 
7.(2008,宁夏)某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。

填写下面空白。
(1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ ;
(2)写出①处发生反应的离子方程式 ;写出③处发生反应的化学方程式 ;
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:
铁红 。
高三化学元素化合物测试
Ⅱ卷(填空题)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com