
题目列表(包括答案和解析)
10.(2010年全国1)下列叙述正确的是
A.若醋酸溶液的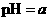 ,将此溶液稀释1倍后,溶液的
,将此溶液稀释1倍后,溶液的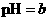 ,则
,则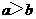
B.在滴有酚酞溶液的氨水里,加入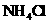 至溶液恰好无色,则此时溶液的
至溶液恰好无色,则此时溶液的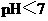
C.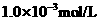 盐酸的
盐酸的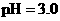 ,
,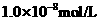 盐酸的
盐酸的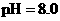
D.若1mL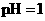 的盐酸与100mL
的盐酸与100mL 溶液混合后,溶液的
溶液混合后,溶液的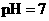 ,则
,则 溶液的
溶液的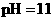


 w_w w. k#s5_
w_w w. k#s5_
解析:若是稀醋酸溶液稀释则C(H+)减小,pH增大,b>a,故A错误;酚酞的变色范围是pH= 8.0-10.0(无色→红色),现在使红色褪去,pH不一定小于7,可能在7~8之间,故B错误;常温下酸的pH不可能大于7,只能无限的接近7;D正确,直接代入计算可得是正确,也可用一般的式子:设强酸pH=a,体积为V1;强碱的pH=b,体积为V2,则有10-aV1=10-(14-b)V2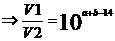 ,现在V1/V2=10-2,又知a=1,所以b=11
,现在V1/V2=10-2,又知a=1,所以b=11
答案:D
9.(2010年全国1)下列叙述正确的是

 w_w w. k#s5_
w_w w. k#s5_
A.Li在氧气中燃烧主要生成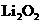
B.将SO2通入 溶液可生成
溶液可生成 沉淀
沉淀
C.将CO2通入次氯酸钙溶液可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
解析:A错误,因为Li在空气中燃烧只能生成Li2O; B错误,酸性:HCl>H2SO3>H2CO3,所以通入后无BaSO3沉淀,因为BaSO3+2HCl=BaCl2+H2O+SO2↑;D错误,溶液中该反应难以发生,先是:2NH3+2H2O+CuSO4=Cu(OH)2↓+(NH4)2SO4,接着Cu(OH)2 CuO+H2O溶液中NH3不能还原CuO为Cu,要还原必须是干燥的固态!C正确,强酸制弱酸,酸性:H2CO3>HClO,反应为:CO2+H20+Ca(ClO)2=CaCO3↓+2HclO。
CuO+H2O溶液中NH3不能还原CuO为Cu,要还原必须是干燥的固态!C正确,强酸制弱酸,酸性:H2CO3>HClO,反应为:CO2+H20+Ca(ClO)2=CaCO3↓+2HclO。
答案:C
8.(2010年四川)有关①100ml 0.1 mol/L  、②100ml 0.1 mol/L
、②100ml 0.1 mol/L 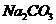 两种溶液的叙述不正确的是
两种溶液的叙述不正确的是

 w_w w. k#s5_
w_w w. k#s5_
A.溶液中水电离出的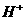 个数:②>①
个数:②>①
B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中: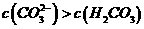
D.②溶液中: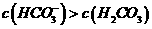
解析:本题考查盐类水解知识;盐类水解促进水的电离,且Na2CO3的水解程度更大,碱性更强,故水中电离出的H+个数更多,A项正确;②中钠离子的物质的量浓度为0.2 mol/L,而①中钠离子的物质的量浓度为0.1 mol/L根据物料守恒及电荷守恒可知溶液中阴离子的物质的量浓度之和:②>①,B项正确;NaHCO3水解程度大于电离程度所以C(H2CO3)>C(CO32-),C错误;C032-分步水解且第一步水解占主要地位,所以C(HCO3-) >C(H2CO3),D正确。
答案: C w w
7.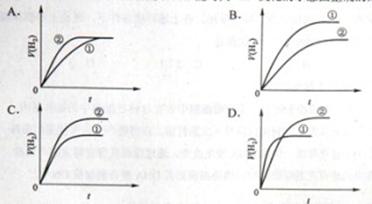 (2010年全国2) 相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
(2010年全国2) 相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

 w_w w. k#s5_
w_w w. k#s5_
解析:在相同体积、相同pH的情况下,根据电离平衡的知识可以得出一元强酸溶液①的物质的量小于一元中强酸溶液②物质的量,因此②放出的氢气多;在反应过程中②中H+的物质的量浓度始终大于①中的H+的物质的量浓度,所以溶液②中的反应速率大于溶液①的反应速率。因此选项C正确。
答案:C
6.(2010年全国2) 在相同条件下,下列说法错误的是

 w_w w. k#s5_
w_w w. k#s5_
A.氯气在饱和食盐水中的溶解度小于在纯水中的溶解度
B.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
C.醋酸在醋酸钠溶液中电离的程度大于在纯水中电离的程度
D.工业上生产硫酸的过程中使用过量的空气可提高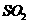 的利用率
的利用率
解析:饱和食盐水中CI-浓度大,可以降低氯气的溶解度,A正确;碘与碘化钾可以发生如下变化:I2+KI=KI3,B正确;醋酸钠溶液中大量的醋酸根离子可以抑制醋酸电离,C错误;使用过量的空气就是增大氧气的浓度从而可以提高SO2的利用率,D正确。
答案:C
5.(2010年北京)下列解释实验事实的方程式不正确的是

 w_w w. k#s5_
w_w w. k#s5_
A.0.1 /L
/L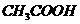 溶液的PH>1:
溶液的PH>1:
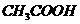
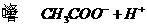
B.“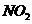 球”浸泡在冷水中,颜色变浅:2
球”浸泡在冷水中,颜色变浅:2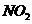 (g)
(g)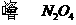 (g)△H<0
(g)△H<0
(红棕色) (无色)
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2N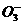 =3Fe2++2NO↑+4H2O
=3Fe2++2NO↑+4H2O
D.向Na2CO3溶液中滴入酚酞溶液,溶液变红:
解析:醋酸是弱酸存在电离平衡,A正确;正反应是放热反应温度降低平衡正向移动,颜色变浅,B正确;铁溶于稀硝酸,溶液变黄,是因为有Fe3+生成,C错误,正确的写法是:Fe+4H++N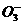 =Fe3++NO↑+2H2O;Na2CO3水解溶液显碱性,D正确。
=Fe3++NO↑+2H2O;Na2CO3水解溶液显碱性,D正确。
答案:C
4.(2010年山东)某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液PH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
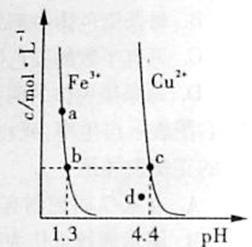 A.
A.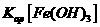 <
<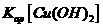
B.加适量NH4Cl固体可使溶液由a 点变到b点
C.c 、d两点代表的溶液中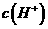 与
与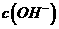 乘积相等
乘积相等
D.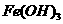 、
、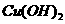 分别在b、c两点代表的溶液中达到饱和
分别在b、c两点代表的溶液中达到饱和

 w_w w. k#s5_
w_w w. k#s5_
解析:由题意知当金属阳离子浓度相等时,溶液中OH-的浓度分别为10-12.7和10-9.6,若设金属阳离子浓度为x,则Ksp[Fe(OH)3]=x·(10-12.7)3,Ksp[Cu(OH)2]=x·(10-96)3,显然Ksp[Fe(OH)3]<Ksp[Cu(OH)2],A正确;a 点变到b点溶液思维酸性减弱,但NH4Cl溶于水是显酸性的,因此B错误;只要温度不变Kw就是不变的,C正确;溶度积曲线上的每一点都代表饱和点,而b、c两点分别在曲线上,所以此时溶液达到饱和,曲线左下方的是不饱和点,右上方的是过饱和点,D正确。
答案:B
3.(2010年天津)下列液体均处于25℃,有关叙述正确的是

 w_w w. k#s5_
w_w w. k#s5_
A.某物质的溶液pH < 7,则该物质一定是酸或强酸弱碱盐
B.pH = 4.5的番茄汁中c(H+)是pH = 6.5的牛奶中c(H+)的100倍
C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
D.pH = 5.6的CH3COOH与CH3COONa混合溶液中,c(Na+) > c(CH3COO-)
解析:某些强酸的酸式盐如NaHSO4其pH<7,故A错;pH=4.5,c(H+)=10-4.5 mol·L-1,pH=6.5,其c(H+)=10-6.5 mol·L-1,故B正确;同浓度的CaCl2溶液的c(Cl-)是NaCl的两倍,它们对AgCl沉淀溶解平衡的抑制程度不同,故C错;混合溶液显酸性,则c(H+)>c(OH-),根据电荷守恒,c(CH3COO-)>c(Na+),故D错。
答案:B
2.(2010年天津)下列各表述与示意图一致的是

 w_w w. k#s5_
w_w w. k#s5_
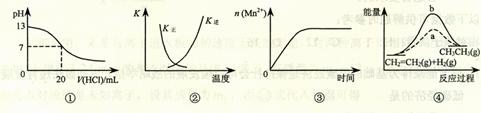
A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g)
+ O2(g)  2SO3(g);ΔH
< 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH
< 0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2
(g) + H2(g)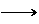 CH3CH3(g);ΔH<
0使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g);ΔH<
0使用和未使用催化剂时,反应过程中的能量变化
解析:酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错;正逆反应的平衡常数互为倒数关系,故B正确;反应是放热反应,且反应生成的Mn2+对该反应有催化作用,故反应速率越来越快,C错;反应是放热反应,但图像描述是吸热反应,故D错。
答案:B
1.(2010年江苏)常温下,用 0.1000 mol·L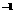 NaOH
NaOH
溶液滴定 20.00mL0.1000 mol·L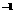 CH3COOH溶液
CH3COOH溶液
所得滴定曲线如右图。下列说法正确的是
A.点①所示溶液中:
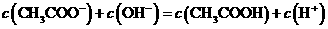 B.点②所示溶液中:
B.点②所示溶液中:
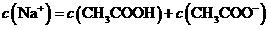
C.点③所示溶液中:
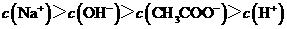
D.滴定过程中可能出现:
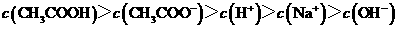
解析:本题主要考查的是酸碱中和过程中粒子浓度的变化及其粒子浓度的大小比较。由装置图可知处于点①时,醋酸过量,根据电荷守恒,则有c(Na+)+ c(H+)=c(OH-)+c(CH3COO-),A错误;CH3COOH和NaOH恰好中和时,溶液应该显弱碱性,而在点②时,pH=7,说明没有完全反应,醋酸过量,依据离子守恒知c(Na+)<(CH3COO H)+c(CH3COO-),B错误;当加入NaOH溶液的体积恰好为20ml时,两者恰好完全反应,此时由于CH3COO-的水解,溶液呈若碱性,但水解程度是微弱的,因此关系式为:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+),C错误;若滴入的NaOH量很少,有可能会出现选项D中的情况,因此D正确。
答案:D
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com