
题目列表(包括答案和解析)
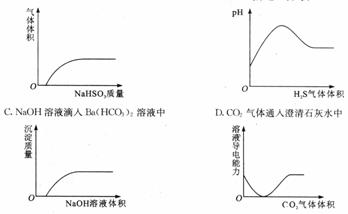
6.下列实验过程中产生的现象与对应的图形相符合的是 ( )
答案:6.D
5.下列实验能证明有SO2存在的是 ( )
①能使澄清石灰水变浑浊;②能使湿润的蓝色石蕊试纸变红;③能使品红溶液褪色;④通入足量的NaOH溶液中,再加BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸;⑤通入溴水中能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成
A.都能证明 B.只有⑤能证明 C.③④⑤能证明 D.都不能证明
 答案:5.B①CO2也能使澄清石灰水变浑浊,②只要酸性气体可使湿润的石蕊变红③Cl2也可使品红溶液褪色⑤通入溴水使溴水褪色说明能与Br2反应,同时生成SO
答案:5.B①CO2也能使澄清石灰水变浑浊,②只要酸性气体可使湿润的石蕊变红③Cl2也可使品红溶液褪色⑤通入溴水使溴水褪色说明能与Br2反应,同时生成SO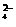 的只有SO2气体
的只有SO2气体
4.下列试剂能用于验证相同物质的量浓度的NaCl、MgCl2、AlCl3溶液的酸、碱性强弱的是 ( )
A.NaOH溶液 B.K2CO3溶液 C.pH试纸 D.氨水
答案:4.C验证相同物质的量浓度的确NaCl,MgCl2,AlC3,溶液中的酸性的强弱就是验证它们c(H+)的大小,只有C可行
3.下列实验的失败是因为缺少必要的实验步骤所造成的是 ( )
A.将无水乙醇和浓H2SO4,共热到140℃收集不到乙烯
B.将氯乙烷(C2H5Cl)与NaOH溶液共煮后加入AgNO3溶液得褐色沉淀
C.将乙醛滴加到新制的Cu(OH)2悬浊液中未出现红色不溶物
D.将Cu和浓HNO3反应,用排水法收集到的气体呈五色
答案:BC A是由于没加热到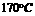 ,B是没有用稀HNO3酸化引起,C是由于没有加热,所以不会产生红色不溶物
,B是没有用稀HNO3酸化引起,C是由于没有加热,所以不会产生红色不溶物
2.氯仿可当麻醉剂,常因保存不慎而被空气氧化产生有剧毒的光气: (光气),为防止事故,使用前要检验氯仿是否变质,所用试剂是 ( )
(光气),为防止事故,使用前要检验氯仿是否变质,所用试剂是 ( )
A.NaOH溶液 B.溴水 C.AgNO3溶液 D.KI淀粉溶液
答案:C氯仿作为麻醉剂变质时产生HCl与COCl2,所以检验是否有HCl产生,可用AgNO3溶液,看是否产生白色沉淀
1.下列实验中用错试剂的是 ( )
A.用稀盐酸清洗做焰色反应的镍铬丝 B.用酒精萃取碘水中的碘
C.用稀HNO3洗去残留在试管壁上的铜 D.用碱石灰吸收氨气中的水蒸气
答案:B1.酒精和水互溶,不可用来萃取碘水中的碘
5.熟悉各种性质的验证途径,以提高学生的发散思维能力,并从中选取最佳途径。例如金属性、非金属性的验证可通过下列途径:

潜能开发
[例1]根据平衡移动原理,设计两种实验方法,以证明氨水是一种弱碱。除氨水外,限在以下范围内选用试剂:蒸馏水、酚酞试液、石蕊试液、NH4Cl晶体、消石灰、浓盐酸、醋酸铵晶体。
思路分析
此题是一道实验设计题。要证明NH3·H2O是弱碱,可采用两种方法:一种是弱碱溶液中一定存在电离平衡,只要说明氨水中存在电离平衡即可证明氨水是弱碱;另一种方法是弱碱阳离子会破坏水的电离平衡,只要证明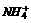 能破坏水的电离平衡即可说明氨水是弱碱。
能破坏水的电离平衡即可说明氨水是弱碱。
[答案](1)取少量氨水,滴加酚酞试液,溶液呈红色,然后向其中加入少量CH3COONH4晶体,振荡,可看到红色变浅,说明氨水中存在电离平衡,说明氨水是弱碱。
(1)
取少量NH4Cl晶体溶于水,滴加石蕊试液,溶液呈红色,说明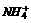 水解,破坏了水的电离平衡,说明氨水是弱碱。
水解,破坏了水的电离平衡,说明氨水是弱碱。
[例2]有一合成纤维尼纶的中间体,其结构为:
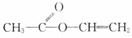
试以实验事实说明它的主要化学性质。
思路分析
从结构式看,该物质是乙酸乙烯(醇)酯,从结构特点分析其主要化学性质有①不饱和性;②能发生水解。基于上述推测,可用溴水证明不饱和性;用NaOH、酚酞验证水解情况,考虑到水解产物乙烯醇易发生重排转化成乙醛,可用新制Cu2(OH)2,与之反应来证明。
[答案](1)取少量乙酸乙烯(醇)酯于试管中,加溴水振荡,观察颜色褪去,证明该有机物具有不饱和性。
(2)取少量乙酸乙烯(醇)酯0.86 g于锥形瓶中,加入20 mL1mol/LNaOH溶液共热,冷却后加2滴酚酞指示剂,用0.5mol/L盐
酸滴定至红色刚好消失时,消耗酸液20mL。

(3)取少量上述滴定后的溶液于试管中,加入少量新制Cu(OH),加热有红色沉淀产生,即证明产物中有乙醛,也就说明了乙酸乙烯酯能发生水解反应。
[例3] 这几种溶液都可以与某些物质反应,生成化合物A。
这几种溶液都可以与某些物质反应,生成化合物A。
(1)写出A的化学式 ;
(2)写出由Na2SO4溶液生成A的化学方程式 .
此题主要考查分解反应中阴阳离子重组知识。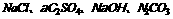 四种物质在组成上的共同点是都含有Na+,既然都能与另外的物质生成化合物A,则A中必含Na+,与上述四种钠的化合物反应的物质也必然含有相同的阴离子(不产生沉淀离子),即A中的阴离子。
四种物质在组成上的共同点是都含有Na+,既然都能与另外的物质生成化合物A,则A中必含Na+,与上述四种钠的化合物反应的物质也必然含有相同的阴离子(不产生沉淀离子),即A中的阴离子。
[答案]
思维诊断
涉及知识点:①弱电解质在水中存在电离平衡 ②弱碱的强酸盐水溶液呈酸性、弱酸的强碱盐水溶液呈碱性,是因为对应的阳离子及酸根离子水解破坏了水的电离平衡。
思维诊断
本题第二步加NaOH溶液、酚酞然后共热,红色消失,即可定性地说明酯的水解性,为了使该酯水解完全并进一步测定产物乙醛,该方案使用了定量的方法,从数据可以看出,酯的水解用去了NaOH0.01mol,0.86 g的酯也是0.01 mol,故说明酯已完全水解。
与上述四种化合物反应的物质中的阳离子分别能与 反应结合成难电离(难溶的)物质,这些阳离子一般是
反应结合成难电离(难溶的)物质,这些阳离子一般是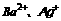 ,而能与
,而能与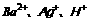 等形成可溶性化合物的只有`
等形成可溶性化合物的只有`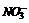 。
。
知能达标训练
4.重视实验基本操作,强化实验技能训练,在进行实验教学时,要重视基本操作中常用仪器(如容量瓶、托盘天平、烧杯、漏斗等)的构造、原理、操作要点及注意事项的剖析,并注意总结物质的分离提纯,气体的制取、干燥、收集和净化等基本操作方法,强化实验动手能力。
3.重视课本知识,将元素及其化合物知识系统化,应用元素周期律来分析元素及其化合物的有关知识,掌握“位一构一性”之间关系。
2.有机物性质实验方案设计常常是利用官能团来推测性质,但是,在有机化合物的分子中,官能团性质又必然地受分子中其他部分的影响,所以在不同的化合物中,官能团的反应活性往往有很大差异。由于分子结构不同或其他官能团的存在,有的活性增大,有的则减小,有的甚至完全失去应有的特性,这样不可能制定出适用于任何有机物中某一官能团的性质实验方案,对于不同的有机化合物,只能从 具体情况出发设计不同方案。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com