
20.(09泉州)(29分)小强同学在化学氧自救器的说明书中看到“人呼出气体中的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气后,对自救器内发生的化学反应原理产生了探究欲望。在老师指导下,小强与同学们展开了以下两个实验探究活动,请你参与。
活动Ⅰ:用下图所示的由a、b、c、d组合成的成套装置和有关药品制取并收集氧气。
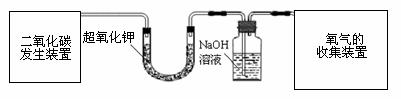
a b c d
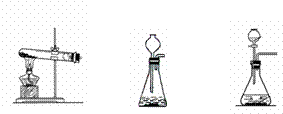 (1)用石灰石与稀盐酸制取二氧化碳,则a装置可采用下图中的 (填序号),有关反应的化学方程式为
。
(1)用石灰石与稀盐酸制取二氧化碳,则a装置可采用下图中的 (填序号),有关反应的化学方程式为
。
① ② ③
(2)用c装置中的氢氧化钠溶液吸收未与超氧化钾反应的二氧化碳。请写出氢氧化钠与二氧化碳反应的化学方程式 。
(3)用 法收集氧气,该收集方法是根据氧气 的性质而确定的。证明生成的气体是氧气,使用 进行检验。
活动Ⅱ:探究二氧化碳与超氧化钾反应除生成氧气还声称什么其它物质?
[老师提示]二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物。
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?小强作出了以下三种猜想:
①是一种酸; ②是一种碱; ③是一种碳酸盐。
通过对反应物有关的元素组成的分析,小影同学认为猜想 、 (填序号)一定是错误的,理由是 。
[进行实验]同学们通过以下实验验证小强同学的另一个猜想。
|
实验步骤 |
实验现象 |
实验结论 |
|
将二氧化碳与超氧化钾反应后的固体
|
|
猜想 (填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是
(填名称)。 |
[交流与讨论](1)小影认为:二氧化碳与超氧化钾反应的化学方程式 。
(2)老师指出:人呼出的气体中含有的水分也能与超氧化钾反应生成氧气。小影简述了鉴定氧自救器药罐中生氧剂超氧化钾是否需要跟换的简便的化学方法:
。
(3)小强简述了化学氧自救器能达到氧自救的化学反应原理 。
23.Ⅰ(1)置换反应 (2)Cl2、Br2、I2或Cl2>Br2>I2
Ⅲ(1)NH4HCO3 (2)在同温度下碳酸氢铵的溶解度小 (3) 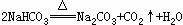
22.(10分)(1) 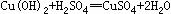 (2)酸+盐 金属+盐
(其他合理答案也可)
(2)酸+盐 金属+盐
(其他合理答案也可)
(3) ①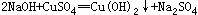
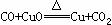 ②步骤Ⅰ和步骤Ⅴ
②步骤Ⅰ和步骤Ⅴ
(09潍坊) 23.(8分)海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还含有大量的化学物质。
I .海水提溴。从海水中提取的溴约占世界溴产量的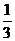 ,工业上常用“吹出法”制溴,其工艺流程如下:
,工业上常用“吹出法”制溴,其工艺流程如下:
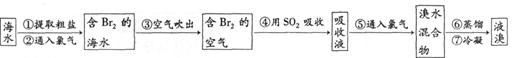
试回答:
(1)步骤②中的化学方程式为2NaBr+C12=2NaCl+Br2,其反应类型是 ,
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:C12+2KBr=2KCl+Br2 Br2+2KI=2KBr2+I2
由此可判断C12、I2、Br2活动性由强到弱顺序是_______。
Ⅱ .食盐制碱。我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向浓氨水中通人足量的二氧化碳生成碳酸氢铵溶液;②然后向溶液中加入食盐细粒充分搅拌,控制条件,利用物质的性质不同,两者发生反应生成碳酸氢钠,便有晶体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水。
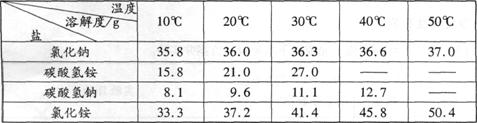
四种盐在不同温度下的溶解度表:
请回答:
(1)碳酸氢铵的化学式是 。
(2)由上表分析过程②中能发生反应的原因是 。
(3)过程③中反应的化学方程式是 。
26.(9分)(1)蒸馏法
(2)蒸发结晶 ①③②⑤⑦④⑥(或①⑤③②⑦④⑥或①③⑤②⑦④⑥)
(3) Mg(OH)2 MgCl2 通电 Mg+Cl2↑ 后者是经过富集和分离后的溶液(或海水中含有氯化钠等多种溶质,氯化镁的浓度很低)
(4) NaCl+NH3+H2O+CO2=NaHCO3+NH4Cl 2NaHCO3△ Na2CO3+ H2O+CO2↑ 氨气溶于水形成碱性溶液,更易于吸收二氧化碳
(09潍坊) 22.(10分)小梅同学学习了单质、氧化物、酸、碱、盐性质后,发现许多不同类别的物质反应时能生产盐,于是她构建了下图所示的知识网络图。
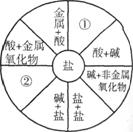 铜及其化合物在工业上有重要的应用。借助网络图回答:
铜及其化合物在工业上有重要的应用。借助网络图回答:
(1)写出用酸和碱生产硫酸铜的化学方程式:
。
(2)请你把图中①②处补充完整,要求不能与图中已有信息重复。
① ;② 。
(3)根据网络图可制备物质。例如,某回收含铜电缆废料的工厂有下列制铜的方案:
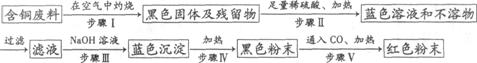
①写出下列步骤中的化学方程式:
步骤Ⅲ: 。
步骤V: 。 。
②上述方案中可能造成空气污染的步骤是 。 .
27.(09南京)(6分)框图中的物质为初中化学所学的物质,其叫属于盐的是B、C、M、N,属于氧化物的是F、G;胃液中含有适量的A,可帮助消化;C是家庭中重要的调味品之-一;D常用于改良酸性土壤。图中“---.”表示两端的物质问能发生化学反应:“→’表示物质间存在转化关系;部分反应物或生成物已略去。
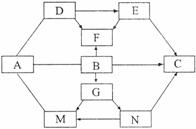 (1)C物质是由
(选填“分子”、“原子”或 “离子”)构成的。
(1)C物质是由
(选填“分子”、“原子”或 “离子”)构成的。
(2)A与镁条反应能 (选填“放出”、“吸收”)
热量。
(3)写出D的俗名: ;
写出化学式:B N
(1)写小G→M的化学方程式:
(09烟台) 26.(9分)海水是一种重要的自然资源。以下是我市对海水资源的部分利用。
(1)从海水中获取淡水。常用的操作方法是 。
(2)从海水中获得氯化钠。将海水进行 可得到粗盐;为除去粗盐中含有
的SO42-、Ca2+、Mg2+等杂质,-有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是 。(用序号填一种合理组合)。
 (3)从海水中得到金属镁。下图是从海水中提取镁的简单流程。
(3)从海水中得到金属镁。下图是从海水中提取镁的简单流程。
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为 ,由无水MgCl2制取Mg的化学方程式为 。海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:
。
(4)海水“制碱”。下图是海水“制碱”的部分简单流程。

步骤Ⅲ、步骤Ⅳ反应的化学方程式为: 、
。
制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为 。
16.(5分)⑴做锅/加工成丝/加工成片 ⑵金属X表面有红色固体生成
⑶
|
你的一种猜想 |
操作 |
现象 |
结论 |
|
金属X的活动性比镁弱 |
取经打磨的金属X固体,放入氯化镁溶液中。 |
无明显现象 |
假设成立,金属X的活动性比镁弱 |
15.(11分)
[提出猜想]所得溶液可能呈碱性,也可能呈 酸 性,还可能呈 中 性。
[实验验证]
|
|
实验现象 |
结论 |
|
|
无色酚酞试液变 红 |
|
|
|
溶液呈 酸性或中性 |
[分析与思考]
⑴OH-;氯化铁/氯化铜(化学式也可),FeCl3+3NaOH = Fe(OH)3↓+3NaCl CuCl2 +2NaOH = Cu(OH)2↓+2NaCl
⑵有所泡产生;Zn+ 2HCl = ZnCl2+ H2↑
(09达州)16.(5分)下表是生活中某种常见金属X的部分性质:
|
颜色状态 |
硬度 |
密度 |
熔点 |
导电性 |
导热性 |
延展性 |
|
银白色固体 |
软 |
7.9g/cm3 |
1525℃ |
良好 |
良好 |
良好 |
将金属X投入盐酸中,有大量气泡生成。根据上述信息,回答下列问题:
⑴试推断金属X可能的一种用途 。
⑵将金属X放入硫酸铜溶液中,观察到的现象是 。
⑶请自选试剂,设计实验比较金属X与Mg的活动性强弱。完成下表:
|
你的一种猜想 |
操作 |
现象 |
结论 |
|
|
|
|
假设成立,金属X的活动性比镁弱 |
15.(09达州)(11分)小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
[探究目的]探究所得溶液的酸碱性
[提出猜想]所得溶液可能呈碱性,也可能呈 性,还可能呈 性。
[实验验证]
|
实验操作 |
实验现象 |
结论 |
|
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 |
无色酚酞试液变
|
溶液呈碱性 |
|
无色酚酞试液不变色 |
溶液呈
|
[分析与思考]
⑴若溶液呈碱性,则溶液中使其呈碱性的离子是 (填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入 溶液,直到不再产生沉淀为止。然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为 。
⑵若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到 ,则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为 ;若无明显现象,则呈中性。
30.(09兰州)(4分)化学就在我们身边,它与我们的生活息息相关。请从A熟石灰、B苏打、C一氧化碳、D氮气、E浓硫酸、F盐酸这六种物质中,选择适当的物质用序号填空。
(1)能与酸发生中和反应的物质是 ; (2)常用于工业除锈的试剂是 ;
(3)有毒的物质是 ; (4)我国著名化学家侯德榜发明的联合制碱法中的“碱”是指 。
28.(09扬州)(16分)菠菜营养丰富,素有“蔬菜之王”的美称。民间流传:菠菜豆腐同食,易得结石。某化学兴趣小组对“菠菜豆腐是否不能同食”等问题进行了探究。
[查阅资料]①菠菜含有丰富的铁、草酸盐、碳酸盐等,豆腐中含有丰富的蛋白质及钙盐。
②人体结石的主要成分:草酸钙(CaC2O4)
③醋酸不与草酸钙反应,但能与碳酸钙反应生成可溶性盐等。
[提出猜想]“菠菜豆腐不能同食”的原因可能是 ▲ 。
 [探究一]菠菜中部分成分分析
[探究一]菠菜中部分成分分析
(1)步骤③中加入足量的CaCl2溶液的目的 ▲ 。
(2)已知气体C能使澄清石灰水变浑浊,醋酸的化学式用HAC表示,写出步骤④的化学反
应方程式 ▲ 。沉淀A、B的质量关系为:m(A) ▲ m(B)(填“>”、“<”
或“=”)。
(3)白色沉淀B的化学式为 ▲ ,由此可见菠菜豆腐不能同食。以下饮食观点正确的是
▲ (填字母)
A.禁吃菠菜 B.高钙牛奶可与菠菜同食
C.菠菜烹饪时可用开水烫,可降低草酸盐含量
[探究二]某草酸钙晶体(CaC2O4·xH2O)热分解研究
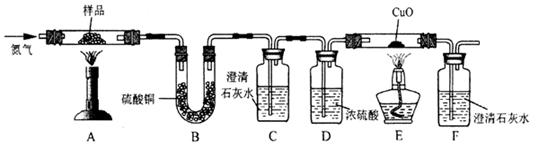 按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)
(4)①反应开始前通入氮气的目的是 ▲ 。
②装置B中硫酸铜粉末变蓝,说明产物中有 ▲ ,C、F中澄清石灰水均变浑浊,E
中CuO变红,说明产物还有 ▲ 和 ▲ ,经检验A中残留固体为氧化物。
③对上述装置从环保角度提一个改进建议 ▲ 。
(5)某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,获得
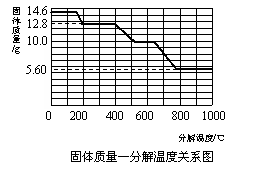 相关数据,绘制成固体质量-分解温度的关系如右图。
相关数据,绘制成固体质量-分解温度的关系如右图。
①800℃以上时,固体成分的化学式为 ▲ 。
②计算CaC2O4·xH2O中的x(写出计算过程,
CaC2O4的相对分子质量:128)。
③残留固体为CaC2O4时的温度范围 ▲ ,
写出固体质量由12.8g变为10.0g时的化学
方程式 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com