
4.实战演练
3. 例题精讲
例1 下列关于钠的说法不正确的是[ ]
A、金属钠和氧气反应,条件不同,产物不同
B、钠钾合金通常状况下呈液态,可作原子反应堆的导热剂
C、钠的化学活泼性很强,少量的钠可保存在有机溶剂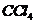 中
中
D、由于钠比较活泼,所以它能从溶液中置换出金属活动顺序表中钠后面的金属
解析 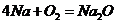 ,
,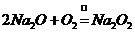 ,A正确;B的说法是正确的,这是钠的重要用途之一;钠的保存原则是将钠与空气和水隔绝,故应保存在密度小于钠的有机溶剂中,
,A正确;B的说法是正确的,这是钠的重要用途之一;钠的保存原则是将钠与空气和水隔绝,故应保存在密度小于钠的有机溶剂中,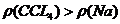 ,故C不正确;盐溶液中的金属阳离子周围有一定数目的水分子包围着,不能和钠直接接触,另外,钠跟水反应速率很快,故不能从盐溶液中置换出金属。
,故C不正确;盐溶液中的金属阳离子周围有一定数目的水分子包围着,不能和钠直接接触,另外,钠跟水反应速率很快,故不能从盐溶液中置换出金属。
答案 C、D
例2 将少量金属钠分别投入下列物质的水溶液中,有气体放出,且溶液质量减轻的是[ ]
A、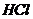 B、
B、 C、
C、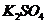 D、
D、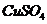
解析 少量钠投入上述四种物质的水溶液中,均有 产生,故都满足题目的第一个条件“有气体放出”,而反应后“溶液质量减轻”是指投入的金属钠的质量小于脱离溶液的物质的质量。在A、B、C三个选项中一只有
产生,故都满足题目的第一个条件“有气体放出”,而反应后“溶液质量减轻”是指投入的金属钠的质量小于脱离溶液的物质的质量。在A、B、C三个选项中一只有 放出,故溶液质量是增加的。D选项中由于
放出,故溶液质量是增加的。D选项中由于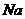 与
与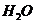 反应生成的NaOH还能继续与
反应生成的NaOH还能继续与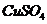 反应析出
反应析出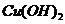 沉淀:
沉淀: ,反应后溶液质量减轻。
,反应后溶液质量减轻。
答案 D
例3 用金属钠制取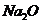 通常采用下法:
通常采用下法: ,试说明不采用钠在氧气中燃烧而用此法制取
,试说明不采用钠在氧气中燃烧而用此法制取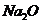 的原因:
的原因:
解析 钠在氧气中燃烧将生成 ,而题示反应有
,而题示反应有 生成,在氮气流中
生成,在氮气流中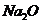 就不会被进一步氧化成
就不会被进一步氧化成 。
。
答案 钠在氧气中燃烧将得到 ,利用题给方法制得氧化钠同时生成
,利用题给方法制得氧化钠同时生成 ,
, 作为保护气,防止
作为保护气,防止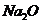 进一步被氧化为
进一步被氧化为 。
。
例4 将4.6 g钠与1.6g硫粉迅速混合起来,并放在石棉网上加热,反应后生成的固体是[ ]
A、黄色固体混合物 B、硫与硫化钠
C、过氧化钠与硫化钠 D、氧化钠与硫化钠
解析 在加热条件下,钠既能与硫化合生成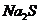 ,也能与空气中的氧气反应生成
,也能与空气中的氧气反应生成 ,而钠又是过量的,所以除生成
,而钠又是过量的,所以除生成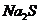 外还有
外还有 生成。
生成。
答案 A、C
例5 A、B、C、D、E五种物质都含有同一元素,它们按下图所示关系相互转化,已知A为单质。
(1)写出A-E的化学式
(2)分别写出有关反应的化学方程式,其中属于氧化还原反应的,请标出电子转移的方向和数目
①A→B:________ ②A→C:________ ③A→D:________
④C→D:________ ⑤C→E:________ ⑥D→E:________
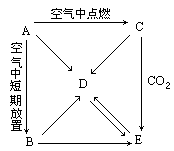
解析 本题属于根据图示转化关系进行物质判断的测试题,该题以第一步转化“A→B”、“A→C”为突破口,即单质与氧气的反应因条件不同(点燃与常温)而产物不同,根据目前所学,很容易想到金属钠,由此推出B为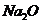 ,C为
,C为 。然后顺其性质往下推,由框图可知A、B、C 3种物质均可转化为D,不难判断D为
。然后顺其性质往下推,由框图可知A、B、C 3种物质均可转化为D,不难判断D为 。最后根据B、C、D在一定条件下都能转化为E,推出E为
。最后根据B、C、D在一定条件下都能转化为E,推出E为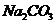 。
。
答案 (1) 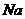 、
、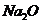 、
、 、
、 、
、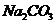
(2)① ,
②
,
②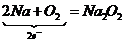 ,
,
③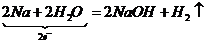 , ④
, ④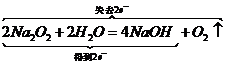 ,
,
⑤ ,
,
⑥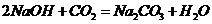 (非氧化还原反应)。
(非氧化还原反应)。
例6 2.1g 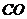 和
和 组成混合气体与足量的
组成混合气体与足量的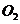 充分反应后,立即通入足量的
充分反应后,立即通入足量的 固体中,固体质量增加[ ]
固体中,固体质量增加[ ]
A、2.1g B、3.6 g C、7.2 g D、不可确定
解析 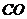 和
和 与
与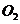 燃烧的化学方程式为:
燃烧的化学方程式为: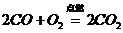 ,
,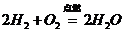 ;
;
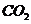 、
、 跟
跟 的反应分别为:
的反应分别为: ,
,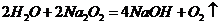 。
。
从4个化学方程式可以看出:增加的质量恰好为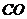 和
和 混合气体的质量,即
混合气体的质量,即 。
。
答案 A
例7 根据图示回答,经数小时后,U形管A、B两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响) [ ]
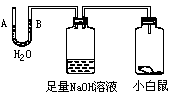
A、A处上升,B处下降 B、A、B两处都下降
C、A处下降,B处上升 D、A、B两处都不变
解析 小白鼠吸收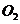 ,呼出
,呼出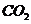 ,呼出的
,呼出的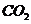 被
被 溶液吸收,导致内压减小,故A处下降、B处上升。
溶液吸收,导致内压减小,故A处下降、B处上升。
答案 C
例8 苏打和小苏打有着广泛应用,试从反应物用量角度说明,在下列用途中选(A)苏打,还是(B)小苏打,并说明原因。
(1)做面条时防止面粉较长时间储存变酸味,常加入适量的碱面,选用________,因为________。
(2)作为泡沫灭火器的药品,选用________,因为________。
(3)用于洗涤餐具及实验室的玻璃仪器等,选用________,因为________(提示:二者水溶液均显碱性,且苏打的碱性强)。
(4)治疗胃酸过多时,选用________,因为________。
解析 本题紧扣本节重点,纯碱和小苏打性质联系用途,由课本演示实验可知: ,
,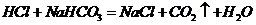 ,等量酸耗苏打的质量相对小;产生等量
,等量酸耗苏打的质量相对小;产生等量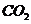 时耗小苏打少;而做洗涤剂和中和胃酸均利用其碱性,前者当然碱性强,洗涤效果好,但碱性太强不利于健康。
时耗小苏打少;而做洗涤剂和中和胃酸均利用其碱性,前者当然碱性强,洗涤效果好,但碱性太强不利于健康。
答案 (1)A,因为中和等量的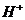 ,
,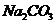 比
比 的用量少(质量比为53∶84)。
的用量少(质量比为53∶84)。
(2)B,因为产生等量的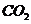 时,
时, 比
比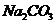 的用量少(质量比为84∶106),且产生
的用量少(质量比为84∶106),且产生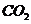 的速率大。
的速率大。
(3)A,因为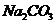 碱性强,洗涤效果好。
碱性强,洗涤效果好。
(4)B,因为适量中和部分胃酸,若用苏打碱性太强,有腐蚀性,不利于人的健康。
例9 某干燥粉末可能由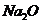 、
、 、
、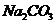 、
、 、
、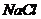 中的一种或几种组成。将该粉末与足量的盐酸反应,有气体X逸出,X通过足量的
中的一种或几种组成。将该粉末与足量的盐酸反应,有气体X逸出,X通过足量的 溶液后体积缩小(同温、同压下测定)。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量,下列判断正确的是[ ]
溶液后体积缩小(同温、同压下测定)。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体的质量大于原混合粉末的质量,下列判断正确的是[ ]
A、粉末中一定有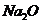 ,
, ,
,
B、粉末中一定不含有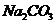 和
和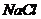
C、粉末中一定不含有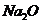 和
和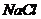
D、无法肯定粉末里是否含有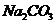 和
和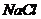
解析 与盐酸反应产生气体的物质可能有 、
、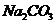 和
和 ,气体X通过足量的
,气体X通过足量的 溶液后体积缩小(而不是气体全部消失),说明X由
溶液后体积缩小(而不是气体全部消失),说明X由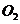 和
和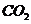 组成,原粉末中
组成,原粉末中 、
、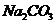 和
和 至少有一种一定存在。将原混合粉末加热,有气体放出,说明混合物中一定有
至少有一种一定存在。将原混合粉末加热,有气体放出,说明混合物中一定有 ,但
,但 受热分解会使混合物粉末质量减少,而实际剩余固体的质量都增加了,原因只能是发生了反应:
受热分解会使混合物粉末质量减少,而实际剩余固体的质量都增加了,原因只能是发生了反应: 。综上分析,混合物中有
。综上分析,混合物中有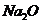 、
、 、
、 ,无法确定混合物中是否有
,无法确定混合物中是否有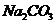 和
和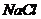 。
。
答案 A、D
5.焰色反应操作的注意事项有哪些?
答案:(1)所用火焰本身的颜色要浅,以免干扰观察.
(2)蘸取待测物的金属丝本身在火焰上灼烧时应无颜色,同时熔点要高,不易被氧化.用铂丝效果最好,也可用铁丝、镍丝、钨丝等来代替铂丝.但不能用铜丝,因为它在灼烧时有绿色火焰产生.
(3)金属丝在使用前要用稀盐酸将其表面的氧化物洗净,然后在火焰上灼烧至无色,以除去能起焰色反应的少量杂质.
(4)观察钾的焰色时,要透过蓝色的钴玻璃片,因为钾中常混有钠的化合物杂质,蓝色钴玻璃可以滤去黄色火焰,以看清钾的紫色火焰.
4.实验室中做固体受热生成气体反应的实验注意事项有哪些?
答案:实验室固体受热生成气体的装置都可用制O2装置.注意事项:①试管应夹持在其中上部(或离管口1/3处);②试管口应略向下倾斜,因为实验室中的药品不是很干燥,加热时有水生成,或固体反应时生成水,若不略向下倾斜会使水倒流把试管炸裂;③受热时先均匀加热试管底部,然后固定在药品集中的部位加热.
3.用稀盐酸与Na2CO3还是NaHCO3制作的灭火器灭火效果好,有哪些优点?
答案:用稀盐酸与NaHCO3制作的灭火器灭火效果好.优点有二:①产生气体速度快,②产生气体CO2多.
2.万一被钠灼伤了皮肤,应该怎么办?
答案:万一被钠灼伤了皮肤,应先用稀醋酸洗涤,然后再涂上3%-5%的硼酸溶液.情况严重者速到医院烧伤科救治.
1.若钠、钾等碱金属在空气中失火,可否用水或CO2灭火,为什么?用什么灭火效果好?
答案:钠、钾等碱金属失火不能用水灭火,因为它们与水反应剧烈,且产生易燃气体H2,易导致爆炸发生;也不能用CO2灭火,因为Na、K有还原性,能夺去CO2中的氧继续燃烧.
钠、钾失火可用沙土、抹布扑灭或盖灭.
(1)实验步骤
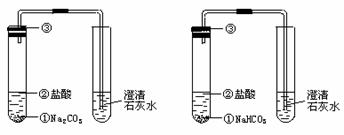
图2-10
(2)反应原理
Na2CO3+2HCl=2NaCl+H2O+CO2↑或CO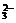 +2H+=H2O+CO2↑
+2H+=H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑或HCO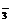 +H+H2O+CO2↑
+H+H2O+CO2↑
(3)注意事项:使用的盐酸浓度不能太大,否则生成的气泡太多太迅速而溢出试管.
(4)实验现象和结论
两者都与盐酸反应生成使澄清石灰水变浑浊的气体,但NaHCO3与盐酸反应更剧烈.
(1)实验过程
①用一干燥大试管,装入NaHCO3粉末.(大约占试管容积1/6)
②将大试管用带导气管的单孔塞塞紧.并将大试管固定在铁架台上,且试管口稍向下倾斜.
③大试管上的导气管另一端插入到盛有澄清石灰水的试管中.
④用酒精灯加热,先均匀受热,然后固定在药品多的部位加热.
⑤当试管中产生气体减少时,先把导管从澄清石灰水中拿出来,再熄灭酒精灯
(2)反应原理
2NaHCO3 Na2CO3+H2O↑+CO2↑
Na2CO3+H2O↑+CO2↑
(3)注意事项
①装药品时,应将药品倾斜地铺在试管底部,以便于受热.
②固定大试管时,应夹在其中上部(离管口1/3处)且要使试管口略向下倾斜.防止反应生成的水冷却回流而将试管炸裂.
③当试管中产生气体减少时,若停止实验,应先将导气管从石灰水中取出来,再撤去酒精灯停止加热,否则,会使石灰水倒吸而引起试管炸裂.
(4)实验现象
澄清石灰水变浑浊,大试管内壁有水生成.
(5)实验结论
NaHCO3受热易发生分解反应.
4.钠和氧气的反应
(1)实验过程:①②③④⑤⑥⑦

钠与氧气的反应
图2-9
(2)反应原理:2Na+O2 Na2O2,2Na2O2+2H2O=4NaOH+O2↑
Na2O2,2Na2O2+2H2O=4NaOH+O2↑
(3)注意事项
①玻璃管中装的钠不能太大,太大反应太剧烈,会将玻璃管炸裂.
②反应开始时,即钠熔成小球后要稍稍倾斜玻璃管,但是角度不能太大,以防止钠从玻璃管中脱出.并能保证空气疏通从而观察到明显现象.
③在取钠时要将其表面的氧化物用小刀除去,用纯钠进行实验.因为表面被氧化的钠在受热熔化后,钠表面会有一层黑色而影响实验现象的观察.
④加热时间不能太长,否则钠与O2迅速反应、燃烧起来,现象就不是很明显了.
⑤盛Na2O2的小试管要干燥.
(4)实验现象
钠熔成小球,先变成白色后变成淡黄色固体,淡黄色固体遇水放出使带火星木条复燃的气体.
(5)实验结论
钠熔点低,与O2加热反应生成Na2O2,Na2O2遇水生成O2.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com