
【题目】实验员小周在学期末整理实验仪器时发现有一瓶标签模糊的溶液,如下图。

请你和小周一起探究该溶液的成分,并测定其质量分数。
第一步:猜想并验证该溶液的溶质是什么。
猜想:根据标签可知,这瓶溶液可能是HCl、KCl、NaCl等含有氯离子的酸或盐。
验证:
步骤 | 现象 | 结论 |
取样,滴加紫色石蕊 | 溶液变成_______色 | 这瓶溶液是盐酸 |
第二步:测定该溶液的溶质质量分数
实验原理:⑴用已知浓度的氢氧化钠溶液和盐酸反应,反应的化学方程式为:______________
⑵当盐酸和氢氧化钠恰好完全反应时,再增加一滴氢氧化钠溶液,溶液就呈碱性(可以使无色酚酞变成红色),而一滴氢氧化钠溶液的体积约为0.05ml,对测定结果的影响很小可忽略不计。
实验步骤:⑴取未知浓度的盐酸20g倒入烧杯中,向其中滴加2滴无色酚酞溶液。此时溶液呈_____色。
(2)量取质量分数1%的氢氧化钠溶液50ml(密度近似为1.0g/ml),用胶头滴管逐滴滴加该氢氧化钠溶液到盐酸中,观察到_______________,停止滴加,剩余氢氧化钠溶液的10ml。
实验反思:小周在做实验的时盛放待测盐酸的烧杯(实验步骤中加点的烧杯)在装入盐酸前内壁附着较多水,用该烧杯完成上述实验会导致结果_______(填“偏大”“偏小”或“无影响”)。
数据处理:计算该盐酸溶液的溶质质量分数_______________。
【答案】 红 NaOH+HCl=NaCl+H2O 无 刚刚变成红色 无影响 1.825%
【解析】盐酸呈酸性,能使紫色的石蕊试液变成红色,氯化钠和氯化钾呈中性,不能使紫色石蕊变色。由结论“这瓶溶液是盐酸”,故现象是紫色的石蕊试液变红。(1)氢氧化钠和盐酸发生中和反应,生成氯化钠和水,反应的化学方程式表示为:NaOH+HCl=NaCl+H2O;实验步骤:⑴盐酸呈酸性,不能使无色酚酞变色,故取未知浓度的盐酸20g倒入烧杯中,向其中滴加2滴无色酚酞溶液,溶液仍是无色的;(2)由“当盐酸和氢氧化钠恰好完全反应时,再增加一滴氢氧化钠溶液,溶液就呈碱性(可以使无色酚酞变成红色),而一滴氢氧化钠溶液的体积约为0.05ml,对测定结果的影响很小可忽略不计”可知,向盐酸中滴加氢氧化钠溶液至恰好变成红色时,表示盐酸与氢氧化钠恰好完全反应,停止滴加氢氧化钠溶液。实验反思:烧杯内壁附着水,溶液的质量会变大,但盐酸中溶质的质量不变,与氢氧化钠溶液发生反应的盐酸中的溶质,故对实验结果没有影响;反应中消耗的氢氧化钠溶液的质量=(50ml-10ml)![]() 1.0g/ml=40g;40g氢氧化钠溶液中溶质的质量=40g
1.0g/ml=40g;40g氢氧化钠溶液中溶质的质量=40g![]() 1%=0.4g
1%=0.4g
设盐酸溶液中溶质的质量为x;
NaOH + HCl = NaCl + H2O
40 36.5
0.4g x
![]()
X= 0.365g
该盐酸溶液的溶质质量分数=![]() 1.825%
1.825%


科目:初中化学 来源: 题型:
【题目】鸡蛋主要由蛋壳、蛋壳膜、蛋白、蛋黄等几个部分组成,其中蛋壳的主要成分是CaCO3,里面覆盖一层蛋壳膜。我校兴趣小组的同学为此开展了以下探究活动:
【提出问题1】
(1)鸡蛋白中含有的营养成分是_________________。
【查阅资料】
a.蛋壳是经过自然形成。科学手段检测蛋壳中含CaCO3约82%—85%,蛋白质15%—17%,并含多种微量元素;
b.蛋壳膜中蛋白质约占90%—93%。
【提出问题2】
蛋壳中的CaCO3含量是多少呢?小华拟将该蛋壳放在空气中充分灼烧完成测定;小明拟通过蛋壳与稀盐酸反应完成测定。请你参与他们的探究。
【设计方案】他们分别称取12.0 g蛋壳设计了以下不同的实验方案:
(2)小华的方案:
称取12.0 g蛋壳研磨成粉末置于通风橱中,灼烧至质量不再减少,再称量剩余固体的质量为7.16g。则:产生的CO2质量__________g,蛋壳中的CaCO3的质量分数为________%(结果保留到小数点后一位)。
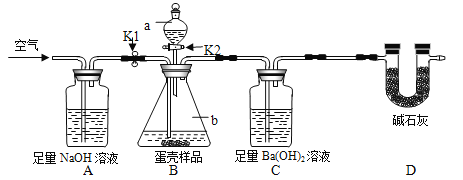
(3)小明的方案:小明设计了如下图所示的实验装置。(已知其他成分均不与稀盐酸反应,装置内试剂均足量)
【实验步骤】
① 出编号仪器的名称:a___________,b__________;
② 按上图连接好装置后,并________________;
③ 向B装置中加入蛋壳样品后,先通入空气一会儿;
④ __________K1,_________K2(填“打开”或“关闭”),向蛋壳样品中滴入10%的盐酸,直到B中___________________为止(填实验现象);
⑤ 再通入一会儿空气,目的是___________________;
⑥ 将装置C中的固液混合物过滤、洗涤、干燥后称量其质量;
⑦ 重复上述实验。
【实验数据】重复实验,3次数据记录如下:
实验次数 | 实验1 | 实验2 | 实验3 |
装置C中沉淀质量(g) | 19.68 | 19.75 | 19.67 |
【实验分析及数据处理】
① 上述数据能否用托盘天平称量_______________。(填“能”或“不能”)
② 若无A装置,直接通入空气,则测定结果将___________。(填“偏大”、“偏小”或“不变”)
③ 实验重复3次的目的是____________________。
④ 请利用3次实验数据的平均值,计算该蛋壳中的CaCO3含量____________(已知:BaCO3相对分子量为197,结果保留到小数点后一位)。(请写出具体的计算过程,该空2分)
【实验反思】
(1)下列各项措施中,能提高小明测定准确度的是____________________(填字母序号)。
A.在装置A、B之间增加盛有浓硫酸的洗气瓶
B.缓缓滴加稀盐酸
C.在装置B、C之间增加盛有饱和NaHCO3的洗气瓶
(2)大家讨论后,一致认为小明的方案更合理,你认为小华方案存在较大误差的原因主要是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上,通过如下转化可制得KClO3晶体。

(1)KClO3中氯元素的化合价为_______。
(2)生产中所用NaCl溶液由粗盐水精制而成,精制时除去粗盐水中泥沙,采用的操作是_______。
(3)完善Ⅰ中反应的化学方程式:NaCl+3H2O=NaClO3 +3_______
(4)已知NaClO3+KCl=NaCl+KClO3,Ⅱ中析出晶体后的滤液是KClO3的_______(填“饱和溶液”或“不饱和溶液”)。
(5)上述流程中,可循环利用的物质是_______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关溶液的说法中正确的是
A. 不饱和溶液转化为饱和溶液,溶液中溶质的质量分数一定增大
B. 将一定质量某物质的饱和溶液降温析出晶体后,所得溶液中溶质的质量分数一定减小
C. 将5 g某物质完全溶解于95 g水中,所得溶液中溶质的质量分数不一定是5%
D. 饱和溶液不一定是浓溶液,不饱和溶液一定是稀溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线。现有t2℃时甲、 乙、丙三种物质的饱和溶液(无固体存在)。 下列说法正确的是

A.三种物质溶解度大小依次为:乙>丙>甲
B.将温度由t2℃降到t1℃时,析出甲的质量比乙多
C.若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯
D.将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙=甲
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】春天的公园,百花盛开,阵阵花香,沁人心脾。花香四溢的现象说明
A.分子是不断运动的 B.分子是由原子构成的
C.分子具有一定的质量 D.分子之间有一定的间隙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】菠菜中含有草酸。将草酸隔绝空气加热,使其完全分解,生成水和碳的氧化物。为了探究上述反应生成的碳的氧化物成分,某同学设计了如下图所示实验。

注:NaOH溶液能与CO2反应
①乙装置对实验结果不产生影响,因此可以去掉乙装置以简化实验方案
②丙装置玻璃管中若发生化学反应,则一定为置换反应
③若甲试管内溶液变浑浊,丁试管内无明显现象,则该碳的氧化物成分为二氧化碳
④若甲试管和丁试管内溶液都变浑浊,丙处玻璃管内的黑色固体变成红色,则该碳的氧化物成分为一氧化碳和二氧化碳
上述正确的说法个数有( )
A. 一个 B. 二个 C. 三个 D. 四个
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像分别与选项中的操作相对应,其中可能合理的是

A.向一定量的稀盐酸和CaCl2混合溶液中滴入Na2CO3 溶液
B.向一定量的MnO2固体中加入一定量的过氧化氢溶液
C.向一定量的稀盐酸中滴入NaOH溶液
D.一定温度时,t ℃时,向一定量的饱和石灰水中加入生石灰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质,加水混合搅拌,待充分反应后过滤,滤纸上留下两种金属的
A. CuSO4(过量)、Al、Na2SO4 B. Fe(过量)、Cu(NO3)2、AgNO3
C. Zn(过量)、KNO3、AgNO3 D. Cu(过量)、FeSO4、H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com