
| ��Ӧǰ | ��Ӧ�� | |
| װ��E������/g | 100.0 | 102.25 |
| װ��F������/g | 50.0 | 51.1 |
���� ��ʵ�鲽�衿
����������μӻ������ʵ�飬ʵ��ǰһ��Ҫ���װ�õ������ԣ��Է�װ��©��Ӱ��ʵ������
Ҫ��Ϥ�������������ơ���;��ʹ�÷�����
Ũ�����ܹ�����ˮ������
��ʯ���ܹ����ն�����̼��ˮ������
���ݾ����������Խ�����ط�����жϣ�
���ݷ�Ӧ��������Ӧ�������������غ㶨�ɿ�����д��Ӧ�Ļ�ѧ����ʽ��
���ݷ�Ӧ�Ļ�ѧ����ʽ���ṩ�����ݿ��Խ�����ط���ļ��㣮
��� �⣺��ʵ�鲽�衿
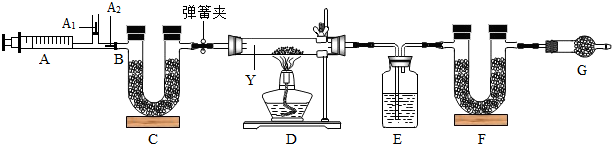
�����Ӻ�װ�ã��ȼ��װ�õ������ԣ��ڷ�������ע�������۳���E��F���������ܹرյ��ɼУ�����D���Թ�ֱ����Ӧ���ٽ��У��ݴ��ɼУ��ٴη�����������ע���������ٴγ���E��F��������
������װ�õ������ԣ�
����̽����
��1������Y��������Ӳ�ʲ����ܣ�
���Ӳ�ʲ����ܣ�
��2��ʵ�鲽������Ӻ�װ�ã��ȼ��װ�õ������ԣ�
������װ�õ������ԣ�
��3��E�е�ҩƷΪŨ���ᣬĿ��������ˮ������F���������������ɵĶ�����̼��G�������Ƿ�ֹ�����еĶ�����̼��ˮ������F���գ�
���Ũ�������ˮ�������������ɵĶ�����̼����ֹ�����еĶ�����̼��ˮ������F���գ�
��4��ʵ�鲽�����۲��ܵߵ�������ߵ���װ���е�ˮ�����Ͷ�����̼�ᱻ���գ�����ʵ������ȷ��
����װ��C��������Ŀ����е�ˮ�����Ͷ�����̼�ᱻŨ���ᡢ��ʯ�����գ���������õ�̼��������������ƫ��
�������в���ݵIJ�������Ӧ���ɵ�ˮ�����Ͷ�����̼���ܱ���ȫ���գ���������õ�̼��������������ƫС��
�ò�������ע����ʱ������Ŀ����ʹ������װ���еĶ�����̼��ˮ������ֱ����գ�
������ܣ�ƫ��ƫС��ʹ������װ���еĶ�����̼��ˮ������ֱ����գ�
��5��װ��D�з����Ļ�ѧ��Ӧ��ѧ����ʽΪ��aNa2CO3•bNaHCO3•cH2O$\frac{\underline{\;\;��\;\;}}{\;}$$\frac{2a+b}{2}$Na2CO3+$\frac{b+2c}{2}$H2O+$\frac{b}{2}$CO2����
���aNa2CO3•bNaHCO3•cH2O$\frac{\underline{\;\;��\;\;}}{\;}$$\frac{2a+b}{2}$Na2CO3+$\frac{b+2c}{2}$H2O+$\frac{b}{2}$CO2����
��6���⣺���ɵ�ˮ��������102.25g-100.0g=2.25g��
���ɵĶ�����̼������51.1g-50.0g=1.1g��
��NaHCO3����Ϊx����ֽ������ˮ������Ϊy��
2NaHCO3�TNa2CO3+H2O+CO2����
168 18 44
x y 1.1g
$\frac{168}{x}$=$\frac{18}{y}$=$\frac{44}{1.1g}$��
x=4.2g��y=0.45g��
m���ᾧˮ��=2.25g-0.45g=1.8g��
m��Na2CO3��=16.6g-4.2g-1.8g=10.6g��
a��b��c�T$\frac{10.6g}{106}$��$\frac{4.2g}{84}$��$\frac{1.8g}{18}$=2��1��2��
���2��1��2��
���� �������ʵ�飬��ѧ�ؽ���ʵ�顢����ʵ�飬�ǵó���ȷʵ����۵�ǰ�ᣬ���Ҫѧ�����ʵ�顢����ʵ�顢����ʵ�飬Ϊѧ�û�ѧ֪ʶ�춨������


 �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ũ���� | B�� | Ũ���� | C�� | �Ȼ��ƹ��� | D�� | �������ƹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 50g | B�� | 100g | C�� | 150g | D�� | 200g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
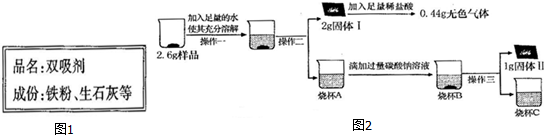
| ʵ����� | ʵ������ | ʵ����� |
| ��1��ȡ������Ʒ�����Թ��У��μ�һ������ϡ���ᣮ�ô���I�ĵ�����Ƥ�������Թܿڣ������� һ���������ʯ��ˮ�У� | �Թ��й�����u���٣��д�����ɫ����������õ�dz��ɫ��Һ������ʯ��ˮ����ǣ� | ��Ʒ��һ������Fe��CaCO3�� ����Fe2O3�� |
| ��2��ȡ������Ʒ�����Թ��У���ˮ �ܽ⣬���ú�ȡ�ϲ���Һ�μ��� ɫ��̪��Һ�� | �Թܵײ��в�����ϲ���Һ����ɫ��Ϊ��ɫ�� | ��Ʒ�к��������ƻ��������ƣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ɱ�����ˮ | B�� | ���ס�����ͭ��ʯ�� | ||
| C�� | ˮ����ʯ��ˮ����Ȼ�� | D�� | ���ʯ��������ء����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ⶨ������O2��������ȼ���������뼯��ƿ������ƿ�������²ⶨ���ƫ�� | |
| B�� | ��ȡ����ʱװ�õ������Բ��ã��ռ������岻���� | |
| C�� | ȡ��ϡ���ȡ��һ������Һ����Һ��Ũ��ƫ�� | |
| D�� | ����ƽ��������ҩƷʱ����ҩƷ������ŷ��ˣ����������һ��������� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com