
科目: 来源: 题型:
【题目】掌握仪器的使用并严格按照操作要求进行实验,才能保障化学实验的成功和安全,根据所学化学知识,回答下列问题
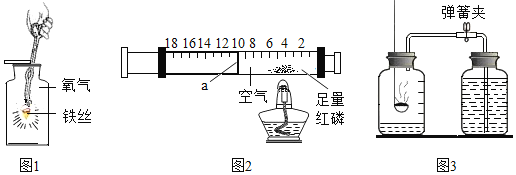
(1)如图1所示进行铁在氧气中燃烧的实验,结果集气瓶炸裂,原因是____________
(2)某同学做“给液体加热”实验时,试管炸裂了,其原因可能是____________(答一点即可)
(3)某学生如图2所示进行“测定空气中氧气含量的实验”
①选择图2代替课本实验图3的优点是____________(答一点即可)
②红磷燃烧后冷却至室温,活塞a应停在刻度____________(填数字)处,若该实验没有达到预期目的,可能的原因之一是________________________________________________
③该实验中的红磷____________(填“能”或“不能”)用硫来代替
查看答案和解析>>
科目: 来源: 题型:
【题目】氨催化氧化是工业制硝酸的反应之一,该反应前后分子种类的微观示意图如图。下列说法不正确的是( )
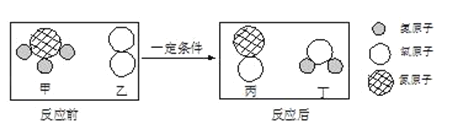
A. 甲中氮、氢原子个数比为1:3
B. 乙的相对分子质量为32
C. 两种生成物均为化合物
D. 生成的丙与丁的分子个数比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】A~G是初中常见的7种物质,它们有如图所示的转化关系.
已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰.
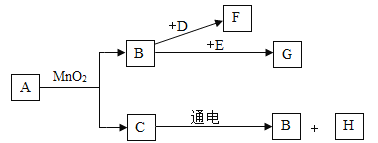
(1)请写出下列物质的化学符号:D_______________,G_______________,H___________________.
(2)请写出下列变化的化学方程式:①B→F_______________,②C→B___________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是王辉同学未完成的实验分析报告,请你帮助完成。
(一)探究影响化学反应快慢的一些因素的相关数据
实验序号 | 过氧化氢溶液浓度 | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ | 反应所需时间/s |
① | 5% | 12 | 20 | 0.4 | 125 | 3 |
② | 5% | 12 | 20 | 0.2 | 125 | 11 |
③ | 30% | 12 | 20 | 0.2 | 125 | 2 |
④ | 30% | 12 | 30 | 0 | 125 | 148 |
⑤ | 30% | 12 | 50 | 0 | 125 | 120 |
(1)通过实验①和②对比可知,化学反应快慢与________________有关;
(2)通过实验②和③对比可知,化学反应快慢与________________有关;
(3)通过实验④和⑤对比可知,化学反应快慢与温度的关系是________。
(4)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是___________。
(二)继续检验催化剂二氧化锰的有关问题:
(1)实验②结束后,重新提纯残余固体,称量其质量是![]() ,其目的是验证______。
,其目的是验证______。
(2)向提纯的固体中重新加入过氧化氢溶液,看到有大量气泡冒出,其目的是验证_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】结合下列实验装置图回答问题:
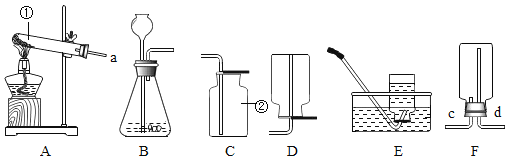
(1)若用高锰酸钾制取氧气,A装置还缺__________;该反应的化学方程式为:___________,基本反应类型为______________。
(2)若用B装置来制取氧气,实验时,先在锥形瓶中添加二氧化锰,再从长颈漏斗添加过氧化氢溶液;该反应的化学方程式为________;装置B中长颈漏斗要伸入液面下,原因是_________。
(3)实验室常用加,固体硫酸铵和固体熟石灰的混合物来制取氨气,制取氨气的发生装置应选用________装置。若使用装置E收集氨气,结合阅读18题的材料,气体应从___________(填“c”或“d”)通入。
(4)用装置E收集一瓶干燥的氧气,验证氧气已收集满的实验操作是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A-G为初中化学常见的物质,其中B为单质,其余均为氧化物。F为黑色固体,G是有刺激性气味的气体。A与D、E与C分别含相同元素,它们之间的相互转化关系如下图所示(反应条件已略去),通过光合作用可实现转化①。
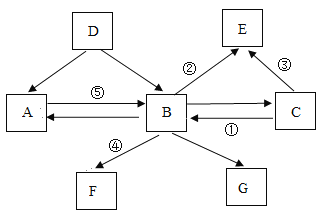
推断后请回答下列问题:
(1)写出化学式G_____________.
(2)写出实现下列转化的化学方程式:
②_______。③_______。④__________。⑤_________。
(3)C与E化学性质不同的原因是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普短文。
氨气(![]() )常用来制化肥和硝酸,科学家们发现它还是一种很有前景的燃料。
)常用来制化肥和硝酸,科学家们发现它还是一种很有前景的燃料。
现有的化石燃料燃烧时,都会产生温室气体![]() ,而氨气燃烧时生成
,而氨气燃烧时生成![]() 和
和![]() 两种对环境友好的产物。氨气价格低、制造技术成熟,便于普及使用。传统的工业合成氨气是将氮气和氢气在高压、高温和催化剂条件下合成的。
两种对环境友好的产物。氨气价格低、制造技术成熟,便于普及使用。传统的工业合成氨气是将氮气和氢气在高压、高温和催化剂条件下合成的。
氨气很容易液化,将氨气常温下加压到![]() ,或者常压下温度降到
,或者常压下温度降到![]() ,均可将其液化。而为了获得含有相同能量的液态氢(
,均可将其液化。而为了获得含有相同能量的液态氢(![]() ),常温下需要
),常温下需要![]() 的压力来压缩它,显然超出了车载燃料储存的压力极限。
的压力来压缩它,显然超出了车载燃料储存的压力极限。
氨气虽然有毒,但氨气具有强烈的刺激性气味,一旦发生泄漏,达到人们觉察到时浓度的1000倍才会致命,因此很容易被发现并及时补救。氨气比空气轻,泄漏后扩散快,不会聚积。泄漏在大气中的氨气还可以参与自然循环,随雨雪移动后,与其他物质反应或被植物吸收。
依据以上内容,回答下列问题。
(1)指出两点氨气的物理性质①___________。②____________。
(2)从阅读材料中可以看出,将氨气液化的一条途径是___________。
(3)氨气在氧气中燃烧生成![]() 和
和![]() 的化学方程式是___________。
的化学方程式是___________。
(4)写出工业上传统合成氨气的化学方程式___________。
(5)指出氨气的一条用途____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“见著知微,见微知著”是化学思维方法。
Ⅰ.从宏观知微观
①酒香不怕巷子深的微观解释为:______________。
②气体X在氧气中不完全燃烧生成硫和水,X中一定含有的元素是____________(填元素符号)。
Ⅱ.从微观知宏观。根据下列化学用语,按要求填空:
a ![]() b
b ![]() c
c  d
d 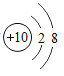
①表示结构相对最稳定的原子是________(填序号);
②a与c两粒子结合形成物质的化学式是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com