
【题目】T℃时,水的离子积为Kw,该温度下将a mol/L一元酸HA溶液与b mol/L一元碱BOH溶液等体积混合,若混合后溶液呈中性,则下列说法一定正确的是( )
A. 混合液中,c(H+) = ![]() B. 混合液的pH=7
B. 混合液的pH=7
C. 混合液中,c(B+) = c(A-) + c(OH-) D. a = b
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案科目:高中化学 来源: 题型:
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:

(1)反应的ΔH___0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为______mol·L-1·s-1;反应的平衡常数K1为________mol·L-1。
(2)100 ℃时达到平衡后,改变反应温度为T,N2O4以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。则T_______100 ℃(填“大于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题目信息完成下列方程式。
(1)钛(Ti)因为具有神奇的性能越来越引起人们的关注。地壳中含钛铁矿石之一是金红石(TiO2),目前大规模生产的方法是:
第一步:金红石、炭粉混合,在高温条件下,通入Cl2制得TiCl4和一种可燃气体,该反应的化学方程式为:____________________________________________;
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。写出此反应的化学方程式:____________________________________________。
(2)用100mL 0.1mol/L的NaOH溶液吸收224mLCO2气体(标准状况),恰好完全吸收。再将所得溶液加入100mL 0.1mol/L氢氧化钙溶液中。请写出所得溶液与氢氧化钙溶液反应的离子方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒夏特列原理解释的事实是( )
A.棕红色的NO2加压后颜色先变深后变浅
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C.黄绿色的氯水光照后颜色变浅
D.合成氨工业使用高压以提高氨的产量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2(g) ![]() 2NO(g)+O2(g)在一恒容的密闭容器中反应,达到平衡状态的标志是( )
2NO(g)+O2(g)在一恒容的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2 ②单位时间内生成n mol O2的同时生成2n mol NO ③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥混合气体的平均相对分子质量不再改变的状态 ⑦混合气体的压强不再改变的状态
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁在自然界中的含量丰富,而且在生活生产中应用广泛。
(1)铁在周期表中的位置为______。
(2)硝普试剂[Fe(NO)CN)5]2-可用于检验S2-,两者反应得紫色溶液,其中两个配体互为等电子体,已知硝普试剂[Fe(NO)(CN)5]2-中Fe为+2价,其基态离子的外围电子排布式为_______。
(3)K4[Fe(CN)6]溶液可用于检验Fe3+,K、C、N的第一电离能由大到小的顺序为______,K4[Fe(CN)6]内界中σ键与π键的个数比为______。
(4)二茂铁是由两个环戊二烯阴离子与Fe2+离子组成的三明治型化合物,即![]() 。环戊二烯分子(
。环戊二烯分子(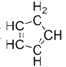 )中碳原子的杂化方式为_______。
)中碳原子的杂化方式为_______。
(5)工业电解熔融的FeO、Fe2O3冶炼高纯铁。FeO与Fe2O3相比,_____熔点高,其主要原因是_______。
(6)铁单质晶体在不同温度下有两种主要的堆积方式——体心立方(A)与面心立方(B),假定Fe原子半径不变,在两种堆积中,配位数之比NA︰NB为_______晶体密度之比ρA︰ρB为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图①、②、③、④、⑤五组仪器(可重复使用),选择合适的装置和药品能完成的实验是( )
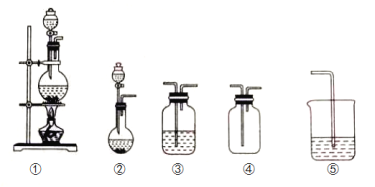
选项 | 实验目的 | 实验装置 | 实验药品 |
A | 制备并收集HCl气体 | ①③④ | 浓盐酸、浓硫酸、水 |
B | 比较氯气和溴的氧化性强弱 | ①③③⑤ | MnO2、浓盐酸、饱和食盐水、溴化钾溶液、氢氧化钠溶液 |
C | 探究乙烯的加成反应 | ①③ | 无水乙醇、浓硫酸、溴的四氯化碳溶液 |
D | 探究二氧化硫的还原性 | ②③③ | 亚硫酸钠、30%的硝酸、溴水、氢氧化钠溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2SO4溶液、K2CO3溶液、盐酸
(1)操作①的名称是___,操作②的名称是___。
(2)试剂a是___,固体B是___。(填化学式)
(3)生成沉淀A的离子反应方程式为:__加入试剂b所发生的化学反应方程式为:___。
(4)该方案能否达到实验目的:___。若不能,应如何改进(若能,此问不用回答)___。
(5)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素是一种重要的非金属元素,可形成多种化合物。试回答下列有关问题:
(1)①已知4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,改变某一反应条件,(已知温度T2>T1)下列图像正确的是_______(填代号)
4CO2(g)+N2(g) ΔH=-1 200 kJ·mol-1对于该反应,改变某一反应条件,(已知温度T2>T1)下列图像正确的是_______(填代号)

②已知CO与H2O在一定条件下可以发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH= - Q kJ·mol-1 ,820 ℃时在甲、乙两个恒容密闭容器中,起始时按照下表进行投料,经过一段时间后达到平衡状态,若甲中CO的转化率为40%,则该反应的平衡常数为____________;乙容器吸收的热量为________________。
CO2(g)+H2(g) ΔH= - Q kJ·mol-1 ,820 ℃时在甲、乙两个恒容密闭容器中,起始时按照下表进行投料,经过一段时间后达到平衡状态,若甲中CO的转化率为40%,则该反应的平衡常数为____________;乙容器吸收的热量为________________。
![]()
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气,已知:
① N2 (g) +2O2 (g) = N2O4 (l) ΔH =-19.5 kJ·mol-1
② N2H4(l)+O2(g) = N2(g) +2H2O(g) ΔH =-534.2 kJ·mol-1
写出肼与四氧化二氮反应的热化学方式______________。
(3)纯的叠氮酸(HN3)是无色液体,常用做引爆剂,常温下向25 mL 0.1mol·L-1 NaOH溶液中加入0. 2mol·L-1 HN3的溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如图。

①根据图像写出HN3的电离方程式:_________。
②下列说法正确的是_________________(填序号)
A.若用已知浓度的NaOH溶液滴定HN3溶液来测定HN3的浓度时应用甲基橙作指示剂
B.常温下,向0.2 mol·L-1 HN3的溶液中加水稀释,则![]() 不变
不变
C.分别中和pH均为4的HN3溶液和HCl溶液,消耗0.1 mol·L-1 NaOH溶液的体积相同
D.D点时溶液中离子浓度存在如下关系:2c(H+) + c(HN3) =c(N3-) + 2c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com