
【题目】铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。指明使用镁条和氯酸钾的目的是___________________。
(2)某同学用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见红色。为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示。
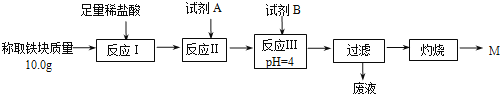
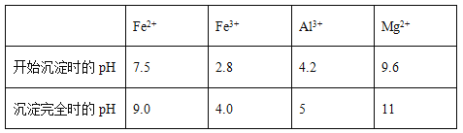
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
① 试剂A应选择________,试剂B应选择_______(填序号)。
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
② 写出反应Ⅱ的离子方程式____________________________。
③ 设计简单实验证明M的成分是Fe2O3而非Fe3O4__________。

④ 上述实验应灼烧至M质量不变,则能证明M质量不变的标志是_______。
⑤ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是_______。
【答案】引发铝热反应 C D 2Fe2++ H2O2+2H+=2Fe3++2H2O 足量稀硫酸;几滴(少量)高锰酸钾溶液;溶液紫红色未褪去 连续两次灼烧质量相差不大于0.1 g 84.0%
【解析】
(1)根据铝热反应需要高温条件分析解答。
(2)取反应后的“铁块”溶于盐酸,生成铁盐或亚铁盐、镁离子和铝离子,根据离子的性质结合流程图分析解答。
(1)使用镁条和氯酸钾的目的是点燃镁条燃烧放热促进氯酸钾分解生成氯化钾和氧气,起到高温引发铝热反应的目的,即使用镁条和氯酸钾的目的是引发铝热反应。
(2)①根据表格可知,要使铁元素完全沉淀而铝离子和镁离子不沉淀,需要将亚铁离子转化为铁离子,又因为不能引入新杂质,所以需要加入双氧水,然后调节4≤pH<4.2即可将铁离子沉淀而铝离子和镁离子不沉淀。调节pH时不能用氧化铁,因为会引入铁元素,因此试剂A应选择双氧水,试剂B应选择氨水,答案选C和D。
②反应Ⅱ是双氧水氧化亚铁离子,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O。
③氧化铁溶于酸生成铁离子,四氧化三铁溶于酸生成铁离子和亚铁离子,因此要设计简单实验证明M的成分是Fe2O3而非Fe3O4只需要证明溶液中含有亚铁离子即可,所以实验方案为取少量M固体于试管中,向其中加入足量稀硫酸,固体完全溶解,溶液呈棕黄色,继续向上层溶液中滴加几滴少量高锰酸钾溶液,振荡观察紫红色溶液未褪去,说明不含有亚铁离子。
④上述实验应灼烧至M质量不变,则能证明M质量不变的标志是连续两次灼烧质量相差不大于0.1 g。
⑤若最终红色粉未M的质量为12.0 g,即氧化铁是12.0g,物质的量是12.0g÷160g/mol=0.075mol,所以铁元素的质量是0.075mol×2×56g/mol=8.4g,则该“铁块”的纯度是8.4g/10g×100%=84.0%。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】元素周期表的一部分如图所示,W、X、Y、Z均为短周期主族元素,X与Z的最高正价之和与W的相等。下列说法错误的是
![]()
A.原子半径:X>Y>Z>W
B.X2W2中含有离子键和共价键
C.Y的最高价氧化物对应的水化物难溶于水
D.将由X、Z的单质组成的混合物放入冷水中,Z的单质不发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如下流程:

下列说法不正确的是( )
A. 溶解烧渣选用足量硫酸,试剂X选用铁粉
B. 固体1中一定含有SiO2,控制pH是为了使Al3+转化为Al(OH)3,进入固体2
C. 从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解
D. 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组设计出利用工业废酸(稀硫酸)来浸取某废弃的氧化铜锌矿的方案,实现废物综合利用,方案如图所示。

已知:各离子开始沉淀及完全沉淀时的pH如表所示:

请回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,除通入空气“搅拌”外,还可采取的措施是(任写一点即可)__________________________________________________________。
(2)物质A最好使用下列物质中的____________(填选项序号)。
A.KMnO4 B.H2O2 C.HNO3
(3)除铁过程中加入氨水的目的是调节溶液的pH,pH应控制在__________范围之间。
(4)物质B可直接用作氮肥,则B的化学式是________。
(5)除铁后得到的氢氧化铁可用次氯酸钾溶液在碱性环境将其氧化得到一种高效的多功能处理剂(K2FeO4),写出该反应的离子方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表示下列过程的方程式正确的是
A.氨水中一水合氨的电离方程式: NH3·H2O =![]() +OH-
+OH-
B.用浓HNO3溶解铜的离子方程式: 3Cu+2![]() + 8H+==3Cu2+ + 2NO↑+ 4H2O
+ 8H+==3Cu2+ + 2NO↑+ 4H2O
C.苯和硝酸反应的化学方程式:![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
D.钢铁发生电化学腐蚀时负极的电极反应式: Fe-3e- = Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
(1) CO2经催化加氢可合成低碳烯烃: 2CO2(g)+6H2(g)CH4(g)+4H2O(g),正反应放热。在1L恒容密闭容器内,按n(CO2): n(H2)=1:3投料,测得各组分物质的量随时间变化如下图所示:
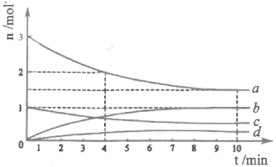
①该反应的△H____(填 “>”,“=”或“<" )0。
②曲线b表示的物质为____ (填化学式),该物质在0~4min内的平均反应速率为______。(保留2位小数)
(2)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如下图所示
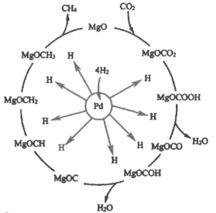
①该反应的化学方程式为_________;
②理论上每有1mol CO2参加反应,反应过程中转移的电子数为_______ mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应H2(g)+I2(g)![]() 2HI(g)达到平衡状态时的标志是( )
2HI(g)达到平衡状态时的标志是( )
A.混合气体的体积恒定不变
B.混合气体的颜色不再改变
C.H2、I2、HI的浓度相等
D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,表中列出12种元素在周期表中的位置,按要求回答下列问题。
周期\族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑥ | (11) | ⑧ | ⑩ | ||||
三 | ① | ③ | ⑤ | ⑦ | (12) | ⑨ | ||
四 | ② | ④ |
(1)在这12种元素中,化学性质最不活泼的元素名称是______,得电子能力最强的原子是_____(用元素符号表示);元素⑦的最高价氧化物对应的水化物是_____(写化学式)。
(2)
(3)①⑧⑨三种元素单核离子半径由大到小的顺序是(用相应的离子符号表示) ______。
(4)请写出:
(ⅰ) ③的单质置换出⑥的单质的化学方程式:_________________________。
(ⅱ) ⑤和(11)两种元素最高价氧化物对应的水化物相互反应的离子方程式为___________。
(ⅲ)元素⑨的单质和元素①的最高价氧化物对应的水化物常温下反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X的结构简式如图所示。下列有关化合物X的说法正确的是
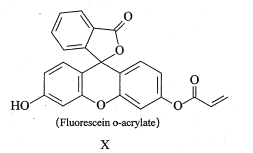
A.分子中3个苯环处于同一平面
B.分子中只有1个手性碳原子
C.1molX最多能与lmolBr2反应
D.1molX 与NaOH溶液反应时最多消耗4molNaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com