
ΓΨΧβΡΩΓΩ±Ϋ““ΆΣ≥ΘΈ¬œ¬ΈΣΈό…ΪΨßΧεΜρ«≥ΜΤ…Ϊ”ΆΉ¥“ΚΧεΘ§ «…ΫιΪΓΔΚ§–Ώ≤ίΓΔΉœΕΓœψΒ»œψΨΪΒΡΒςΚœ‘≠ΝœΘ§≤ΔΙψΖΚ”Ο”Ύ‘μ”ΟœψΨΪΚΆ―Χ≤ίœψΨΪ÷–Θ§Ω…”…±ΫΨ≠œ¬ ωΖ¥”Π÷Τ±ΗΘΚ
![]() +(CH3CO)2O(““Υατϊ)
+(CH3CO)2O(““Υατϊ) ![]() +CH3COOHΘ§ NA¥ζ±μΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
+CH3COOHΘ§ NA¥ζ±μΑΔΖϋΦ”Β¬¬ό≥Θ ΐΒΡ÷ΒΓΘœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
A.1 mol±ΫΥυΚ§ΒΡΜ·―ßΒΞΦϋ ΐΡΩΈΣ12NA
B.0.1 mol““Υατϊ÷–Κ§”–ΒΡΒγΉ” ΐΡΩΈΣ5.4NA
C.ΤχΧ§±Ϋ““ΆΣΒΡΟήΕ» «ΤχΧ§““ΥαΟήΕ»ΒΡ2±Ε
D.1L 2 molΓΛLΘ≠1 CH3COOH»ή“Κ”κΉψΝΩΡΤΖ¥”Π…ζ≥…ΒΡΤχΧεΖ÷Ή” ΐΈΣNA
ΓΨ¥πΑΗΓΩB
ΓΨΫβΈωΓΩ
A. ±Ϋ÷–6ΗωΧΦ–Έ≥…![]() ΦϋΘ§1 mol±ΫΥυΚ§ΒΡΜ·―ßΒΞΦϋC-H ΐΡΩΈΣ6NAΘ§Ι A¥μΈσΘΜ
ΦϋΘ§1 mol±ΫΥυΚ§ΒΡΜ·―ßΒΞΦϋC-H ΐΡΩΈΣ6NAΘ§Ι A¥μΈσΘΜ
B. 0.1 mol““Υατϊ÷–Κ§”–ΒΡΒγΉ” ΐΡΩΈΣ0.1ΓΝΘ®6ΓΝ4+8ΓΝ3+1ΓΝ6Θ©NA=5.4NAΘ§Ι B’ΐ»ΖΘΜ
C. ΤχΧεΟήΕ»”κΤχΧεΉ¥Χ§”–ΙΊΘ§ΤχΧεΉ¥ΩωΈ¥÷ΣΘ§ΈόΖ®±»ΫœΟήΕ»¥σ–ΓΘ§Ι C¥μΈσΘΜ
D. ¥ΉΥα»ή“Κ÷–Θ§¥ΉΥαΖ÷Ή”ΓΔΥ°Ζ÷Ή”ΕΦΡή”κΡΤΖ¥”Π≤ζ…ζ«βΤχΘ§Υυ“‘1L 2 molΓΛLΘ≠1CH3COOH»ή“Κ”κΉψΝΩΡΤΖ¥”Π…ζ≥…ΒΡΤχΧεΖ÷Ή” ΐ‘Ε‘Ε¥σ”ΎNAΘ§Ι D¥μΈσΘΜ
Ι ―ΓBΓΘ


 ‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥÷÷Α±≈πΆι(NH3ΓΛBH3)Βγ≥ΊΉΑ÷Ο»γΆΦΥυ Ψ(Έ¥Φ”»κΑ±≈πΆι÷°«ΑΘ§ΝΫΦΪ “ΡΎ“ΚΧε÷ ΝΩœύΒ»)Θ§Βγ≥ΊΖ¥”ΠΈΣNH3ΓΛBH3+3H2O=NH4BO2+4H2O(≤ΜΩΦ¬«ΤδΥϊΖ¥”ΠΒΡ”Αœλ)ΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
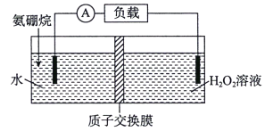
A.Α±≈πΆι÷–NΚΆBΒΡ‘”Μ·ΖΫ Ϋ≤ΜΆ§
B.Βγ≥Ί’ΐΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣH2O2+2H++2e-=2H2O
C.ΤδΥϊΧθΦΰ≤Μ±δΘ§œρH2O2»ή“Κ÷–Φ”»κ ΝΩΝρΥαΡή‘ω¥σΒγΝς«ΩΕ»
D.»τΦ”»κΒΡΑ±≈πΆι»Ϊ≤ΩΖ≈ΒγΚσΉσ”“ΝΫΦΪ “ΡΎ“ΚΧε÷ ΝΩ≤νΈΣ3.8gΘ§‘ρΒγ¬Ζ÷–ΉΣ“Τ1.2molΒγΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”–BaCl2ΚΆNaClΒΡΜλΚœ»ή“ΚVLΘ§ΫΪΥϋΖ÷≥…ΝΫΒ»ΖίΓΘ“ΜΖίΒΈΦ”œΓΝρΥαΘ§ ΙBa2+Άξ»Ϊ≥ΝΒμΘΜΝμ“ΜΖίΒΈΦ”AgNO3»ή“ΚΘ§ ΙCl-Άξ»Ϊ≥ΝΒμΓΘΖ¥”Π÷–œϊΚΡamolH2SO4ΓΔbmolAgNO3ΓΘ‘ρ‘≠ΜλΚœ»ή“Κ÷–ΒΡc(Na+)ΈΣ(ΓΓΓΓ)
A. ![]() mol/LB.
mol/LB. ![]() mol/LC.
mol/LC. ![]() mol/LD.
mol/LD. ![]() mol/L
mol/L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Κλ…ΪΙΧΧεΖέΡ©Ω…Ρή «Fe2O3ΓΔCu2OΜρΕΰ’ΏΜλΚœΈοΘ§ΈΣΧΫΨΩΤδΉι≥…Θ§≥Τ»ΓmgΗΟΙΧΧεΖέΡ©―υΤΖΘ§”ΟΉψΝΩΒΡœΓH2SO4≥δΖ÷Ζ¥”ΠΚσΘ§≥ΤΒΟΙΧΧε÷ ΝΩΈΣagΓΘ
“―÷ΣΘΚCu2O+2H+ = Cu+Cu2++H2O
(1)»τa=____________(”ΟΚ§mΒΡΉνΦρ Ϋ±μ Ψ)Θ§‘ρΚλ…ΪΙΧΧεΖέΡ©ΈΣ¥ΩΨΜΈοΘΜ
(2)»τa=m/9Θ§‘ρΚλ…ΪΙΧΧεΖέΡ©÷–Fe2O3ΒΡΈο÷ ΒΡΝΩΈΣ____________mol(”ΟΚ§mΒΡΉνΦρ Ϋ±μ Ψ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ© Β―ι “÷Τ¬»ΤχΒΡΈ≤Τχ¥Πάμ”Ο_____»ή“ΚΈϋ ’Θ§ΤδΜ·―ßΖ¥”ΠΖΫ≥Χ ΫΈΣ_____ΓΘ
Θ®2Θ©œρAlCl3»ή“Κ÷–÷πΒΈΦ”»κNaOH»ή“ΚΘ§œ÷œσ «œ»≤ζ…ζΑΉ…Ϊ≥ΝΒμΘ§ΤδΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_____Θ§ΚσΑΉ…Ϊ≥ΝΒμ”÷»ήΫβœϊ ßΘ§ΤδΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_____ΓΘ
Θ®3Θ©‘ΎΚ§”–0.2molΒΡΝρΥαΚΆ0.2molΒΡœθΥαΒΡΜλΚœ»ή“Κ200mL÷–Θ§Φ”»κ19.2gΆ≠ΖέΘ§≤ζ…ζΒΡΤχΧε≥…Ζ÷ΈΣ_____Θ®ΧνNOΜρH2Θ©Θ§ΡψΥυ―ΓΤχΧε‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣ_____L
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ΘΈ¬ ±Θ§œρ120 mL 0.005 molΓΛLΘ≠1 CaCl2»ή“Κ÷–÷πΒΈΦ”»κ0.1 molΓΛLΘ≠1 Na2CO3»ή“ΚΘ§ΜλΚœ»ή“ΚΒΡΒγΒΦ¬ ±δΜ·«ζœΏ»γΆΦΥυ ΨΓΘ“―÷Σ25Γφ ±Θ§Ksp(CaCO3)=3.36ΓΝ10Θ≠9Θ§Κω¬‘CO32-Υ°ΫβΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
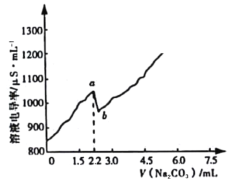
A.aΒψΕ‘”ΠΒΡ»ή“Κ÷–Ca2+ΩΣ Φ–Έ≥…≥ΝΒμΘ§»ή“Κ÷–c(Ca2+)=c(CO32Θ≠)
B.bΒψΕ‘”ΠΒΡ»ή“Κ÷–Ca2+“―Άξ»Ϊ≥ΝΒμΘ§«“¥φ‘ΎΙΊœΒΘΚc(Na+)+c(H+)=c(ClΘ≠)+c(OHΘ≠)
C.‘ΎΒΈΦ”Na2CO3»ή“ΚΒΡΙΐ≥Χ÷–Θ§ΜλΚœ»ή“ΚΒΡpHœ»Φθ–ΓΚσ‘ω¥σ
D.”“ΆΦΩ…“‘ΥΒΟςCaCO3‘Ύ»ή“Κ÷–¥φ‘ΎΙΐ±ΞΚΆœ÷œσ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≥ύΆ≠ΩσΒΡ÷ς“Σ≥…Ζ÷ «Cu2OΘ§Μ‘Ά≠ΩσΒΡ÷ς“Σ≥…Ζ÷ «Cu2SΘ§ΫΪ≥ύΆ≠Ωσ”κΜ‘Ά≠ΩσΜλΚœΦ”»»ΖΔ…ζ“‘œ¬Ζ¥”ΠΘΚ
Cu2S+2Cu2O=6Cu+SO2ΓϋΘ§ΙΊ”ΎΗΟΖ¥”ΠΒΡΥΒΖ®÷–’ΐ»ΖΒΡ «
A.ΗΟΖ¥”ΠΒΡ―θΜ·ΦΝ”κΜΙ‘≠ΦΝΈο÷ ΒΡΝΩ÷°±»ΈΣ2ΘΚ1
B.Cu2S ‘ΎΖ¥”Π÷–÷ΜΉωΜΙ‘≠ΦΝ
C.Cu «―θΜ·≤ζΈοΘ§SO2 «ΜΙ‘≠≤ζΈο
D.ΟΩ…ζ≥…38.4gCuΘ§Ζ¥”Π÷–ΉΣ“Τ0.6molΒγΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣΦΉΈΣΚψ―Ι»ίΤςΓΔ““ΈΣΚψ»ί»ίΤςΓΘœύΆ§ΧθΦΰœ¬≥δ»κΒ»Έο÷ ΒΡΝΩΒΡNO2ΤχΧεΘ§«“Τπ Φ ±ΧεΜΐœύΆ§ΓΘΖΔ…ζΖ¥”ΠΘΚ2NO2(g)![]() N2O4(g)ΓςHΘΦ0ΓΘ“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΉ¥Χ§Θ§œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «
N2O4(g)ΓςHΘΦ0ΓΘ“ΜΕΈ ±ΦδΚσ¥οΒΫΤΫΚβΉ¥Χ§Θ§œ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «
A.ΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐ±μ¥ο ΫK=![]()
B.¥οΒΫΤΫΚβΥυ–η ±ΦδΘ§ΦΉ”κ““œύΒ»
C.ΤΫΚβ ±NO2ΧεΜΐΖ÷ ΐΘΚΦΉΘΦ““
D.»τΝΫ»ίΤςΡΎΤχΧεΒΡ―Ι«Ω±Θ≥÷≤Μ±δΘ§ΨυΥΒΟςΖ¥”Π“―¥οΒΫΤΫΚβΉ¥Χ§
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ‘Ύ150Γφ ±ΧΦΥαοßΩ…“‘ ή»»Άξ»ΪΖ÷ΫβΘ§(NH4)2CO3 ![]() 2NH3Γϋ + H2OΓϋ + CO2ΓϋΘ§‘ρΤδΆξ»ΪΖ÷ΫβΚσΥυ≤ζ…ζΒΡΤχΧ§ΜλΚœΈοΒΡΟήΕ» «œύΆ§ΧθΦΰœ¬«βΤχΟήΕ»ΒΡΦΗ±Ε
2NH3Γϋ + H2OΓϋ + CO2ΓϋΘ§‘ρΤδΆξ»ΪΖ÷ΫβΚσΥυ≤ζ…ζΒΡΤχΧ§ΜλΚœΈοΒΡΟήΕ» «œύΆ§ΧθΦΰœ¬«βΤχΟήΕ»ΒΡΦΗ±Ε
A. 96±Ε B. 48±Ε C. 12±Ε D. 32±Ε
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com