
【题目】镍是有机合成的重要催化剂。某化工厂有含镍催化剂废品(主要成分是镍,杂质是铁、铝单质及其化合物,少量难溶性杂质)。某学习小组设计如下流程利用含镍催化剂废品制备硫酸镍晶体:
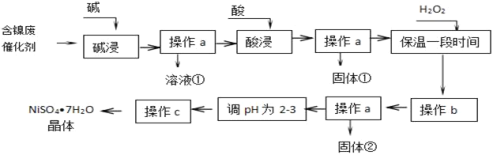
几种难溶碱开始沉淀和完全沉淀的pH:
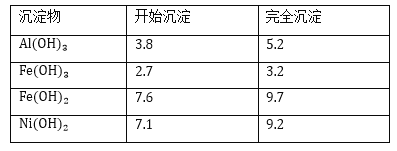
回答下列问题:
(1)溶液①中含金属元素的离子是_________;
(2)用离子方程式表示加入双氧水的目的______________;双氧水可以用下列物质替代的是_________
A.氧气 ![]() 漂白液
漂白液 ![]() 氯气
氯气 ![]() 硝酸;
硝酸;
(3)操作b调节溶液pH范围为______________;
(4)操作a和c需要共同的玻璃仪器是_______;上述流程中,防止浓缩结晶过程中,Ni2+水解的措施是_______。
【答案】AlO2- 2Fe2++H2O2+2H+=2Fe3++2H2O A 3.2![]() pH<7.1 玻璃棒 调节溶液pH为2--3
pH<7.1 玻璃棒 调节溶液pH为2--3
【解析】
(1)根据废料成分知,碱和铝、氧化铝反应,溶液中含有偏铝酸根离子;
(2)根据数据表知,应将亚铁离子转化成铁离子除去,且不能引入新的杂质离子;
(3)调节溶液pH使Fe3+完全沉淀,使Ni2+不沉淀,分离出固体是氢氧化铁;
(4)过滤、蒸发都需要用玻璃仪器:玻璃棒;硫酸镍是强酸弱碱盐,根据盐的水解规律判断选择的条件。
(1)碱和铝、氧化铝均能反应,溶液中含有的含有金属的离子是AlO2-;
(2)亚铁离子具有还原性,双氧水具有氧化性,加入双氧水是为了氧化亚铁离子成为铁离子,离子反应方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O。选项的物质都具有强的氧化性,会把Fe2+氧化为Fe3+,但漂白液(主要成分次氯酸钠)、氯气、硝酸替代双氧水会引入新杂质,而氧气不能引入杂质离子,故可以用作替代试剂为氧气,合理选项是A;
(3)由表格可知,氢氧化铁的沉淀范围为,2.7-3.2,镍离子的沉淀范围是7.1-9.2,调节溶液的pH在3.2-7.1,既可以除去杂质铁离子,而又不使镍离子形成沉淀;
(4)操作a是过滤得到固体和滤液,操作c是蒸发浓缩得到晶体过滤得到NiSO47H2O,操作a、c中均需使用的仪器为玻璃棒;镍离子水解使溶液呈酸性,根据盐的水解规律,为抑制镍离子水解,溶液始终保持酸性,调节溶液pH为2—3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
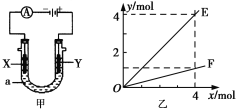
【题目】电解原理在化学工业中有着广泛的应用。图甲表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。则下列说法不正确的是( )
A. 若此装置用于电解精炼铜,则X为纯铜、Y为粗铜,电解的溶液a可以是硫酸铜或氯化铜溶液
B. 按图甲装置用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,加入0.5 mol的碳酸铜刚好恢复到通电前的浓度和pH,则电解过程中转移的电子为2.0 mol
C. 按图甲装置用惰性电极电解AgNO3溶液,若图乙横坐标x表示流入电极的电子的物质的量,则E可表示反应生成硝酸的物质的量,F表示电解生成气体的物质的量
D. 若X、Y为铂电极,a溶液为500 mL KCl和KNO3的混合液,经过一段时间后,两极均得到标准状况下11.2 L气体,则原混合液中KCl的物质的量浓度至少为2.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下,两个容积相同的烧瓶中分别盛满X和Y两种气体,打开开关a,使两烧瓶内的气体相通,最后容器内的压强由大到小的顺序排列正确的是

编号 | ① | ② | ③ | ④ |
气体X | HI | NH3 | H2 | NO |
气体Y | Cl2 | HCl | Cl2 | O2 |
A. ②>③>①>④ B. ③>①=④>②
C. ③>①>④>② D. ④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①R—![]() —
—![]()
②苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
以下是用苯作原料制备一系列化合物的转化关系图:

(1)A转化为B的化学方程式是_______________________________________。
(2)图中“苯→①→②”省略了反应条件,请写出①、②物质的结构简式:
①________________________,②____________________________。
(3)B在苯环上的二氯代物有 种同分异构体。
(4)有机物 的所有原子 (填“是”或“不是”)在同一平面上。
的所有原子 (填“是”或“不是”)在同一平面上。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)________。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
(2)若链烃A分子中所有的碳原子共平面,则A的结构简式为_____________;
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3:2:1,且不存在顺反异构体,则A的名称为_____。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下![]()
![]()
![]() 个HCl分子
个HCl分子 ![]()
![]()
![]()
![]() ,下列对这四种气体的关系从大到小表达正确的是( )
,下列对这四种气体的关系从大到小表达正确的是( )
![]() 体积
体积![]() 密度
密度![]()
![]() 电子总数
电子总数![]() 原子总数
原子总数![]()
A. abcdB. bcdC. acdD. abc
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
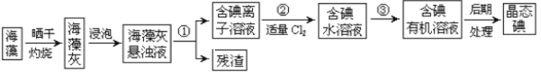
(1)指出提取碘的过程中有关的实验操作名称:①_________;③__________
(2)提取碘的过程中,可选择的有机试剂是:___________
A.酒精 B.四氯化碳 C.苯
(3)实验操作③中,实验室已有烧杯、玻璃棒以及必要的夹持仪器,尚缺少的玻璃仪器是__________。
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出实验装置图中的错误之处:

①____;②_________;③__________。
(5)最后晶态碘在_____________里聚集(填仪器名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4 溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是
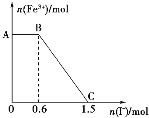
A. 图中AB段的氧化剂为K2Cr2O7
B. 图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C. 若将上述过程中的KI溶液换为K3[Fe(CN)6]溶液,则AB段有蓝色沉淀生成
D. 开始加入的K2Cr2O7为0.25 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com