
【题目】25℃,向40mL0.05mol/L的FeCl3溶液中加入10mL0.15mol/L的KSCN溶液,发生反应:Fe3++3SCN-![]() Fe(SCN)3,混合溶液中c(Fe3+)与反应时间(t)的变化如图所示。(盐类的水解影响忽略不计)下列说法正确的是( )
Fe(SCN)3,混合溶液中c(Fe3+)与反应时间(t)的变化如图所示。(盐类的水解影响忽略不计)下列说法正确的是( )
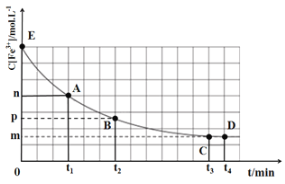
A.在该反应过程中,A点的正反应速率小于B点的逆反应速率
B.E点对应的坐标为(0,0.05)
C.该反应的平衡常数K=
D.t4时向溶液中加入50mL0.1mol/LKCl溶液,平衡不移动
【答案】C
【解析】
A.A点反应物浓度大于B点反应物浓度,A和B两点均没有达到平衡状态,则在该反应过程中,A点的正反应速率大于B点的逆反应速率,A错误;
B.E点混合后溶液的浓度为(0.04L×0.05mol/L)÷0.05L=0.04mol/L,则E点坐标为(0,0.04),B错误;
C.由图可知,平衡时Fe3+浓度为m,则络合离子浓度为0.04-m,SCN-的浓度为(0.01×0.15)÷0.05-3×(0.04-m)=3m-0.09,则K= ,C正确;
,C正确;
D.t4时向溶液中加入50mL 0.1mol/L KCl溶液,溶液总体积增大,浓度减小,向浓度增大的方向移动,即逆向移动,D错误;答案选C。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如图:
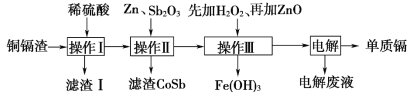
表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1mol·L-1)
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.2 |
沉淀完全的pH | 3.3 | 9.9 | 9.5 |
(1)酸浸时粉碎铜镉渣的目的是___。
(2)操作Ⅰ产生的滤渣主要成分为__(填化学式)。
(3)①操作Ⅲ中先加入适量H2O2,发生反应的离子方程式为__。
②再加入ZnO控制反应液的pH,pH范围为__,判断依据是__。
③若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以鉴别:__。
(4)处理含镉废水常用加入碳酸钙实现沉淀转化,该沉淀转化的反应方程式为___。除去工业废水中的Cd2+时,若反应达到平衡后溶液中c(Ca2+)=0.1mol·L-1,溶液中c(Cd2+)=__mol·L-1[已知25℃,Ksp(CdCO3)=5.6×10-12,Ksp(CaCO3)=2.8×10-9]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)=2CO2(g) △H=-566 kJ·mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g) △H=-452 kJ·mol-1
根据以上热化学方程式判断,下列说法正确的是
A. 1molCO 完全燃烧,放出热量为283 J
B. Na2O2(s)+CO2(s)=Na2CO3(s)+ ![]() O2(g) △H=-226 kJ·mol-l
O2(g) △H=-226 kJ·mol-l
C. CO(g) 与Na2O2(s)反应放出509kJ 热量时,电子转移数为1.204×1024
D. CO 的燃烧热为566 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是药物合成的一种中间体,可通过以下方法合成:
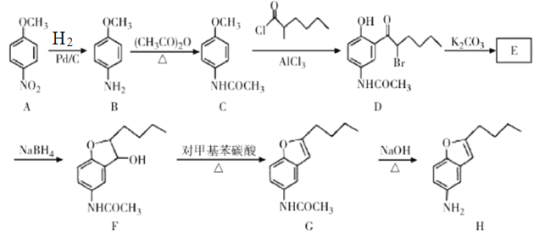
(1)B中官能团名称为____________。
(2)G→H的反应类型为____________。
(3)已知C的一种同分异构体为: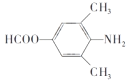 ,下列说法正确的是________。
,下列说法正确的是________。
a.能发生酯化反应
b.能发生银镜反应
c.l mol该物质完全水解产物能消耗3 mol NaOH
d.该分子的核磁共振氢谱中峰面积之比为1:2:6:2
e.其水解产物之一能与FeCl3溶液发生显色反应
(4) 中手性碳原子个数为____________。
中手性碳原子个数为____________。
(5)E的分子是为C14H17O3N,E经还原得到F,写出E→F的反应方程式______________。
(6)已知:①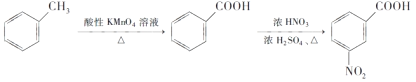
②苯胺(![]() )易被氧化
)易被氧化
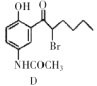
请以甲苯和(CH3CO)2O为原料制备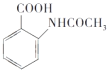 ,写出制备的合成路线流程图(无机试剂任选)______________。
,写出制备的合成路线流程图(无机试剂任选)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2A(g)+B(g)![]() 3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
3C(g)+D(s)△H<0,在其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是
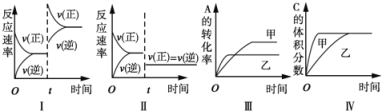
A. 图I表示增加反应物浓度对该平衡的影响
B. 图II表示减小压强对该平衡的影响
C. 图Ⅲ表示温度对该平衡的影响,温度:乙>甲
D. 图IV表示催化剂对该平衡的影响,催化效率:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是_____,D是_____,G是_____,H是_____(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:__________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为_________。
(3)A中元素的原子结构示意图为________。
(4)F在溶液中的电离方程式为_________。
(5)上述反应中属于氧化还原反应的是_______(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在密闭容器中充入CO2与H2进行反应:2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):
CH3OCH3(g)+3H2O(g) ΔH。采用催化剂甲和催化剂乙分别发生上述反应,测得反应进行相同时间时CO2的转化率α(CO2)随反应温度T的变化曲线如下图所示(忽略温度对催化剂活性的影响):
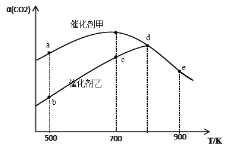
下列叙述正确的是
A. 该可逆反应的ΔH>0
B. 催化剂甲作用下反应的活化能比催化剂乙作用下反应的活化能大
C. 500K下达到平衡时,反应在催化剂甲作用下的转化率比在催化剂乙作用下的转化率高
D. d、e两点反应已经达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常监测SO2含量是否达到排放标准的反应原理是SO2+H2O2+BaCl2=BaSO4↓+2HCl。NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 molBaCl2晶体中所含离子总数为0.1NA
B.25℃时,pH=1的HCl溶液中含有H+ 的数目为0.1NA
C.l7g H2O2中含有非极性键数目为0.5NA
D.生成2.33gBaSO4沉淀时,转移电子数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,水既作氧化剂又作还原剂的是( )
A. 2F2+2H2O===4HF+O2 B. 2Na+2H2O===2NaOH+H2↑
C. CaO+H2O===Ca(OH)2 D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com