
����Ŀ��2019��10��9�գ����ʼҿ�ѧԺ��˹�¸��Ħ����2019���ŵ������ѧ������������ӵ�صķ�չ�����������Ŀ�ѧ�ҡ�﮵����Ϊ����Ҫ�ı�Яʽ����Դ��Ӱ������������ķ������档﮿�����طŵ�Ĺ���ԭ����ͼ��ʾ������������ȷ���ǣ� ��
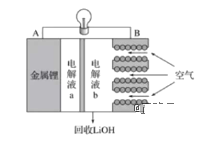
A.��طŵ�ʱ�����缫����ʽΪO2+2H2O+4e-=4OH-
B.�ŵ�ʱ������B����A���ƶ�
C.���Һa��b֮��ɲ��������ӽ���Ĥ
D.���Һb����ΪϡLiOH��Һ
���𰸡�D
��������
﮿����������ԭ��أ�﮵缫��Ϊԭ��صĸ�������������Ӧ��ͨ�������һ����Ϊԭ��������������乤��ԭ��ͼ��֪���ʧȥ���Ӻ���������Ӳ�Ǩ�������Һb����LiOH����ʽ���л��գ��ʵ�صĿ����缫����ΪOH-����ϸ���Ǩ�ƹ���������ӣ��Դ˽��н���⡣
A��������������֪����طŵ�ʱ�����ĵ缫��ӦʽΪ��Li-e-=Li+����A����
B���ŵ�ʱ�缫AΪ�������缫BΪ������������A����B���ƶ�����B����
C��������������֪�����ӽ���ĤӦ���������ӽ���Ĥ����C����
D��������������֪�����Һb����ΪϡLiOH��Һ����D��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ˮ�ĵ���ƽ��������ͼ��ʾ���Իش��������⣺
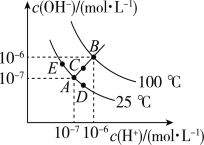
��1��ͼ��ABCDE����KW��Ĵ�С��ϵ��___________������ABCDE��ʾ��
��2������A�㵽D�㣬�ɲ��õĴ�ʩ��______��
a������
b����������������
c������������NaOH����
��3����B��Ӧ�¶������£�ij��ҺpH�T7����ʱ����Һ��____�����ԡ����ԡ����ԣ�����E��Ӧ���¶��£���pH=9��NaOH��Һ��pH=4��H2SO4��Һ��ϣ������û����Һ��pH=7����NaOH��Һ��H2SO4��Һ�������Ϊ________��
��4����B��Ӧ���¶��£���100���pH1=a��ijǿ����Һ��1���pH2=b��ijǿ����Һ��Ϻ���Һ�����ԣ�����ǰ����ǿ���pH1��ǿ���pH2֮��Ӧ����Ĺ�ϵ��pH1+ pH2= ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D��E��F��GΪ���ֶ���������Ԫ�أ�ԭ����������������֪��A��F�������������ֱ���ڸ��Եĵ��Ӳ���������A�ĵ����ڳ�����Ϊ���塣C��B��G��Ԫ�����ڱ��д�������λ�ã�������Ԫ��ԭ�ӵ�����������֮��Ϊ17��������֮��Ϊ31��D��Fͬ���ڣ����ڸ�������DԪ�ص�ԭ�Ӱ뾶�����������Ϣ�ش��������⣺
(1)B��C��G���⻯�����ȶ�����ǿ����__________(�ѧʽ)��G��ij����������ʹ��ˮ��ɫ��д���÷�Ӧ�Ļ�ѧ����ʽ__________________________________________��
(2)B��C��D��E��F�γɵļ����Ӱ뾶�ɴ�С��˳��Ϊ__________________(�����ӷ��ű�ʾ)��
(3)A��B���γ����ӻ�����A5B��A5B�мȺ����Ӽ��ֺ����ۼ��������ʽΪ________������������ˮ���ҷ�Ӧ�����������壬����������Ļ�ѧʽ��__________��
(4)D��A��C��̼Ԫ����ɵĻ������ˮ��Һ��________�ԣ������ӷ���ʽ������ԭ��________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1mol/LNaOH��Һ�ֱ�ζ������Ϊ20mL��Ũ�Ⱦ�Ϊ0.1mol/LHCl��Һ��HX��Һ����Һ��pH������NaOH��Һ����仯��ͼ������˵����ȷ����
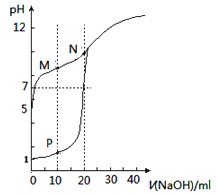
A. M��c(HX)-c(X-)>c(OH-)-c(H+)
B. N���pH>7��ԭ��������NaOH��������
C. HXΪ���ᣬ�ҵ���ƽ�ⳣ��Ka��1��10-10
D. P��c(Cl-)=0.05mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ��һ���ܴ���������ǣ� ��
A.��Ư��Һ�У�Ag+��K+��NO3-��SO32-
B.K+��Na+��Br-��AlO2-����Һ���ܴ������棬ͨ�������CO2�����ܴ�������
C.![]() =1012����Һ�У�NH4+��Ca2+��Cl-��NO3-
=1012����Һ�У�NH4+��Ca2+��Cl-��NO3-
D.��ˮ�����c(H+)=1��10-10mol/L����Һ�У�K+��Na+��HCO3-��AlO2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ŵ���������ڵ���ľ���ͻ�ױƷ�������㾫��ŵ������һ���Ʊ�������ͼ��ʾ������˵����ȷ����( )
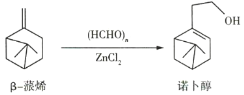
A.�������![]() ��Һ������-��ϩ��ŵ����
��Һ������-��ϩ��ŵ����
B.��-��ϩ�ı���̼ԭ���ϵ�һ�ȴ��������7��
C.��-��ϩ��ŵ���������ж���һ����5��̼ԭ�ӹ��ɵ�������
D.�������Ը��������Һ������-��ϩ��ŵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�߷��ӻ�����M�ĺϳ�·�����£�
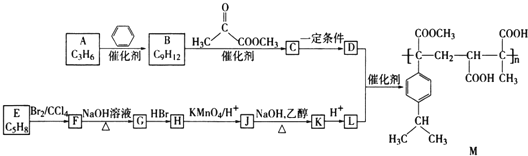
��֪��R-CH2OH![]() R-COOH��ʾ��������
R-COOH��ʾ��������![]() �ش��������⣺
�ش��������⣺
(1)![]() �ķ�Ӧ������ ______ ��
�ķ�Ӧ������ ______ ��
(2)![]() �ķ�Ӧ����Ϊ ______ ��
�ķ�Ӧ����Ϊ ______ ��
(3)![]() ����ʹ������Ȼ�̼��Һ��ɫ����E��ϵͳ������ ______ ��
����ʹ������Ȼ�̼��Һ��ɫ����E��ϵͳ������ ______ ��
(4)��Ʒ�Ӧ![]() ��
��![]() ��Ŀ���� ______ ��
��Ŀ���� ______ ��
(5)![]() �����ֿ��ܵĽṹ��Ϊ��ȷ����ṹ��ѡ�õ������� ______
�����ֿ��ܵĽṹ��Ϊ��ȷ����ṹ��ѡ�õ������� ______ ![]() �����
�����![]() ��
��
![]() ���������
���������![]() ������
������![]() Ԫ�ط�����
Ԫ�ط�����![]() �˴Ź�����
�˴Ź�����
(6)�߷��ӻ�����M�ĵ���Ϊ ______ ![]() д�ṹ��ʽ
д�ṹ��ʽ![]() ��
��
(7)![]() �Ļ�ѧ����ʽΪ ______ ��
�Ļ�ѧ����ʽΪ ______ ��
(8)��L������ͬ�����ŵ�L��ͬ���칹�廹�� ______ �֣����к˴Ź�������Ϊ3��壬�������Ϊ3��2��1���� ______ ![]() д�ṹ��ʽ
д�ṹ��ʽ![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и����������ض���Һ��һ���ܴ����������
A.pH=12�ij������Һ�У�K+��Na+��MnO![]() ��SO
��SO![]()
B.c��Al3+��=0.1molL��1����Һ�У�Na+��Cl����HCO![]() ��SO
��SO![]()
C.���ȳʺ�ɫ����Һ�У�NH![]() ��Ba2+��AlO
��Ba2+��AlO![]() ��Cl��
��Cl��
D.�����������ۺ��ܲ�����������Һ�У�NH![]() ��Fe2+��NO
��Fe2+��NO![]() ��SO
��SO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������кܶ�ʵ�����ԣ���ǿ�����Գ���������ɱ���ͷ������ʡ�Ŀǰ��ȡ�����ķ����ܶ࣬���е��ηŵ編��DBD���͵�ⴿˮ��ԭ����ͼ��ʾ������˵���д�����ǣ� ��
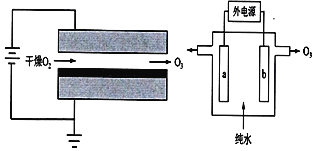
A.���ַ������ǽ�����ת��Ϊ��ѧ��
B.��ⴿˮʱ�����������ĵ缫��Ӧ��3H2O��6e����O3����6H��
C.���ηŵ編�͵�ⴿˮ����ȣ��������Ⱦ�Ե�NOx����
D.��ⴿˮʱ��H���ɵ缫b����缫a
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com