
【题目】某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
(提出假设)
假设1:沉淀为Cu(OH)2
假设2:沉淀为________
假设3:沉淀为碱式碳酸铜[化学式可表示为nCuCO3mCu(OH)2]
(查阅资料)无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
(物质成分探究)
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤。
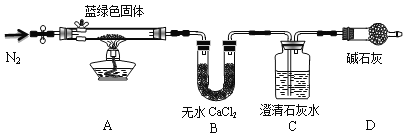
步骤2:甲同学取一定量固体,用气密性良好的下图装置(夹持仪器未画出)进行定性实验。请回答下列问题:
(1)假设2中的沉淀为________________。
(2)假设1中沉淀为Cu(OH)2的理论依据是____________________________________。
(3)无水乙醇洗涤的目的____________________________________________________。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设____(填写序号)成立。
(5)乙同学认为只要将上图中B装置的试剂改用_____________________试剂后,便可验证上述所有假设,装置D的作用是__________________________。
(6)乙同学更换B试剂后验证假设3成立的实验现象是_________________。
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2溶液代替C中澄清石灰水,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为____________________。
【答案】CuCO3 碳酸根水解,溶液中含有较多的OH—(或者答双水解,相互促进,或者写出双水解离子方程式或化学方程式均可) 利用乙醇的易挥发,带走洗涤的水 假设1 无水CuSO4 防止空气中二氧化碳进入C影响实验 A中蓝绿色固体变黑色,B中固体变蓝,C中有白色沉淀产生 2 CuCO33Cu(OH)2或3Cu(OH)22 CuCO3或Cu5 (OH)6(CO3)2
【解析】
CuSO4溶液与Na2CO3溶液混合产生蓝绿色沉淀,可能是反应生成了碳酸铜沉淀,也可能发生双水解生成了氢氧化铜沉淀,或是碱式碳酸铜;加热时,碳酸铜分解生成二氧化碳和黑色氧化铜,加热氢氧化铜时生成水蒸气和黑色氧化铜,可以通过验证水的存在和二氧化碳的存在来证明产生的物质成分,据此分析解答。
(1)CuSO4溶液与Na2CO3溶液混合产生蓝绿色沉淀,可能是反应生成了碳酸铜沉淀,或双水解生成了氢氧化铜沉淀,或是碱式碳酸铜,假设1中沉淀为Cu(OH)2,假设2为CuCO3,故答案为:CuCO3;
(2)Na2CO3溶液中碳酸根能水解,产生氢氧根离子,所以与CuSO4溶液混合产生的蓝绿色沉淀可能为氢氧化铜,故答案为:碳酸根水解,溶液中含有较多的OH-;
(3)所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤,可以洗去固体中残留的水分,通风晾干可以让乙醇完全挥发,故答案为:利用乙醇的易挥发,带走洗涤的水;
(4)加热时,碳酸铜分解生成二氧化碳和黑色氧化铜,二氧化碳能使澄清的石灰水变浑浊,加热氢氧化铜时生成水蒸气和黑色氧化铜,若反应后A中蓝绿色固体变黑,C中无明显现象证明一定不含有碳酸铜,则假设1正确,故答案为:1;
(5)实验验证碳酸铜或氢氧化铜是利用受热分解生成的产物性质验证,加热时,碳酸铜分解生成二氧化碳和黑色氧化铜,加热氢氧化铜时生成水蒸气和黑色氧化铜,所以需要验证水的存在和二氧化碳的存在就可以证明产生的物质成分,装置A中加热是否变化为黑色固体,装置B选择无水硫酸铜验证是否生成水,澄清石灰水是否变浑浊证明是否生成二氧化碳,所以要将上图中B装置的试剂改用无水CuSO4,装置D中的碱石灰可以防止空气中二氧化碳进入C影响实验,故答案为:无水CuSO4;防止空气中二氧化碳进入C影响实验;
(6)装置A中加热是否变化为黑色固体,装置B选择无水硫酸铜,是否变蓝色验证是否生成水,装置C中澄清石灰水是否变浑浊证明是否生成二氧化碳,所以证明假设3是否正确的现象为:A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生,故答案为:A中蓝绿色固体变黑色,B中无水CuSO4固体变蓝,C中有白色沉淀产生;
(7)B中吸收的是水,水的物质的量=![]() =0.15mol,C中吸收的是二氧化碳生成碳酸钡白色沉淀,根据碳原子守恒得二氧化碳的物质的量=
=0.15mol,C中吸收的是二氧化碳生成碳酸钡白色沉淀,根据碳原子守恒得二氧化碳的物质的量=![]() =0.1mol,氧化铜的物质的量=
=0.1mol,氧化铜的物质的量=![]() =0.25mol,则铜离子、氢氧根离子和碳酸根离子的物质的量之比=0.25mol∶0.3mol∶0.1mol=5∶6∶2,所以其化学式为:2CuCO33Cu(OH)2或3Cu(OH)22CuCO3或Cu5(OH)6(CO3)2,故答案为:2CuCO33Cu(OH)2或3Cu(OH)22CuCO3或Cu5(OH)6(CO3)2。
=0.25mol,则铜离子、氢氧根离子和碳酸根离子的物质的量之比=0.25mol∶0.3mol∶0.1mol=5∶6∶2,所以其化学式为:2CuCO33Cu(OH)2或3Cu(OH)22CuCO3或Cu5(OH)6(CO3)2,故答案为:2CuCO33Cu(OH)2或3Cu(OH)22CuCO3或Cu5(OH)6(CO3)2。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知可逆反应:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
A. 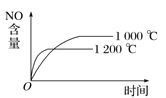 B.
B. 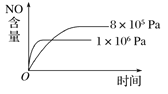
C. 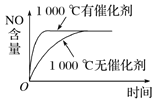 D.
D. 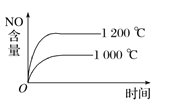
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别用浓度均为0.5 mol/L的NH3·H2O和NaOH溶液,滴定20 mL 0.01 mol/L Al2(SO4)3溶液,随滴定溶液体积的增大,溶液的导电能力变化曲线如图所示,下列说法中正确的是
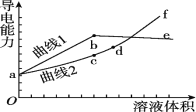
A. 曲线2 代表滴加NH3·H2O溶液的变化曲线
B. b和d点对应的溶液均显碱性
C. b点溶液中c(NH4+)>c(SO42-)>c(H+)>c(OH-)
D. d~f段导电能力升高的原因是发生了反应Al(OH)3+OH-===2H2O+AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol/L某一元酸(HA)溶液中c(H+)=1×10-3 mol/L,下列叙述正确的是( )
A. 该溶液中由水电离出的c(H+)=1×10-11 mol/L
B. 该一元酸溶液的pH=1
C. 该溶液中水电离的c(H+)=1×10-3 mol/L
D. 用pH=11的NaOH溶液V1 L和V2 L 0.1 mol/L该一元酸(HA)溶液混合,若恰好反应,则V1=V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示中,A为一种常见的单质,B、 C、 D、 E是含A元素的常见化合物,它们的焰色反应均为黄色。

请填写下列空白:
(1)写出化学式:A____________,B____________,D____________。
(2)以上反应中,属于氧化还原反应的有____________(填写编号)。
(3)A→C反应的离子方程式是____________________。
(4)E→D反应的化学方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,有![]() 盐酸;
盐酸;![]() 硫酸;
硫酸;![]() 醋酸三种酸的稀溶液
醋酸三种酸的稀溶液![]() 用a、b、c、
用a、b、c、![]() 、
、![]() 、
、![]() 号填写
号填写![]()
![]() 当其物质的量浓度相同时,
当其物质的量浓度相同时,![]() 由大到小的顺序是____________,
由大到小的顺序是____________,
![]() 同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是____________,
同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是____________,
![]() 当其
当其![]() 相同时,物质的量浓度由大到小的顺序为____________,
相同时,物质的量浓度由大到小的顺序为____________,
![]() 当
当![]() 相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气
相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气![]() 相同状况
相同状况![]() ,则开始时反应速率的大小关系是____________.
,则开始时反应速率的大小关系是____________.
![]() 将
将![]() 相同的三种酸均加水稀释至原来的10倍,
相同的三种酸均加水稀释至原来的10倍,![]() 由大到小的顺序为_____________.
由大到小的顺序为_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬醛的结构简式如图所示,主要用作柠檬和什锦水果型香精,也是合成紫罗兰酮的主要原料

(1)柠檬醛不能发生的反应类型为_____________(填字母)。
A.酯化反应 B.加成反应 C.氧化反应 D.消去反应
(2)香叶醇经催化氧化可制得柠檬醛,则香叶醇的结构简式为_____________
(3)双羟基香茅酸(![]() 也是一种重要的香料,可由柠檬醛合成,合成路线如下
也是一种重要的香料,可由柠檬醛合成,合成路线如下

双羟基香茅酸的分子式为________,写出A→B的化学方程式___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用阴离子交换膜和过滤膜制备高纯度的Cu的装置示意图,下列有关叙述不正确的是
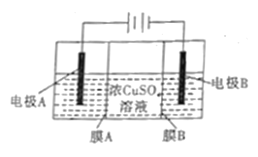
A. 电极A是粗铜,电极B是纯铜
B. 电路中通过1mol电子,生成32g铜
C. 溶液中SO42-向电极A迁移
D. 膜B是过滤膜,阻止阳极泥及杂质进入阴极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。

试回答下列问题(凡涉及的物质均用化学式表示):
(1)a的氢化物的分子构型为_________,中心原子的杂化形式为______;d的最高价氧化物分子构型为__________,中心原子的杂化形式为_______。
(2)g位于第________族,属于________区。写出其基态原子的电子排布式_____________________________。
(3)将f的无水硫酸盐溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配离子,请写出生成此配离子的离子方程式:_______________________________________。
(4)CH3+、—CH3、CH3— 都是重要的有机反应中间体,有关它们的说法正确的是___________。
A.它们均由甲烷去掉一个氢原子所得
B.它们互为等电子体,碳原子均采取sp2杂化
C.CH3—与NH3、H3O+互为等电子体,几何构型均为三角锥形
D.CH3+中的碳原子采取sp2杂化,所有原子均共面
E.两个—CH3或一个CH3+和一个CH3—结合均可得到CH3CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com