
【题目】某学生探究0.25 mol·L-1 Al2(SO4)3溶液与0.5 mol·L-1 Na2CO3溶液的反应,实验如下。下列分析错误的是
实验1 |
|
实验2 |
|
A. 实验1中,白色沉淀a是Al(OH)3
B. 实验2中,白色沉淀b中含有CO![]()
C. 检验白色沉淀a、b是否洗涤干净,不可使用相同的检验试剂
D. 实验1、2中,白色沉淀成分不同可能与混合后溶液的pH有关
【答案】C
【解析】
实验1在过量的硫酸铝溶液中加入碳酸钠溶液,过滤、洗涤,得到沉淀a,加入稀硫酸,沉淀溶解,没有气泡,说明沉淀a中含有Al(OH)3。
实验2在过量的碳酸钠溶液中加入硫酸铝溶液,过滤、洗涤,得到沉淀b,加入稀硫酸,沉淀溶解,并有少量气泡,说明沉淀b中含有Al(OH)3,同时含有碳酸盐。
A.由以上分析可知,实验1中白色沉淀a是Al(OH)3,故A项正确;
B.实验2中有气泡生成,该气体为二氧化碳,可说明白色沉淀b含有CO32-,故B项正确;C.最后溶液中均含有硫酸根离子,检验沉淀是否洗涤干净,都可通过检验硫酸根离子的方法,即用盐酸酸化的BaCl2溶液,观察是否有白色沉淀生成,故C项错误;
D.实验1、2中,加入试剂的顺序不同,溶液的pH不同,生成的沉淀不同,说明白色沉淀的成分与溶液的pH有关,故D项正确。
答案选C。


科目:高中化学 来源: 题型:
【题目】I.常温常压下,一氧化二氯(Cl2O)为棕黄色气体。沸点为3.8℃,当温度高于42℃时,分解生成Cl2和O2,Cl2O易溶于水并与水反应生成HClO。将氯气和空气(不参与反应)按照体积比1:3混合后,通入含水量为8%(质量分数)的碳酸钠中制备Cl2O,并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。

(1)仪器a的名称是 ________________。
(2)上述装置合理的连接顺序为 ___ →___ →___ → C →___ →(填装置下方的大写字母)。
(3)反应过程中装置B需要放在冷水中,其目的是________________________________。
(4)装置C的作用 __________________________________。
(5)制备Cl2O的化学方程式____________________________________________。
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点主要为_________________。
II.(7)探究NO与Na2O2反应的产物。
假设1:产物只有NaNO2;
假设2:__________;
假设3:产物为NaNO3和NaNO2的混合物。
为验证反应产物,该小组同学准确称取反应后的固体3.50 g,用煮沸并冷却后的蒸馏水配成100.00 mL溶液,取10.00 mL溶液于锥形瓶中,用0.200 0 mol·L-1KMnO4溶液(硫酸酸化)滴定,共消耗KMnO4溶液10 mL。滴定过程中发生反应的离子方程式为_______________,反应产物中NaNO2的质量分数为_________(保留四位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(X) | n(Y) | n(M) | |||
① | 700 | 0.40 | 0.10 | 0.090 | |
② | 800 | 0.10 | 0.40 | 0.080 | |
③ | 800 | 0.20 | 0.30 | a | |
④ | 900 | 0.10 | 0.15 | b | |
下列说法正确的是( )
A. 实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B. 实验②中,该反应的平衡常数K=2.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.060
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基乙酸(H2NCH2COOH)是蛋白质的水解产物之一,1 mol 的氨基乙酸中含有( )
A.2 mol氧气分子
B.12 mol氢原子
C.6.02×1023个H+
D.6.02×1023个氨基乙酸分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质长期露置于空气中会变质,且变质过程中涉及氧化还原反应的是
①Na ②NaOH ③FeSO4 ④氯水
A.①②B.②③C.①③④D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属冶炼的叙述中,不正确的是( )
A.电解铝时,以氧化铝—冰晶石熔融液为电解质,也常加入少量CaF2帮助降低熔点
B.电解铝时阴极碳块需定期更换
C.可利用铝热反应从V2O5中冶炼金属V
D.可用加热法从HgO中冶炼Hg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21。下列说法不正确的是
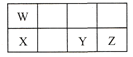
A.原子半径大小:X > Y > Z
B.W、Y两种元素都能与氧元素形成化合物WO2、YO2
C.氧化物对应水化物的酸性: Z > Y > W
D.Y能形成H2Y、H2YO4的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X是合成一种新型抗肝炎药的中间体,其生产路线如下:
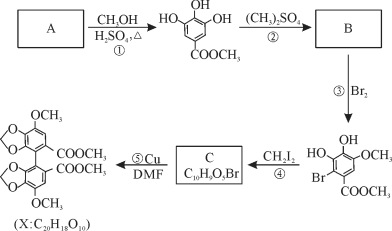
回答下列问题:
(1)反应①的反应类型为_____________。
(2)反应③的化学方程式为____________________________________________________。
(3)反应④生成C的结构简式为______________________,无机产物为_____(填化学式)。
(4)A有多种同分异构体,同时符合下列条件的有______种(不考虑立体异构)。请写出其中一种核磁共振氢谱有4组峰,且峰面积之比为2∶2∶1∶1的结构简式___________。
a.苯环上有4个取代基;
b.与FeCl3溶液发生显色反应;
c.能发生水解反应。
(5)参照上述合成路线及信息,以氯气、苯和一氯乙烯为原料(其它试剂任选),设计制备聚苯乙烯的合成路线____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,Cl-的物质的量浓度最大的是( )
A.300 mL0.1 mol/L NaCl溶液B.10 mL0.2 mol/LAlCl3溶液
C.标况下4.48LHCl气体配成的1 L溶液D.100 mL0.1 mol/LFeCl3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com