
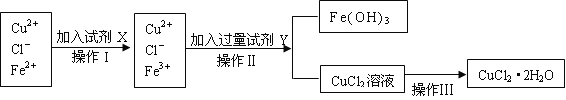
【题目】氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
请参照下表给出的数据填空。
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Cu2+ | 4.7 | 6.7 |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.7 |
(1)操作I加入X的目的是_________________。
(2)下列物质都可以作为X,适合本实验的X物质可以是(填选项)_________ 。
A、KMnO4 B、NaClO C、H2O2 D、Cl2
(3)操作II的Y试剂为____________(填化学式),并调节溶液的pH在______范围。
(4)实验室在配制CuCl2溶液时需加入少许_________(填物质名称),理由是(文字叙述并用有关离子方程式表示)_________________ __________。
(5)若将CuCl2溶液蒸干灼烧,得到的固体是_________________(填化学式);若要得无水CuCl2,请简述操作方法_________________________。
【答案】(1)加入氧化剂,使Fe2+氧化为Fe3+ (2)C、D
(3)CuO;3.7≤pH<4.7
(4)盐酸 Cu2+水解:Cu2++2H2O![]() Cu(OH)2+2H+ ,加入盐酸抑制其水解
Cu(OH)2+2H+ ,加入盐酸抑制其水解
(5)CuO,HCl气流中蒸发
【解析】
试题分析::1)分析流程和实验过程可知,操作Ⅰ加入X的目的是加入氧化剂,使Fe2+氧化成Fe3+;
(2)加入X的目的是氧化亚铁离子,加入的是氧化剂,能将Fe2+氧化为Fe3+,且易除去,除杂时,不能引入新的杂质,所以选项中:A.KMnO4 氧化剂加入会增加杂质离子,故A不符合:B.NaClO是氧化剂,但引入杂质钠离子,故B不符合;C.H2O2 做氧化剂没有增加新杂,故C符合;D.Cl2是氧化剂,反应过程中不引入新的杂质,故D符合;故答案为CD;
(3)分析图表数据结合题示,调节pH3.7~4.7,调节pH使Fe3+全部沉淀,同样不引进新杂质,所以Y最好为CuO或Cu(OH)2或CuCO3;
(4)CuCl2属于强酸弱碱盐,溶液中水解显酸性,加盐酸时抑制其水解,反应的离子方程式为:Cu2++2H2O![]() Cu(OH)2+2H+;
Cu(OH)2+2H+;
(5)CuCl2属于强酸弱碱盐,加热蒸发时促进其水解(HCl易挥发),生成Cu(OH)2沉淀,最后灼烧分解生成CuO,若要得到无水CuCl2,需要在HCl气氛中采用蒸发结晶的方法。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】Heck反应是偶联反应的一种,例如:反应①如下:
![]() +CH3OOCCH=CH2(Ⅰ)
+CH3OOCCH=CH2(Ⅰ)![]()
![]() (Ⅱ)
(Ⅱ)
化合物I可以由以下途径合成:
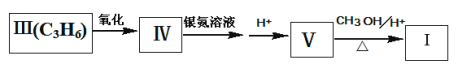
回答以下问题:
(1)化合物Ⅱ的分子式为_____,1mol该物质最多可与________molH2发生加成反应。
(2)卤代烃CH3CHBrCH3发生消去反应可以生成化合物Ⅲ,相应的化学方程式为: ________(注明条件)。
(3)分子式为C4H6O的化合物Ⅵ,满足以下条件:①与化合物IV互为同系物;②含有甲基且无支链,写出其结构简式________。
(4)一定条件下,![]() 与
与 ![]() 也可以发生类似反应①的反应,其有机产物的结构简式为__________。
也可以发生类似反应①的反应,其有机产物的结构简式为__________。
(5)设计一条以CH3CHClCHClCH3和![]() 为原料合成
为原料合成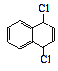 的路线_______。
的路线_______。
提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:(用合成路线流程图表示为:A![]() B……
B……![]() 目标产物)。
目标产物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组性质比较中,正确的是()
①沸点:![]()
②离子还原性:![]()
③酸性:![]()
④金属性:![]()
⑤气态氢化物稳定性:![]()
⑥半径:![]()
A.①②③B.③④⑤⑥C.②③④D.①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地球化学中,通常用热重分析研究矿物在受热时的质量变化以确定其组成。取66.6 mg由高岭石[Al4Si4O10(OH)8]和方解石(CaCO3)组成的矿物,加热到673K~1123K区间内分解为氧化物,样品总失重13.8 mg。高岭石受热分解反应方程式:Al4Si4O10(OH)8 →2Al2O3+4SiO2+4H2O
(1)硅原子核外电子排布在____个不同的电子层中,核外最外层电子分布在____个不同的轨道中。
(2)硅与铝同周期且相邻,化学性质有相似性,写出Si与NaOH溶液反应的化学方程式________。
(3)高岭石是长石的一种,不同类长石其氧原子的物质的量分数相同。由钙长石化学式CaAl2Si2O8可推知钠长石的化学式为_________________。
(4)此矿物中高岭石的质量分数为____________。
a. 44% b. 56% c. 77.5% d. 80%
(5)若对高岭土进行煅烧活化,然后利用盐酸进行分解,对于分解出的氯化铝溶液及二氧化硅再分别加入碱溶液进行去杂提纯,最后得到的氯化铝溶液可制备氧化铝。写出由氯化铝溶液得到纯净氧化铝的化学反应方程式(要求最节约):_____________________。
(6)用焦炭与石英砂(SiO2)混合高温,产生粗硅,现由两种方法将粗硅提纯:
第一种方法:Si+2Cl2 ![]() SiCl4 SiCl4+2H2
SiCl4 SiCl4+2H2![]() Si+4HCl
Si+4HCl
第二种方法:Si+3HCl ![]() SiHCl3 SiHCl3+H2
SiHCl3 SiHCl3+H2![]() Si+3HCl。
Si+3HCl。
工业上常用第二种方法来提纯单晶硅,其原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三份不同质量的硫化铜与硫化亚铜的混合物样品①②③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中硫化铜的量。
(1)甲取2.56克样品①,置于空气中加强热,产物为氧化铜和二氧化硫。若产生0.448 L气体(标准状况),该气体被30 mL一定浓度氢氧化钠恰好完全吸收,将所得溶液小心低温蒸干得固体2.3克。则样品①中硫化铜的质量为_____g,氢氧化钠浓度_______mol·L-1;
(2)乙取3.52克样品②,投入过量的浓硝酸中加热,充分反应后,样品全部参与反应,溶液失重8.44克。样品②中硫化铜的物质的量为____mol;若浓硝酸的浓度为14.2 mol·L-1,则反应消耗浓硝酸____mL。(已知:Cu2S+14HNO3→2Cu(NO3)2+10NO2↑+H2SO4+6H2O)
(3)丙称量样品③强热后剩余的固体质量比原样品减小了a g,若该固体为氧化铜,则样品③中硫化铜物质的量(n)为_________mol。若要计算硫化亚铜的质量,则缺少_____________数据,若设该数据为b克,则硫化亚铜的质量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水存在H2O![]() H++OH--Q的平衡,下列叙述一定正确的是( )
H++OH--Q的平衡,下列叙述一定正确的是( )
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B.将水加热,Kw增大,pH减小
C.向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低
D.向水中加入少量固体硫酸钠,c(H+)=10-7mol/L,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列物质变化,所得能量变化关系正确的是
物质变化 | 能量关系 | |
A | 将充满NO2的针筒置于热水中,气体颜色变深 | 1molN2O4(g)的能量>2molNO2(g)的能量 |
B | 将NaOH溶液与HCl溶液混合 |
|
C | 1g气态SiH4在空气中燃烧,生成SiO2 (s)与液态水,放热44.6kJ | SiH4(g)+2O2(g)→SiO2(s)+2H2O(l)+44.6kJ |
D | 合成氨:N2(g)+3H2(g) | 反应物的总键能>生成物的总键能 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述不正确的是( ).
A.在滴有酚酞的 Na2CO3溶液中慢慢滴入BaCl2溶液至过量,溶液的红色褪去
B.往Na2CO3溶液中加水,![]() 增大
增大
C.pH相同的①NH4Cl、②NH4Al (SO4)2、③NH4HSO4三种溶液中c(NH4+):①>②>③
D.在水电离出的c(H+)=1×10-12 mol/L的溶液中,Al3+一定不可能大量存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨水是氨气的水溶液,主要用作化肥。现有25℃时0.1 mol/L的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中的c(NH4+)_________,溶液的pH_________(填“增大”“减小”“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:____________;所得溶液的pH_________7(填“>”、“<”或“=”),用离子方程式表示其原因________。
(3)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺是_______
(4)实验室可用向浓氨水中加入CaO的方法制取氨气,从氨水中存在的平衡入手分析产生NH3的原因:__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com