
【题目】某学生为确定某烃的分子式及其可能的结构简式,做了如下实验:标准状况下,取0.1 mol该烃,在氧气中完全燃烧,生成的二氧化碳体积为22.4 L,同时得到16.2 g水。
(1)该烃的摩尔质量为________。
(2)该烃的分子式为________。
(3)该烃有一种可能的结构为  ,属于________(选填序号)。
,属于________(选填序号)。
A.环烃 B.烷烃 C.芳香烃 D.不饱和烃
科目:高中化学 来源: 题型:
【题目】把镁条直接投入到盛有盐酸的敞口容器中,产生H2的速率如图所示,
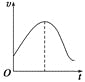
在下列因素中,影响反应速率的因素是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A. ①④B. ③④C. ①②③D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
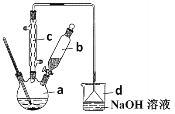
【题目】溴苯是一种化工原料,实验室合成溴苯装置图及有关数据如下:
项目 | 苯 | 溴 | 溴苯 |
密度/(g·cm-3) | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴。仪器c的名称是____________,其进水口为_____(填“上”或“下”)口,装置d中倒置漏斗作用为________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是_______。
③向分出的粗溴苯中加入少量的无水硫酸镁,静置、过滤。
(3)经以上分离操作后,要进一步提纯,下列操作中必需的是____(填入正确选项前的字母):
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)将d中的NaOH溶液换成硝酸银溶液,则出现的现象为_____________,该现象_____(填“能”或“不能”)说明该反应为取代反应。
解决(3)时用到题干中的哪些信息_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究实验室制乙烯及乙烯和溴水的加成反应:甲同学设计了如图所示的实验装置,并进行了实验。当温度升至170℃左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速褪去。甲同学认为达到了实验目的。乙同学仔细观察了甲同学的整个实验过程,发现当温度升到100℃左右时,无色液体开始变色,到160℃左右时,混合液全呈黑色,在170℃超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:

(1)写出甲同学实验中认为达到实验目的的两个反应的化学方程式:__________________。
(2)乙同学观察到的黑色物质是__________,刺激性气体是__________。乙同学认为刺激性气体的存在就不能认为溴水褪色是乙烯的加成反应造成的。原因是(用化学方程表示):________________________________ 。
(3)丙同学根据甲乙同学的分析,认为还可能有CO、CO2两种气体产生。为证明CO存在,他设计了如下过程(该过程可把实验中产生的有机产物除净):发现最后气体经点燃是蓝色火焰,确认有一氧化碳。
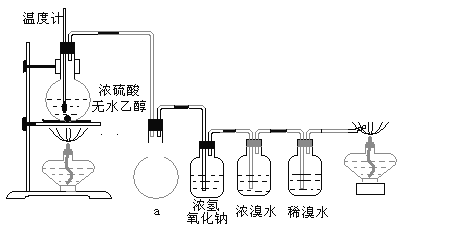
①设计装置a的作用是_____________________________________________
②浓溴水的作用是_________________________________________________,
稀溴水的作用是___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是巨大的资源宝库,除了可以得到氯化钠还可以从海带中提取碘。碘是人 体不可缺乏的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定 量的 KIO3 进去。某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其 检测原理是:KIO3+5KI+3H2SO4=3I2+3H2O+3K2SO4
(1)氧化产物与还原产物的物质的量比是_____;如果反应生成 0.3mol 的单质碘,则转 移的电子数目是_____。
(2)先取少量的加碘盐加蒸馏水溶解,然后加入稀硫酸和 KI 溶液,最后加入一定量的 CCl4, 振荡,这时候,观察到的现象是_____。
(3)若采用下图实验装置将四氯化碳和 I2 的混合溶液分离。
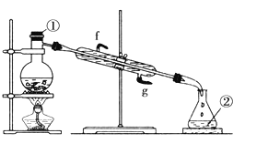
该装置还缺少的仪器是_______;冷凝管的进水口是:_______ (填 g 或 f)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实所对应的离子方程式正确的是
选项 | 事实 | 离子方程式 |
A | 向酸性 |
|
B | 硫代硫酸钠溶液中滴加盐酸,有淡黄色沉淀产生 |
|
C | 明矾溶液中加入 |
|
D | 碘化亚铁溶液中滴加少量溴水,溶液变为黄色 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。
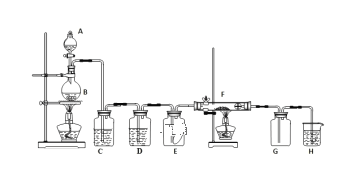
(1)装置C中盛装的溶液是___,D中试剂的作用是___。
(2)写出F中反应的化学反应方程式:__ ,其反应现象为___。
(3)H中的试剂为____,用来吸收多余氯气。该反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下列材料后回答有关问题
一个体重50kg的健康人,体内含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4),服用维生素C可使食物中的Fe转化成Fe2+,有利于人体对铁的吸收
(1)人体中经常进行Fe2+与Fe3+的转化,在此转化过程中,Fe2+作_______剂(填氧化或还原,下同),被__________
(2)“服用维生素C可使食物中的Fe3+转化为Fe2+这句话说明,维生素C在这个反应中作____剂(填氧化或还原,下同),具有_______性
(3)补血剂的主要成分是FeSO4请写出产物有FeSO4的符合要求的化学方程式:
①置换反应:__________________________
②复分解反应:__________________________
(4)有人在研究硫酸亚铁(FeSO4)热稳定性时,作出了两种假设
①假设它按CaCO3受热分解的方式分解,反应的化学方程式为_________________________
②假设它按KClO3受热分解的方式分解,已知产物都是氧化物,其中有两种酸性氧化物生成,则分解反应的化学方程式为____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合图回答问题:如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
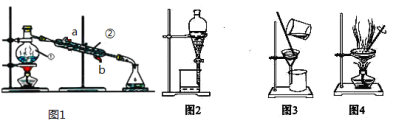
(1)写出上述装置中仪器的名称:①________。
(2)若利用上述装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________,图1中仪器 ②是从______口进水(填a或b)。
(3)图2在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______
(4)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的序号,下同);除去自来水中的Cl等杂质,选择装置______。
(5)实验室常用上述装置分离碘水中的碘,进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________(填序号)。
①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com