
【题目】查耳酮常用作有机合成试剂和指示剂,其结构如图所示。下列说法错误的是( )

A.查耳酮的分子式为C15H12O
B.查耳酮分子中所有的碳原子可能共平面
C.查耳酮能发生加聚反应制备高分子
D.查耳酮的同分异构体中含有碳氧双键、碳碳双键且两苯环不直接相连的共有6种(不考虑立体异构)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有关甲、乙、丙、丁四个图示的叙述不正确的是( )
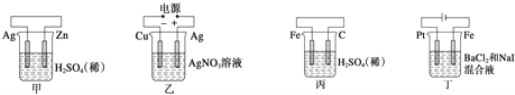
A.甲中负极反应式为![]()
B.乙中阳极反应式为![]()
C.丙中![]() 向碳棒方向移动
向碳棒方向移动
D.丁中电解开始时阳极产生黄绿色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是具有紫色光泽的粉末,是一种高效绿色强氧化剂,碱性条件下稳定,可用于废水和生活用水的处理。实验室以石墨和铁钉为电极,以不同浓度的NaOH溶液为电解质溶液,控制一定电压电解制备高铁酸钠,电解装置和现象如下:
c(NaOH) | 阴极现象 | 阳极现象 |
1 mol·L-1 | 产生无色气体 | 产生无色气体,10min内溶液颜色无明显变化 |
10 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,3min后溶液变为浅紫红色,随后逐渐加深 |
15 mol·L-1 | 产生大量无色气体 | 产生大量无色气体,1min后溶液变为浅紫红色,随后逐渐加深 |
下列说法不正确的是

A. a为铁钉,b为石墨
B. 阴极主要发生反应:2H2O + 2e-=== H2↑+ 2OH-
C. 高浓度的NaOH溶液,有利于发生Fe-6e-+ 8OH-=== FeO42-+ 4H2O
D. 制备Na2FeO4时,若用饱和NaCl溶液,可有效避免阳极产生气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是______。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)______。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为______。
②完成NaClO3氧化FeCl2的离子方程式:
___![]() +___Fe2++___=___Cl+___Fe3++__
+___Fe2++___=___Cl+___Fe3++__
(3)FeCl3在溶液中分三步水解:
Fe3++H2O![]() Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O![]()
![]() +H+ K2
+H+ K2
![]() +H2O
+H2O![]() Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是__________。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:xFe3++yH2O![]() Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号)______。
Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号)______。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是___。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为_____mg·L-1。
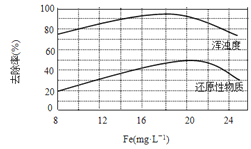
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气是城市主要污染之一,治理的一种办法是在汽车排气管上装催化转化器,它使一氧化氮与一氧化碳反应生成可参与大气生态循环的无毒气体,并促使烃类充分燃烧及二氧化硫的转化,下列说法错误的是
A. 一氧化氮与一氧化碳反应的化学方程式为2CO+2NO![]() 2CO2+N2
2CO2+N2
B. 此方法的缺点是由于二氧化碳的增多,会大大提高空气的酸度
C. 为减少城市污染应开发新能源
D. 汽车尾气中有两种气体与血红蛋白结合而使人中毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol·L-1的盐酸滴定10mL0.1mol·L-1的Na2SO3溶液,滴定曲线如图所示(不考虑滴定过程中SO2的逸出)。下列说法错误的是( )

A.a点由水电离出的氢离子浓度大于d点由水电离出的氢离子浓度
B.0.05mol·L-1NaHSO3溶液的pH=4.25
C.c点时,c(Na+)>c(Cl-)>c(HSO![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.d点时,c(H2SO3)>c(HSO![]() )>c(SO
)>c(SO![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃分子的球棍模型(如图),据此回答下列问题:
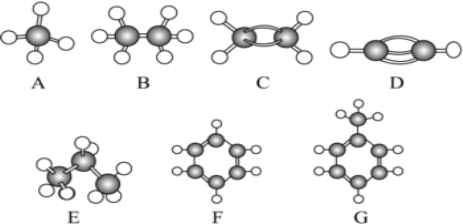
(1)常温下含氢量最高的烃是(填对应字母)________________;
(2)能够发生加成反应的烃有(填数字)________种;
(3)写出A失去一个氢原子形成的甲基的电子式______________________;
(4)F与浓硝酸和浓硫酸的混酸水浴加热生成的有机产物的名称为____________
(5)上述物质中互为同系物的是______________________或_______________(填对应字母)
(6)D与等物质的量溴反应的化学方程式为_________________所得产物的名称为____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。如图是氟离子电池工作示意图,其中充电时F-从乙电极流向甲电极,下列关于该电池的说法正确的是( )

A.放电时,甲电极的电极反应式为Bi-3e-+3F-=BiF3
B.放电时,乙电极电势比甲电极高
C.充电时,导线上每通过1mole-,甲电极质量增加19g
D.充电时,外加电源的正极与乙电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个烧瓶中分别充满NO2气体并分别放置在盛有下列物质的烧杯(烧杯内有水)中:在(1)中 加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1))中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )
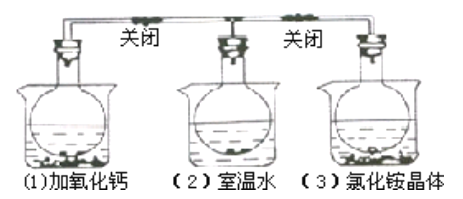
A. 2NO2![]() N2O4是放热反应
N2O4是放热反应
B. NH4Cl溶于水时放出热量
C. 烧瓶(1)中平衡混合气的平均相对分子质量增大
D. 烧瓶(3)中气体的压强增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com